Лекарства для лечения фибрилляции предсердий
Целью лечения пациентов с фибрилляцией предсердий (ФП) служит снижение риска тромбоэмболии (ТЭ) и осуществление контроля над симптомами. Последнее выполняют путем контроля желудочкового ритма во время ФП и/или восстановления и поддержания синусового ритма. В настоящее время не выявлены преимущества одной стратегии перед другой (контроль ЧСЖ или контроль ритма), в частности, потому, что ААП эффективны только на 50-70% и несут риск развития проаритмий.
Результаты крупномасштабных клинических исследований, например AFFIRM, PI AF (Pharmacologic Intervention in Atrial Fibrillation) и RACE (Rate Control versus Electrical Cardioversion), показали, что обе тактики лечения имеют право на существование. Во время AFFIRM, самого крупного из этих исследований, 4060 пациентов с ФП и ФР развития ТЭ были разделены на 2 группы: в одной осуществляли контроль над ритмом, а в другой — над ЧСЖ с применением стандартных фармакологических подходов. Исследование не выявило разницы в показателях смертности или качестве жизни.
В обеих группах тромбоэмболия (ТЭ) происходила в случае отмены антикоагулянтов. Эти исследования сравнивали тактики лечения, но не сравнивали синусовый ритм с ФП на фоне контроля ЧСЖ. В исследовании AFFIRM только 60% пациентов с контролем над ритмом сохранили синусовый ритм при повторных осмотрах. Также осуществлялся тщательный мониторинг на предмет рецидивов ФП между осмотрами.
Общая тактика лечения (т.е. контроль над ЧСЖ или восстановление и поддержание синусового ритма) должна подбираться индивидуально в каждом случае на основании того факта, появляются ли симптомы у пациентов в связи с отсутствием контроля над ЧСЖ или из-за самой ФП (т.е. потеря АВ-синхронности и отсутствие сокращений предсердий), а также в зависимости от риска возникновения побочных эффектов при приеме ААП. Иногда сложно определить, вызваны ли симптомы высокой ЧСЖ или отсутствием сокращений предсердий. Существует общее правило, по которому бессимптомным пациентам, у которых ФП была выявлена в ходе проведения стандартной ЭКГ, контроль над ритмом не требуется, достаточно осуществлять контроль над ЧСЖ.
В этом случае может помочь амбулаторный мониторинг, коррелирующий желудочковый ответ пациентов и ритм с симптомами, а также проведение нагрузочных тестов. Иногда для окончательного решения необходимо провести исследование с активным контролем ЧСЖ или выполнить КВ с поддержанием синусового ритма. Непереносимость медицинских препаратов или повышенный риск при выбранной тактике лечения может заставить изменить тактику. Нужно помнить, что тактика контроля нал ритмом не может заменить антикоагулянтную терапию для снижения риска развития инсульта.
Многие пожилые пациенты хорошо переносят ФП без лечения, т.к. у них в результате сопутствующей недостаточности АВ-узла ЧСЖ низкая. У этих пациентов также присутствует синдром слабости синусового узла, и развитие ФП является своего рода лечением. У таких пациентов после КВ могут наблюдаться тяжелая наджелудочковая либо желудочковая аритмия и асистолия, поэтому возможность восстановления и поддержания синусового ритма нужно противопоставлять риску при проведении КВ или других форм терапии.

а) Неотложное лечение фибрилляции предсердий. Пациента с впервые выявленной ФП следует обследовать для выявления причины (ТТ, стеноз МК, легочная эмболия или перикардит). Клинический статус пациента обусловливает выбор первоначального лечения: замедление ЧСЖ и/или восстановление сокращения предсердий. Если острый приступ ФП с высокой ЧСЖ приведет к острой сердечно-сосудистой декомпенсации, методом выбора становится электрическая КВ. В других случаях решение о назначении КВ основывается на конкретной клинической ситуации. Необходимость восстановления синусового ритма следует противопоставить вероятности успешной КВ и длительному поддержанию синусового ритма.
Поддержание синусового ритма после КВ зависит от длительности ФП и степени дилатации предсердия (у некоторых больных). Исследования на животных показали, что ФП порождает ФП — чем дольше у пациента ФП, тем выше вероятность, что она сохранится в связи с процессом электрофизиологического ремоделирования. Такие же электрофизиологические аномалии можно обнаружить у пациентов после коротких приступов ФП, но механизм(ы) и клиническая значимость не ясны. Несмотря на то что размер предсердия и длительность ФП предопределяли успех КВ в ходе популяционного исследования, расширенное предсердие и длительная ФП не являются абсолютными противопоказаниями проведения КВ. Внутриполостная катетерная КВ может помочь в случае неудачи трансторакальной КВ, в частности, у пациентов с ожирением или у людей с тяжелой легочной патологией.
Однако с появлением двухфазных внешних дефибрилляторов процент успеха и результаты проведения КВ улучшились, а необходимость в проведении внутриполостной катетерной КВ снизилась. В качестве альтернативы перед процедурой можно применить ААП, снижающие порог дефибрилляции, например ибутилид, и таким образом повысить успешность КВ постоянным током. Сокращение предсердий может не восстановиться сразу после восстановления электрической систолы, а клиническое улучшение может произойти позднее. КВ постоянным током восстанавливает нормальный синусовый ритм в 90% случаев, но синусовый ритм сохраняется в течение 12 мес только в 30-50% наблюдений.
У пациентов с ФП в течение < 12 мес больше шансов на сохранение синусового ритма после КВ. Пациентам, которым не требуется неотложного проведения КВ, в 35-75% случаев может помочь химическая КВ путем в/в введения ААП. Несмотря на то что прокаинамид широко применяли в клинической практике долгое время, контролируемых исследований его эффективности проведено не было. За пределами США с хорошими результатами применяют флекаинид в/в. Оказывается, амиодарон в/в менее эффективен, разницы между его применением и плацебо нет.
Ибутилид в/в также эффективен в 35-75% случаев, в зависимости от популяционного исследования. В отсутствие декомпенсации у пациента можно использовать такие препараты, как дигиталис, β-АБ или антагонисты кальция, с целью поддержания максимальной ЧСЖ 60-80 уд/мин в покое, чтобы после легкой ФН она не превышала 100 уд/мин. Комбинация дигиталиса и β-АБ или антагонистов кальция может способствовать замедлению ЧСЖ. Дигиталис для осуществления контроля ЧСЖ становится более эффективным при наличии дисфункции ЛЖ; если дисфункция отсутствует, лучше применять β-АБ.
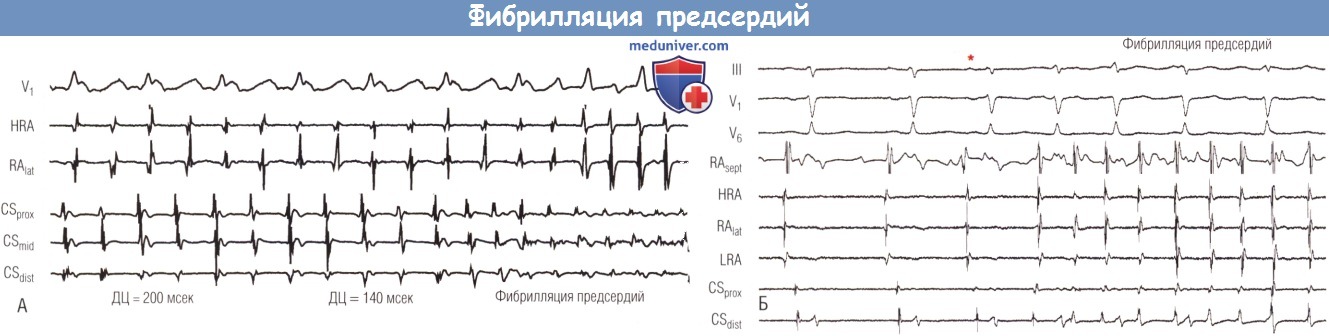
(А) Быстрая регулярная предсердная тахикардия (слева) с длиной цикла (ДЦ) 200 мсек переходит в фибрилляцию предсердий (справа),
которая характеризуется быстрой нерегулярной деполяризацией предсердий.
(Б) ППК (*) вызывает фибрилляцию предсердий (справа). Устранение фокальных триггеров фибрилляции предсердий может устранить фибрилляцию предсердий.
III, V1, V6 — поверхностные отведения; CSdist — дистальная область коронарного синуса;
CSmid — средняя область коронарного синуса; CSprox — проксимальная область коронарного синуса;
HRA — верхняя часть правого предсердия; LRA — нижняя часть правого предсердия;
RAlat — латеральная часть правого предсердия; RAsept — септальная часть правого предсердия.
б) Длительное лечение фибрилляции предсердий. Придерживаясь тактики контроля частоты сокращений желудочков (ЧСЖ), можно применять дигиталис, антагонисты кальция (дилтиазем и верапамил) и β-АБ по отдельности или в комбинации. При постоянном лечении дигиталиса обычно недоста точно для адекватного контроля над ЧСЖ во время периодов повышенного напряжения. Не следует ориентироваться на ЧСС в покое во время однократного осмотра. Подтвердить адекватность контроля нал ЧСС во время ФН помогут амбулаторный мониторинг и/или нагрузочные пробы.
У некоторых пациентов с частыми рецидивами и высокой ЧСЖ, не поддающимися контролю лекарственными препаратами, или у пациентов с непереносимостью ЛС для осуществления контроля над частотой сокращений можно изменить или устранить АВ-узловую проводимость методом катетерной РЧА или имплантацией частотночувствительного искусственного водителя ритма с режимом VVI. Если это возможно, то предпочтительнее предсердные или двухкамерные ИВР, т.к. при них частота ФП и инсультов снижена по сравнению с ИВР с режимом VVI.
Если было принято решение поддерживать синусовый ритм, то для купирования острых приступов ФП и профилактики рецидивов ФП можно использовать препараты класса IA, IC и III. Ни один из препаратов не доказал свое преимущество, поэтому выбор обычно основывается на возможности развития ПЭ и риске появления проаритмий. Это также относится к новым препаратам — азимилиду и дофетилиду, хотя сравнительные исследования еще не проведены. Большинство ААП повышают вероятность поддержания синусового ритма у 30-70% пациентов в год после проведения КВ. Некоторые относительно новые данные свидетельствуют о том, что соталол менее эффективен, чем амиодарон или другие препараты класса IC. Препараты класса IА обычно плохо переносятся пациентами, поэтому их редко используют при длительном лечении ФП.
Пациенты без структурной патологии сердца хорошо переносят препараты класса IC (пропафенон и флекаинид), поэтому эти препараты являются препаратами первого выбора при поддержании синусового ритма. Для пациентов со структурной патологией сердца препаратами первого выбора для поддержания синусового ритма являются амиодарон, дофетилид и соталол. В некоторых случаях эти препараты (особенно класса IC) могут «переводить» ФП в ТП, которое может иметь меньшую частоту на фоне препаратов. У этих пациентов для поддержания синусового ритма может быть эффективной аблация ТП и поддержание результата с помощью ААП (эффективность 80%). До проведения электрической КВ часто назначают ААП на несколько суток с целью возвращения синусового ритма и профилактики рецидивов ФП.
Для некоторых пациентов с редкими эпизодами персистирующей ФП (требующей проведения КВ) эффективна тактика «таблетка в кармане». Таким пациентам обычно назначают флекаинид или пропафенон в высокой дозировке после развития приступа ФП с целью его купирования. У пациентов, которым не подошла лекарственная терапия, с успехом применяют катетерную РЧА, цель которой — изоляция легочных вен или аблация широкой области сзади ЛП вокруг ЛВ. Данная тактика была эффективна в 70-85% случаев у пациентов с пароксизмальной ФП и у 50-70% пациентов с постоянной ФП в краткосрочных наблюдательных исследованиях. Хирургическую процедуру Maze применяют с целью устранения ФП, часто в комбинации на клапанах сердца, с высоким процентом успеха.
Новейшие хирургические техники с использованием специально разработанных инструментов (например, РЧ-скрепка, криоаблация, РЧ-ручка, высокочастотный ультразвук) замещают традиционную процедуру Maze, что позволяет провести более быстрое вмешательство через ограниченное число разрезов.
- Читать "Симптомы трепетания предсердий и ее диагностика по ЭКГ"
Оглавление темы "Аритмии сердца":- Что такое нормальный синусовый ритм?
- Классификация тахиаритмий и их краткая характеристика в таблице
- Симптомы синусовой тахикардии и ее диагностика по ЭКГ
- Лекарства для лечения синусовой тахикардии
- Преждевременные предсердные комплексы на ЭКГ и ее лечение
- Диагностика фибрилляции предсердий по ЭКГ
- Симптомы фибрилляции предсердий и ее клиника
- Лекарства для лечения фибрилляции предсердий
- Симптомы трепетания предсердий и ее диагностика по ЭКГ
- Лечение трепетания предсердий - предсердной тахикардии re-entry
