Причины и механизмы развития re-entry
Электрическая активность во время каждого нормального сердечного цикла начинается в синусовом узле (СУ) и продолжается до полной активации сердца. Клетки активируются поочередно, и, когда все волокна разрядятся и станут полностью рефрактерными (невозбудимыми), сердечный импульс затухает. Во время периода абсолютной рефрактерности сердечному импульсу «некуда двигаться».
Он должен быть погашен и возобновлен за счет следующего синусового импульса. Однако, если группа волокон не активируется в течение начальной волны деполяризации, возбудимость восстанавливается на такой промежуток времени, чтобы разрядиться прежде, чем затухнет импульс.
Группа волокон может служить соединительным мостиком для нового возбуждения тех участков, которые только что разрядились и восстанавливаются после начальной деполяризации. Этот процесс имеет разные названия, но смысл их одинаков — re-entry, возвратное возбуждение, циркуляция волны возбуждения, реципрокное или эхо-сердцебиение, реципрокная тахикардия.
а) Феномен вхождения. Феномен вхождения в тахикардию (т.е. увеличения скорости тахикардии путем кардиостимуляции) с восстановлением истинной скорости тахикардии после окончания кардиостимуляции закончится, что позволяет установить наличие re-entry.
Вхождение представляет собой захват или длительный возврат в исходное положение реципрокного тока тахикардии путем активации, вызванной кардиостимулятором. При каждом сердечном стимуле создается волновой фронт, который движется антероградно (ортодромно) и восстанавливает тахикардию до ритма кардиостимулятора.
Волновой фронт, распространяющийся ретроградно в противоположном направлении (антидромно), сталкивается с ортодромной волной предыдущего сокращения.
При взаимодействии волновых фронтов появляются электрографические и электрофизиологические особенности, которые можно объяснить только механизмом re-entry, поэтому критерии вхождения можно использовать для подтверждения реципрокного механизма клинической тахикардии и определения основ локализации источников тахикардии (путей движения волнового фронта) для лечения с помощью аблации.
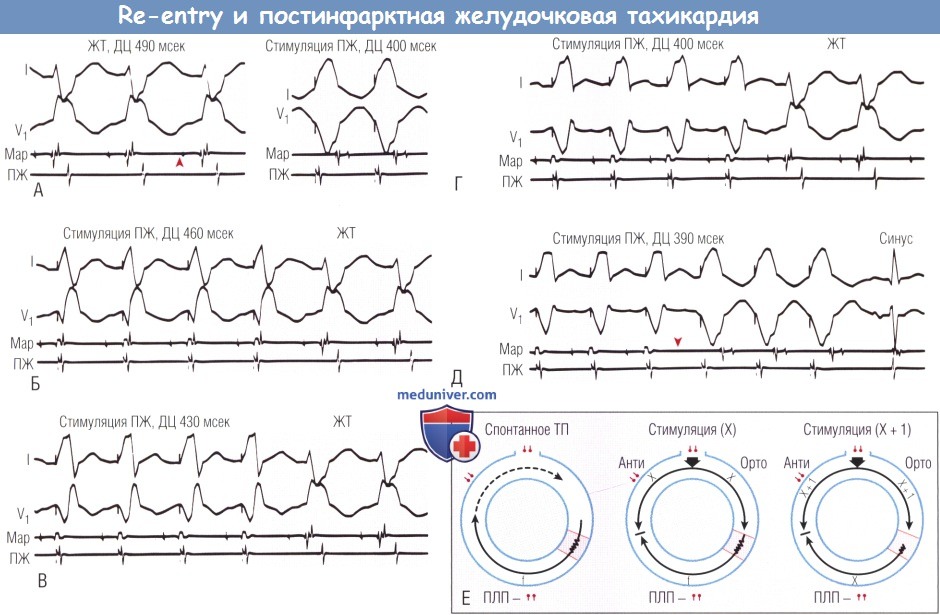
(А) Слева. Два отведения ЭКГ с ЖТ и внутрисердечная запись с катетера для картирования (Мар) в участке левого желудочка, критичного для поддержания ЖТ, как и из верхушки правого желудочка (ПЖ).
Отмечен диастолический потенциал (острие стрелки) во время ЖТ. Подобным образом организованы записи во всех последующих примерах.
(А) Справа. Стимуляция ПЖ при синусовом ритме. (Б) При стимуляции ПЖ с длиной цикла (ДЦ) немного короче,
чем ЖТ, возникают комплексы QRS, которые представляют собой сочетание ЖТ и полностью навязанных комплексов (слияние).
Все записи ускорены до стимулируемой ДЦ, после прекращения стимуляции возвращается та же ЖТ.
Все сливные комплексы идентичны, последнее сокращение навязанное, но поверхностное слияние отсутствует.
(В) и (Г) Тот же феномен, но с более короткой ДЦ при стимуляции. Стоит отметить, что сливной комплекс больше похож на комплекс стимуляции, чем на ЖТ при укорочении ДЦ.
(Б-Г) Прогрессирующее слияние зубцов на ЭКГ. Запись картирования с (Б) по (Г) также свидетельствуют о нарастании наслоения и изменений зубцов ЭКГ как по структуре, так и по времени при быстрой стимуляции.
(Д) Все еще короткая ДЦ при стимуляции приводит к неожиданным изменениям как на электрограмме картирования (блок в небольшом диастолическом потенциале, острие стрелки),
так и на поверхностной ЭКГ, которая полностью стимулируется. Когда стимуляция прекращается, ЖТ также прекращается.
(Е) Схематичное представление контура re-entry во время спонтанного трепетания предсердий (ТП) преходящего захвата цикла при ТП.
Слева. Контур re-entry при спонтанном ТП типа 1, f — циркулирующий волновой фронт ТП. В середине.
Введение первого стимулирующего импульса (X) при частой стимуляции из верхней части ПП при ТП.
Большая стрелка указывает вход стимулирующего импульса в контур re-entry, сразу после этого он проводится ортодромно (Орто) и антидромно (Анти).
Антидромный волновой фронт стимулирующего импульса (X) сталкивается с предыдущим, в данном случае с циркулирующим волновым фронтом спонтанного ТП (f), что приводит к слиянию предсердных импульсов и купированию ТП.
Ортодромный волновой фронт стимулирующего импульса (X) поддерживает тахикардию и перезапускает ее до стимулируемого ритма.
Справа. Введение следующего стимулирующего импульса (X + 1) во время частой стимуляции в той же верхней части предсердия.
Большая стрелка указывает на вход стимулирующего импульса в контур re-entry, сразу после чего он проводится ортодромно и антидромно.
Снова антидромный волновой фронт от стимулирующего импульса (X + 1) сталкивается с ортодромным волновым фронтом предыдущего импульса.
В этом случае именно ортодромный волновой фронт предыдущего стимулирующего импульса (X) и формирует предсердный сливной комплекс (сокращение).
Ортодромный волновой фронт от стимулирующего импульса (X + 1) поддерживает тахикардию и перезапускает частоту до стимулируемого ритма.
Во всех трех рисунках стрелки указывают направление распространения импульса; волнистая стрелка указывает на область медленного проведения (обозначена пунктиром) в контуре re-entry, красные точки обозначают биполярные электроды в области стимуляции в верхней части предсердия, переднезаднюю часть ЛП (ПЛП) и другие части предсердия.
I, V1 — поверхностные отведения.
б) Анатомическое re-entry. В ранних исследованиях механизма re-entry использовались модели с анатомически определенными отдельными путями, на которых были показаны:
(1) области с однонаправленным блоком;
(2) рециркуляция импульса к точке его начала;
(3) прекращение аритмии при пересечении этого патологического пути.
В моделях с анатомически определенными путями из-за наличия двух (или более) путей с разными электрофизиологическими характеристиками (например, рефрактерный период одного пути длиннее, чем рефрактерный период второго пути) импульс сначала блокируется в одном пути и затем медленно распространяется на прилежащий путь.
Если проведение по этому дополнительному пути достаточно подавлено, медленно распространяющийся импульс возбуждает ткань под блокированным путем (область с горизонтальными линиями) и возвращается в обратном направлении по пути, который был блокирован первым, чтобы передать возбуждение участкам ткани, располагающимся проксимально от области блока. Клинически аритмия, развившаяся по механизму re-entry, скорее всего, является мономорфной.
Для возникновения re-entry этого типа время проведения по подавленной, но не заблокированной области и для возбуждения дистальных сегментов должно превышать рефрактерный период первого блокированного пути и миокарда, расположенного проксимально к области блока. Другой путь поддержания контура re-entry требует анатомической протяженности пути, равной или превосходящей длину волны re-entry.
Последняя равна средней скорости проведения импульса, умноженной на самый длинный рефрактерный период элементов контура re-entry. Оба значения могут быть разными в различных участках вдоль пути re-entry; таким образом, показатели длины волны являются чем-то искусственным.
в) Условия формирования контура re-entry. Длина пути фиксирована и определяется анатомическими особенностями. Условия, подавляющие скорость проведения или сокращающие рефрактерный период, способствуют формированию контура re-entry в этой модели, в то время как удлинение периода рефрактерности и увеличение скорости проведения препятствуют формированию контура re-entry.
Например, если показатели скорости проведения (0,30 м/сек) и периода рефрактерности (350 мсек) для миокарда желудочков являются нормальными, для возникновения re-entry необходим путь длиной в 105 мм (0,30 м/сек х 0,35 сек). Тем не менее в определенных условиях скорость проведения по миокарду желудочков и волокнам Пуркинье может быть очень медленной (0,030 м/сек), и, если рефрактерный период не сильно увеличен (600 мсек), длина пути re-entry может быть всего 18 мм (0,030 м/сек х 0,60 сек).
Такое re-entry чаще всего представляет собой интервал возбудимости — временной интервал между концом периода рефрактерности одного цикла и началом деполяризации следующего, когда ткань возбудима. Это условие следует из того, что длина волны контура re-entry меньше, чем длина пути. Электрическая стимуляция в этот период может вторгаться в контур re-entry и перезапускать или заканчивать тахикардию.
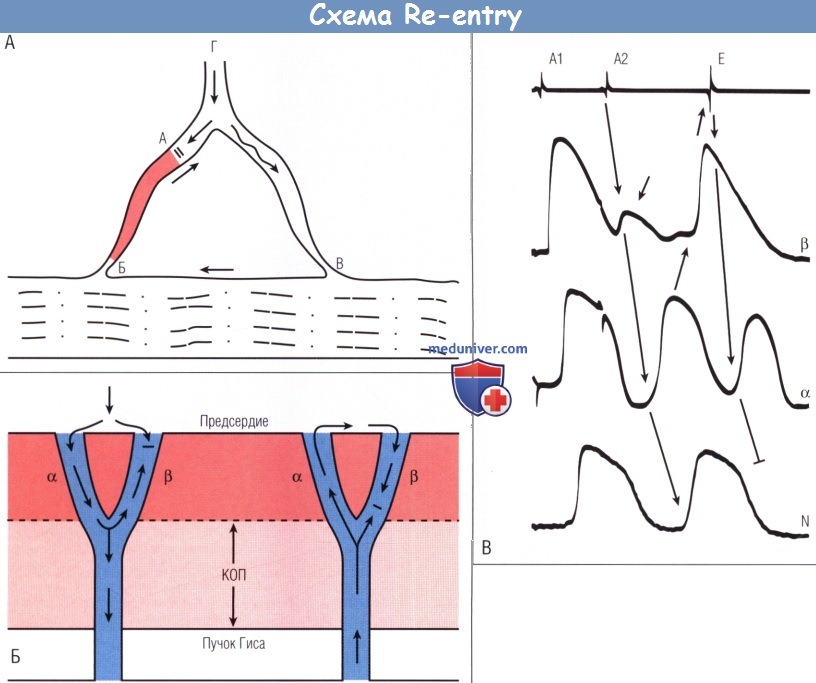
Волокна Пуркинье (Г) разделяются на два пути (Б и В), которые, в свою очередь, соединены с миокардом желудочка.
Предполагают, что импульс продвигается вниз по Г, блокируется в своем антероградном направлении в области А (стрелка, указывающая на двойную линию) и продолжает медленно продвигаться по В (волнистая стрелка),
возбуждая миокард желудочка. Затем импульс повторно входит в волокна Пуркинье на участке Б и ретроградно возбуждает А и Г.
Если импульс продолжает продвигаться по Г до миокарда желудочка и вызывает деполяризацию желудочка,
то образуется желудочковая экстрасистола re-entry. Продолжающееся re-entry такого типа вызовет желудочковую тахикардию.
(Б) Схематическое изображение внутриузловой диссоциации, отвечающей за предсердное эхо (слева).
Преждевременный предсердный ответ не пенетрирует в β-путь, где происходит однонаправленный блок, а распространяется антероградно по a-пути.
Когда конечный общий путь (КОП) занят, импульс может вернуться в предсердие по уже восстановленному β-пути и вызвать предсердное эхо.
На правой схеме — пример распространения во время генерации желудочкового эхо.
Преждевременный ответ в пучке Гиса переходит на КОП, наталкивается на рефрактерный β-путь (однонаправленный блок),
достигает предсердия по a-пути и возвращается по уже восстановленному β-пути, создавая желудочковый эхо-ответ. (В) Запись с предсердия (первая кривая) с клетками, отмеченными в β-области (вторая кривая),
α-область (третья кривая) и часть N АВ-узла (четвертая кривая) в изолированном препарате сердца кролика.
Основной ответ на А1 — активация как а-, так и β-пути и N-клеток (первый уровень ПД).
Преждевременный предсердный ответ на А2, вызванный только локальным ответом в β-клетках (короткая стрелка), с задержкой переходит на а-клетки, в дальнейшем с задержкой распространяется на N-клетки.
Вслед за ответом а-клетки происходит спонтанный ответ β-клетки и распространяется на предсердия (Е). Этот предсердный ответ представляет собой предсердное эхо.
Эхо возвращается для стимуляции а-клеток, но не распространяется на N-клетки. Важно отметить, что, хотя внутриузловое re-entry показано в АВ-узле кролика,
АВ-узловое re-entry у человека, возможно, проходит по внеузловым путям.
Частая стимуляция может запустить тахикардию, т.е. непрерывно перезапускать ее, внедряясь в контур и распространяясь по ткани таким же образом, как и импульс re-entry. Это ускоряет тахикардию до частоты стимуляции без купирования тахикардии.
В контуре re-entry с промежутком (интервалом) возбудимости скорость проведения определяет длительность цикла (время прохождения импульсом одного контура) и, таким образом, частоту тахикардии. Увеличение периода рефрактерности, если он не превышает значений, необходимых для окончания периода возбудимости, и не заставляет импульс распространяться по относительно рефрактерной ткани, не влияет на длительность цикла или частоту тахикардии.
Анатомическое re-entry может возникать при синдроме Wolff-Parkinson-White (WPW), АВ-узловой реципрокной тахикардии, при некоторых ПТ, ЖТ и ФЖ. Например, в исследованиях по картированию изолированных желудочков сердца свиньи была показана ключевая роль анизотропных анатомических структур (например, грубые изменения ориентации волокон) в поддержании контура re-entry во время ФЖ.
г) Функциональное re-entry. У функционального re-entry нет определенных анатомических границ, оно может возникать вследствие локальных различий трансмембранного потенциала в смежных волокнах, обладающих разными электрофизиологическими свойствами (например, переходом Пуркинье-КМЦ). Различия в возбудимости и/или рефрактерности, а также в анизотропном распределении межклеточного сопротивления обусловливают возникновение и поддержание re-entry.
Выявлено, что функциональная гетерогенность электрофизиологических свойств миокарда участвует в развитии и поддержании тахикардии и фибрилляции. Эти различия могут быть фиксированными, как в случае пространственного перераспределения нексусов ЩС при СН или на границе зоны ИМ либо в случае пространственных градиентов по абсолютному значению основного тока К+ (IK1).
Различия могут динамически меняться, как это бывает при острой ишемии миокарда или в присутствии веществ, удлиняющих реполяризацию. Важным определяющим условием динамически вызванного компонента гетерогенеза являются электрический возврат (восстановление), колебание (изменение) длительности потенциала действия (ДПД) и скорости проведения с диастолическим интервалом. Предполагают, что распад периодических волн ускоряется колебаниями ДПД (так называемые чередования ДПД) достаточно большой амплитуды, чтобы вызвать блок проведения вдоль спирального волнового фронта.
- Читать "Трепетание и фибрилляция предсердий по механизму re-entry"
Оглавление темы "Механизмы развития аритмий":- Механизмы развития аритмии - аритмогенез
- Нарушение образования импульса в синусовом узле сердца
- Нарушение автоматизма сердца
- Механизм триггерной активности сердца
- Механизм возникновения парасистолии сердца
- Нарушение проведения импульса в сердце
- Причины и механизмы развития re-entry
- Трепетание и фибрилляция предсердий по механизму re-entry
- Механизмы атриовентрикулярного узлового re-entry (АВУРТ)
- Механизмы синдрома преждевременного возбуждения (WPW-синдрома)
