Показания для имплантации кардиовертера-дефибриллятора (ИКД)
Рекомендации ACC/AHA/HRS по использованию ИВР и ИКД приведены в таблице ниже.
а) Клинические исследования по применению имплантируемых кардиовертеров-дефибрилляторов (ИКД). Исследования по вторичной профилактике. Возможности профилактики ВСС с помощью ИКД-терапии впервые были продемонстрированы в многочисленных исследованиях по вторичной профилактике (т.е. у пациентов, которые уже перенесли за пределами лечебного учреждения внезапную остановку кровообращения или спонтанную устойчивую ЖТ либо ФЖ).
Снижение летальности при использовании ИКД-терапии с целью вторичной профилактики было продемонстрировано в исследованиях: AVID (Antiarrhythmics Versus Implantable Defibrillators), CIDS (Canadian Implantable Defibrillator Study) и CASH (Cardiac Arrest Study Hamburg). Исключением является исследование CIDS, в котором не было получено достоверных различий в ОС при ИКД-терапии (однако корректность проведения данного исследования подвергается критике).
Анализ подгрупп в исследованиях по вторичной профилактике продемонстрировал значительные преимущества ИКД-терапии у пациентов с ФВ 20-34%.

б) Исследования по первичной профилактике внезапной сердечной смерти. Исследования по первичной профилактике ВСС с помощью ИКД-терапии у пациентов без гемодинамически значимой желудочковой тахиаритмии, но имеющих повышенный риск таких нарушений ритма, включают: MADIT I (Multicenter Automatic Defibrillator Implantation Trial), CABG (Coronary Artery Bypass Graft), PATCH trial, MUSTT (Multicenter Unsus tained Tachycardia Trial), MADIT II, DEFINITE (Defibrillators in Non-Ischemic Cardiomyopathy Treatment Evaluation), SCD-HeFT (Sudden Cardiac Death in Heart Failure Trial), DINAMIT (Defibrillator in Acute Myocardial Infarction Trial).
В исследовании MADIT I участвовали пациенты, перенесшие ИМ с ФВ ЛЖ < 35%, имеющие неустойчивую ЖТ и индуцибельную устойчивую ЖТ при проведении электрофизиологического исследования. Пациенты были рандомизированы в группы ИКД-терапии и приема амиодарона. Через 27 мес в группе ИКД-те-рапии было зарегистрировано снижение относительного риска на 54%.
В исследование MADIT II вошли пациенты, перенесшие ИМ не менее чем за 1 мес до исследования и с выраженной дисфункцией ЛЖ (ФВ ЛЖ < 30%). Желудочковая тахиаритмия не была критерием включения. У 70% пациентов была СИ I/II ФК NYHA.
В группе ИКД-терапии было зарегистрировано снижение относительного риска на 31% по сравнению с группой традиционной лекарственной терапии.
Исследования CABG и PATCH следует рассматривать отдельно, т.к. пациенты, которым выполняли АКШ, были рандомизированы либо в группу имплантации ИКД во время операции, либо в группу с назначением послеоперационной антиаритмической терапии. Исследование было прекращено преждевременно, т.к. промежуточный анализ не показал разницы в выживаемости между двумя группами. Летальные исходы в обеих группах были обусловлены периоперационными причинами и, следовательно, не могли быть предотвращены с помощью антиаритмической терапии. Анализ подгрупп показал преимущества ИКД-терапии у пациентов с риском жизнеугрожающих желудочковых тахиаритмий.
Исследование DINAMIT включало пациентов со сниженной функцией ЛЖ (ФВ ЛЖ < 35%) и вегетативной нейропатией через 6-40 сут после ИМ. Первичной конечной точкой была ОС. Выявлено, что ИКД-терапия в группе пациентов высокого риска, перенесших недавно ИМ, не снижает ОС. Однако ИКД-терапия ассоциировалась с уменьшением частоты летальных исходов, связанных с аритмиями, что компенсировалось увеличением частоты летальных исходов вследствие неаритмических причин. Результаты исследований ИКД-терапии для первичной профилактики приведены в таблице ниже.
б) Наиболее существенные исследования сердечной ресинхронизирующей терапии (СРТ) имплантируемым кардиовертер-дефбриллятором (ИКД). Исследования сердечной ресинхронизирующей терапии (СРТ) расширили показания к ИКД-терапии и предоставили дополнительную информацию о популяции с СН. Исследование COMPANION (Comparison of Medical Therapy, Pacing and Defibrillation in Heart Failure), спланированное как исследование летальности, было первым, в котором оценивали эффекты СРТ на показатели смертности и число госпитализаций. В этом параллельном открытом исследовании пациентов рандомизировали в группы с оп тимальной медикаментозной терапией (ОМТ), ОМТ + СРТ и ОМТ + ИКД-СРТ. Все пациенты имели стандартные показания для СРТ.
Исследование продемонстрировало, что риск общей смертности (ОС) или госпитализации по любым причинам может быть существенно снижен с помощью СРТ или ИКД-СРТ. Выживаемость была выше в группе ИКД-СРТ, чем в группе СРТ. При сравнении группы ИКД-СРТ с группой ОМТ было получено 40% снижение риска смерти или госпитализации при СИ и 36% снижение риска ОС. В группе СРТ также было отмечено уменьшение ОС, но оно не было статистически значимым.
В исследовании CARE-HF (Cardiac Resynchronization in Heart Failure) пациентов со стандартными показаниями к СРТ (диссинхрония подтверждалась, если QRS составлял 120-149 мсек) рандомизировали в группы СРТ или ОМТ. У пациентов с СРТ относительный риск первичной конечной точки (комбинация «ОС и госпитализация вследствие сердечно-сосудистых событий») был снижен на 37%, а на 36% снизилась ОС но сравнению с пациентами, получавшими только медикаментозную терапию.
Наследственные аритмогенные заболевания, при которых часто рекомендуют ИКД-терапию: синдром удлиненного интервала QT, синдром Brugada, аритмогенная дисплазия ПЖ, ГКМП и другие.
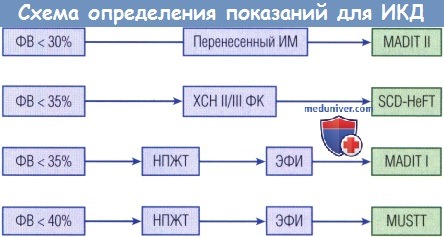
основанная на клинических рандомизированных исследованиях MADIT I и II, MUSTT, SCD-HeFT.
Сразу после принятия решения о том, что пациент соответствует критериям и ему следует имплантировать ИКД, необходимо выбрать между одно- и двухкамерным ИКД.
Если у пациента есть показания к постоянной ЭКС (явные нарушения проведения и синусовый ритм), следует выбрать двухкамерный ИКД.
Если пациенту предположительно не требуется постоянная ЭКС, за исключением «постшоковой», или если у пациента присутствует постоянная форма фибрилляции предсердий,
при которой необходима ЭКС, следует выбрать однокамерный ИКД.
Если у пациентов, которым показана ЭКС, нет нарушений атриовентрикулярной проводимости, следует запрограммировать устройство так,
чтобы минимизировать или исключить желудочковую стимуляцию, которая возможна из-за потенциальных негативных эффектов длительной стимуляции из верхушки правого желудочка.
MADIT I и II — Multicenter Automatic Defibrillator Implantation Trial I и II; MUSTT — Multicenter Sustained Tachycardia Trial;
SCD-HeFT — Sudden Cardiac Death in Heart Failure Trial; ИМ — инфаркт миокарда НПЖТ — неподавляемая желудочковая тахикардия;
ФВ — фракция выброса ФК — функциональный класс; ХСН — хроническая сердечная недостаточность ЭФИ — электрофизиологическое исследование.
в) Технические аспекты имплантации кардиовертера-дефибриллятора. Основные компоненты ИКД — электронная схема, источник питания и модуль памяти с микропроцессором, который управляет различными частями системы. Высоковольтные конденсаторы источника питания обеспечивают напряжение электрического тока в диапазоне от < 1 В для стимуляции до 750 В для дефибрилляции (в отличие от усилителя напряжения, используемого в ИВР, который увеличивает напряжение на выходе, сохраняя электрическую мощность до тех пор, пока не будет аккумулировано оптимальное количество энергии, и затем высвобождает ее).
ИКД имеет отличающиеся от большинства ИВР схемы детекции. Это необходимо для надежной детекции низкоамплитудных сигналов ФЖ и предотвращения детекции экстракардиальных помех и кардиальных импульсов иных, чем при ЖТ и ФЖ. Схема детекции также позволяет автоматически настраивать чувствительность.
Большинство ИКД систем имплантируют трансвенозно. Они имеют антитахикардическую стимуляцию (АТС) и функцию стимуляции при брадикардии (широко распространены одно- и двухкамерные ИКД с функцией программирования стимуляции и адаптации по частоте). Устройства ИКД-СРТ — это СРТ с возможностями ИКД.
Срок службы ИКД зависит от частоты электрических разрядов, степени зависимости от ИВР и других программируемых параметров (в большинстве случаев — 5-9 лет). ИКД постоянно мониторирует сердечный ритм пациента и реагирует, когда частота превышает программируемый предел. Например, если ИКД запрограммирован для лечения желудочковой тахиаритмии при пороге детекции 175 уд/мин, то ИКД, определив частоту > 175 уд/мин, проводит АТС или электрический разряд в зависимости от запрограммированных параметров терапии.

Необходимо различать чувствительность (или корректную интерпретацию кардиального события, которое повлекло за собой клинически оправданное действие устройства) и детекцию аритмии. Детекция касается возможности устройства распознавать определенные типы аритмий и оптимально реагировать на них, т.е. с помощью детекции осуществляется и контроль терапии.
Преимущество антитахикардической стимуляции (АТС) — купирование нарушений ритма без электрического разряда ИКД. АТС обладает возможностями более гибкого программирования различных параметров и терапии тахикардии, т.е. запрограммировать можно параметры лечения индивидуально для каждого пациента. Различные зоны (или модули) терапии могут быть запрограммированы для детекции желудочковой тахиаритмии и позволяют прервать медленные аритмии до электрического разряда, что делает возможным более «агрессивно» лечить быст рые тахикардии. Программирование для гипотетического пациента описано в таблице ниже. У этого пациента медленная ЖТ в диапазоне 126-190 уд/мин купируется АТС в зоне 1.
Если первая антитахикардическая стимуляция (АТС) безуспешна, автоматически используется вторая АТС. Если и она безуспешна, то перед выполнением высокоэнергетического электрического разряда будет проведен низкоэнергетический разряд. Электрические разряды синхронизированы с ЖТ (кардиоверсия) или несинхронизированы (дефибрилляция). Вторую зону терапии программируют для быстрых ЖТ (быстрая ЖТ или ФЖ купируется с помощью высокоэнергетического разряда).
Следует отметить, что, хотя цель антитахикардической стимуляции (АТС) заключается в прерывании ЖТ, возможна акселерация ЖТ и дегенерация в быструю гемодинамически неустойчивую ЖТ или ФЖ, требующую дефибрилляции.
Зоны и диапазоны детекции, особенности различных видов терапии и стимуляции при брадикардии являются программируемыми параметрами, а возможности программирования в различных устройствах существенно варьируют.
- Читать "Выбор кардиовертера-дефибриллятора и его имплантация"
Оглавление темы "Имплантация кардиовертера-дефибриллятора (ИКД)":- Причины и устранение ЭКГ нарушений электрокардиостимуляции (ЭКС)
- Показания для имплантации кардиовертера-дефибриллятора (ИКД)
- Выбор кардиовертера-дефибриллятора и его имплантация
- Осложнения имплантации кардиовертера-дефибриллятора
- Влияние электромагнитного излучения на кардиовертер-дефибриллятор (ИКД)
- Влияние лекарств на кардиовертер-дефибриллятор (ИКД)
- Наблюдение за пациентом после имплантации кардиовертера-дефибриллятора (ИКД)
- Современные показания для постоянной ЭКС (электрокардиостимуляции)
- Рекомендации по выбору электрокардиостимулятора (ЭКС)
- Рекомендации по лечению имплантируемым кардиовертером-дефибриллятором (ИКД)
