Взаимосвязь между сахарным диабетом и артериальной гипертензией
Сегодня консультация эндокринолога доступна для любого гражданина. Эндокринологи имеются в поликлиниках, стационарах, если их нет, то их функцию выполняют терапевты. Доступны эндокринологи в платных клиниках. Стоимость консультации составляет от 800 до 2500 рублей в зависимости от региона, квалификации врача. К примеру, тут первичная консультация эндокринолога, в частной клинике Москвы, обойдется в 2000 рублей. Для региона со средней заработной платой значительно выше чем по стране - это не является существенной суммой. Тем не менее, по всей стране продолжают встречаться случаи лечения артериальной гипертензии у пациентов с сахарным диабетом различными специалистами, что наталкивает на мысль о том, что врачи не совсем понимают взаимосвязь между данными патологиями. В данной статье предлагаю разобрать взаимосвязь сахарного диабета и артериальной гипертензии.
Гормоны в нормальных условиях во многом определяют тонус сосудов. Сложное взаимодействие между различными эндокринными компартментами управляет широким спектром медиаторов, участвующих в контроле артериального давления (АД). Эндокринные заболевания могут приводить к патологическому повышению артериального давления, также известному как вторичная гипертензия.
Их выявление и коррекция могут улучшить контроль АД или даже вылечить заболевание, в конечном итоге снизив сердечно-сосудистый риск. Кроме того, в ходе экспериментальных исследований эндокринных нарушений получены интересные сведения о патофизиологии первичной гипертензии. В связи с этим и сахарный диабет, и гормоны, контролирующие фосфорно-кальциевый обмен, не только считаются основными причинами эндокринной гипертензии, но и играют ключевую роль в развитии первичной гипертензии. Патофизиологические механизмы, лежащие в основе первичной гипертензии, в случае развития вторичной гипертензии становятся неуправляемыми из-за лежащих в ее основе нарушений уровня гормонов щитовидной железы, минералокортикоидов и ГКС, гормона роста инсулиноподобного фактора роста и половых гормонов.
Следовательно, изучение патофизиологических механизмов вторичной гипертензии может помочь в понимании способов контроля АД, и ее следует рассматривать как источник для выявления потенциальных биомаркеров и даже как терапевтическую мишень. Здесь суммируются современные знания, связывающие эндокринную систему и развитие гипертонии. Будут проанализированы прямые эффекты инсулина, гормонов щитовидной железы, минералокортикоидов и ГКС, гормона роста/инсулиноподобного фактора роста, половых гормонов и гормонов, регулирующих фосфорно-кальциевый обмен, с учетом их сложного взаимодействия. Будут рассмотрены как клинические данные, так и интервенционные клинические исследования, а также описаны возможные клинические последствия.
Термин «вторичная гипертензия» включает все случаи артериальной гипертензии с установленной причиной. Среди них около 3% случаев вторичных форм гипертензии приходится на эндокринные нарушения. Хотя эти формы гипертонии довольно редки, выявление эндокринной причины может привести к улучшению контроля АД или даже к излечению, что в конечном итоге снизит риск ССЗ. Несмотря на то, что эндокринные нарушения у пациентов с гипертонией встречаются нередко, современные рекомендации не поддерживают скрининговые стратегии выявления вторичных причин гипертонии. Следовательно, подозрение на потенциальную эндокринную причину артериальной гипертензии должно быть основано на данных клинической картины.
В развитии вторичной гипертензии играют роль многие эндокринные системы. Наиболее частыми причинами являются повышение уровня минералокортикоидов (МК), катехоламинов, гормонов щитовидной железы и ГКС. Другие причины эндокринной гипертензии включают нарушение уровня гормона роста/ИФР-1 и половых гормонов. Хотя и сахарный диабет, и изменение фосфорно-кальциевого (Са2+) обмена не считаются основной причиной эндокринной гипертензии, они могут способствовать ее развитию. В этой главе мы стремились обновить имеющиеся знания об эндокринной гипертензии, сосредоточив внимание на клинических данных крупных клинических исследований и новых взглядах на лежащие в ее основе патофизиологические механизмы.
а) Взаимосвязь между сахарным диабетом и артериальной гипертензией. Сахарный диабет представляет собой серьезную проблему для общественного здравоохранения. По данным Международной федерации диабета, в 2015 г. численность больных составляла 415 млн человек, а к 2040 г. прогнозируется увеличение этой цифры до 642 млн (Zimmet и соавт., 2016). Почти 70% пациентов с сахарным диабетом в возрасте >40 лет также страдают артериальной гипертензией, особенно среди представителей негроидной расы и латиноамериканцев. Большинство пациентов с гипертонией и нарушением уровня глюкозы страдают СД 2 или нарушением толерантности к глюкозе. При СД 2-го типа гипертензия обычно является частью метаболического синдрома, включающего ИР, центральное ожирение и дислипидемию, тогда как при СД 1-го типа повышение артериального давления может развиться через несколько лет после постановки диагноза и манифестировать с диабетической нефропатии.
Все эти патофизиологические факторы могут усугублять друг друга.
Первое упоминание эпидемиологической и патофизиологической связи между сахарным диабетом и гипертонией относится к 1930-м гг., когда впервые было сообщено о повышенной вероятности развития гипертонии у пациентов, страдающих сахарным диабетом. Распространенность гипертонии среди пациентов с диабетом в значительной степени зависит от порогового значения артериального давления и исследуемой популяции. В Британском проспективном исследовании сахарного диабета 39% пациентов имели артериальную гипертензию по критерию АД >160/90 мм рт.ст. или получали антигипертензивную терапию. В последующих отчетах крупных исследований предполагаемая распространенность была выше, увеличившись с 51% в 1988— 1994 гг. до 66% в 2005—2008 гг.
В долгосрочном наблюдательном исследовании, проведенном в Финляндии в 1968 г., мужчины с нормальным артериальным давлением и отсутствием диабета были разделены на тертили по уровню концентрации глюкозы в крови (в соответствии со значениями глюкозы через 1 ч после нагрузки глюкозой), при этом было обнаружено, что 18 лет спустя большее количество людей в двух верхних тертилях страдали гипертонией [отношение шансов (ОШ) 1,36 и 1,71 соответственно], даже с учетом поправки на возраст, потребление алкоголя, ожирение и изначальный уровень систолического и диастолического АД. Аналогичные результаты были получены в исследовании сердца в Сан-Антонио, в котором в течение 7 лет наблюдались 1039 пациентов без диабета и гипертонии; почти у 10% из них развилась гипертензия, что было продиктовано возрастом, соотношением окружности талии и бедер, ИМТ, уровнем триглицеридов и инсулина натощак. Последнее предопределило развитие гипертонии как у худых, так и у тучных испытуемых.
В целом эти результаты показывают, что люди с предрасположенностью к развитию сахарного диабета имеют повышенный уровень АД. При этом артериальная гипертензия у них наблюдалась задолго до того, как они пересекли диагностический порог диабета. Также была продемонстрирована обратная связь, согласно которой наличие гипертонии предопределяло развитие СД 2-го типа. В последующем исследовании с участием 10 000 израильских мужчин было доказано, что систолическое АД является значимым предиктором развития СД 2-го типа независимо от возраста, наличия заболевания периферических артерий и ожирения. В исследовании риска развития атеросклероза было обнаружено, что вероятность развития СД 2-го типа у пациентов с гипертонией почти в 2,5 раза выше, чем у пациентов с нормальным давлением.
В любом случае важно учитывать, что риск развития диабета у пациентов с гипертонией может увеличиваться при приеме лекарств, таких как бета-блокаторы и тиазидные/тиазидоподобные диуретики, тогда как данные в отношении ингибиторов ангиотензин-превращающего фермента (АПФ) до сих пор остаются спорными. В исследовании почечной недостаточности и сердечно-сосудистых событий (RIACE) мужской пол, семейный анамнез, возраст и И МТ были признаны независимыми факторами риска развития артериальной гипертензии, при этом риск увеличивается в зависимости от длительности заболевания, а нормальная функция почек действует как фактор защиты.
Гипертония и диабет оказывают значительный эффект на сердечнососудистый (СС) риск с точки зрения смертности и заболеваемости, вызывая как микрососудистые (ретинопатия, нефропатия и нейропатия), так и макрососудистые (заболевания периферических артерий, ишемическая болезнь сердца и инсульт) осложнения. Более того, гипертония и диабет вместе приводят к увеличению относительной смертности от ССЗ в 2,5—7,2 раза. Согласно анализу обеих фремингемских когорт, индивидуальный сердечно-сосудистый риск для пациентов с диабетом снизился за последние 40 лет, при том, что общее количество сердечно-сосудистых заболеваний, связанных с диабетом, увеличилось.
Таким образом, пациенты с гипертонией на момент постановки диагноза сахарного диабета имели более высокие показатели смертности от всех причин и частоту сердечно-сосудистых событий. Позднее эти результаты были подтверждены у пациентов с сахарным диабетом, поскольку артериальная гипертензия была ассоциирована с увеличением на 72% риска смертности от всех причин и на 57% увеличивала риск развития любого сердечно-сосудистого события. Следовательно, артериальная гипертензия играет ключевую роль в повышении риска развития сердечно-сосудистых заболеваний у пациентов с диабетом, в основном среди мужчин, даже после поправки на другие факторы риска сердечно-сосудистых заболеваний (Ferrannini and Cushman, 2012).
б) Патофизиологические взаимодействия между сахарным диабетом и артериальной гипертензией. Повышение периферического сосудистого сопротивления и эндотелиальная дисфункция являются основными точками соприкосновения между артериальной гипертензией и СД 2-го типа (рис. ниже). Ожирение — главный фактор риска, влияющий на АД и СД 2-го типа (Balakumar и соавт., 2016). У лиц с ожирением наблюдается более высокий уровень норадреналина в плазме, чем у худых, а также более быстрый обмен норадреналина в периферических тканях и более продолжительная симпатическая активность мышц. Доказано, что симпатическая активность более выражена в висцеральной, чем в периферической жировой ткани. Было высказано предположение, что нейроадренергические влияния играют роль в патофизиологическом процессе метаболического синдрома и связанном с ним риске сердечно-сосудистых заболеваний.
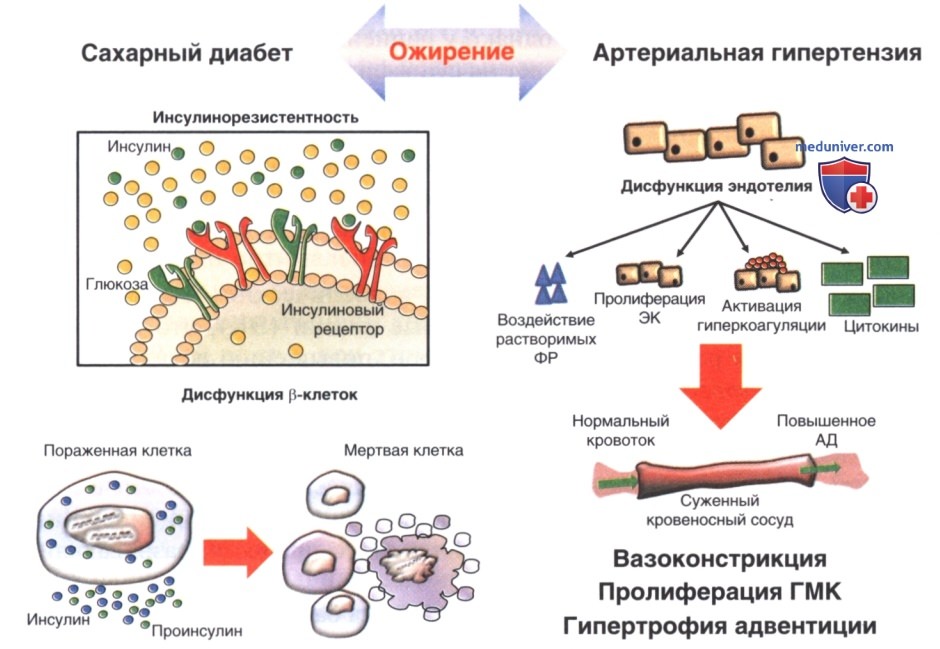
Симпатические реакции проявляются в снижении чувствительности к инсулину за счет гемодинамических и клеточных эффектов и могут как прямо, так и косвенно способствовать прогрессированию поражения органов. При метаболическом синдроме длительные симпатические влияния могут повышать АД посредством различных механизмов. ИР при этом играет важную роль, так как при этом состоянии активация симпатической системы сочетается с частичной нечувствительностью к лептину, высоким уровнем свободных жирных кислот и низкими уровнями грелина и адипонектина. У пациентов с артериальной гипертензией отмечается ИР скелетных мышц, при этом точные механизмы, приводящие к возникновению гипертонии, еще полностью не изучены.
В физиологических условиях инсулин может вызывать небольшое увеличение кровотока за счет высвобождения NO и усиления опосредованной ацетилхолином вазодилатации, однако у пациентов с инсулинорезистентно-стью отмечается более слабый ответ на супрафизиологические концентрации инсулина. ИР и нарушение вазодилатации часто встречаются как при СД 2-го типа, так и при гипертонии, однако коррекция эндотелиальной дисфункции или вазодилатации не улучшает инсулино-опосредованное поглощение глюкозы у пациентов с гипертонией. ИР и нарушение транспорта глюкозы компенсаторно стимулируют выработку инсулина поджелудочной железой, что приводит к развитию гиперинсулинемии.
Затем инсулин вызывает чрезмерный анаболический ответ в чувствительных тканях, таких как эндотелиальные клетки (ЭК), что в конечном итоге приводит к ремоделированию сосудов, повышению ригидности артерий и потере ауторегуляции АД. Гиперинсулинемия также может оказывать хронический антинатрийуретический эффект, стимулируя задержку натрия (Na+) и воды почками, что дополнительно повышает АД. Этот эффект также может быть связан с повышением симпатической активности в почках и активацией РААС, что часто наблюдается при ожирении и гипертензии. Гломерулосклероз — отдаленный результат этого процесса, развивающийся из-за стойкой гиперфильтрации.
Другой механизм связан с нарушением ответа барорецепторов, активность которых может быть нарушена при ожирении. РААС имеет важное значение в развитии эндотелиальной дисфункции, особенно за счет стимуляции высвобождения ангиотензина II и норадреналина помимо подавления симпатоингибирующего эффекта NO. Активность РААС аномально повышена у пациентов с ожирением, что в конечном итоге приводит к усилению реабсорбции Na+, увеличению периферического артериального сопротивления и хронической активации симпатической системы. Было высказано предположение, что роль альдостерона в развитии гипертонии у пациентов с ожирением может быть связана с выработкой мощных факторов, стимулирующих высвобождение минералокортикоидов в жировой ткани, или способностью окисленной линолевой кислоты стимулировать синтез альдостерона.
в) Влияние сахароснижающих препаратов на артериальную гипертензию. В последние годы появилось много свидетельств того, что снижение АД у пациентов с гипертонией и сахарным диабетом значительно улучшает сердечно-сосудистые исходы (табл. 1) (1998; Curb и соавт., 1996; Estacio и соавт., 1998; Xiang и соавт., 2010; Hansson и соавт., 1998; Patel и соавт., 2007; Schrier и соавт., 2002; Tuomilehto и соавт., 1999). Несмотря на это, оптимальный порог снижения АД у пациентов с сахарным диабетом долгое время оставался предметом споров (1998; Curb и соавт., 1996; Estacio и соавт., 1998; Xiang и соавт., 2010; Hansson и соавт., 1998; Patel и соавт., 2007; Schrier и соавт., 2002; Tuomilehto и соавт., 1999).
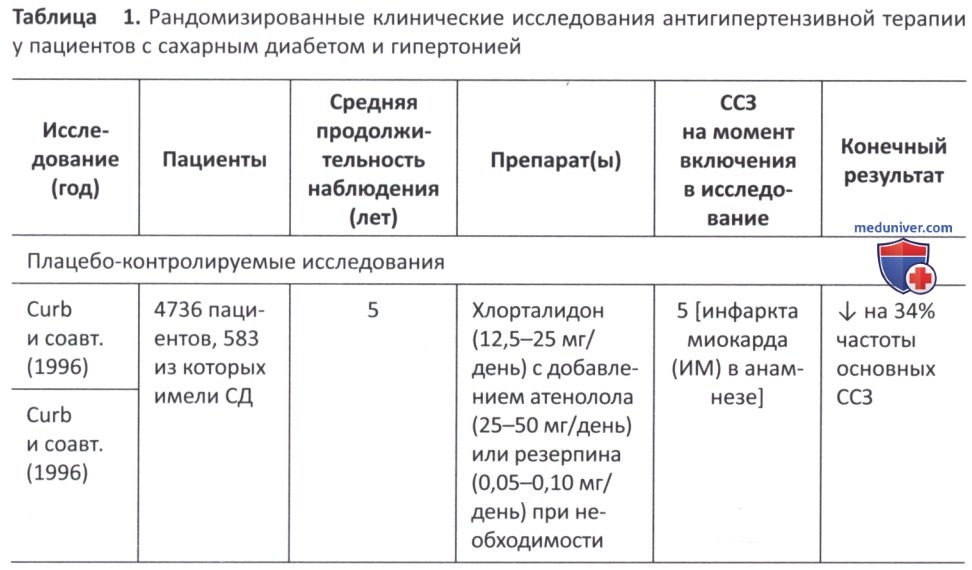
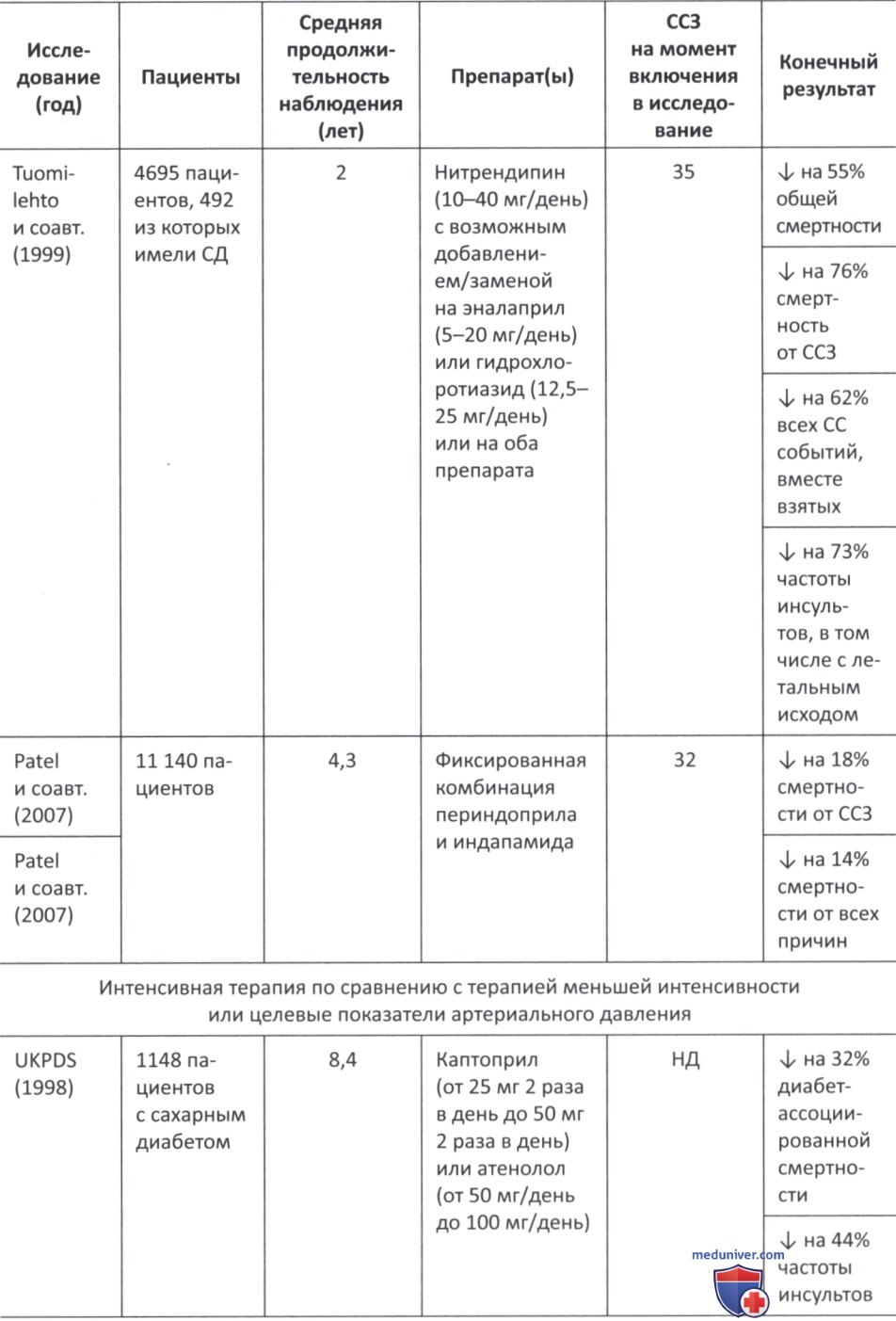
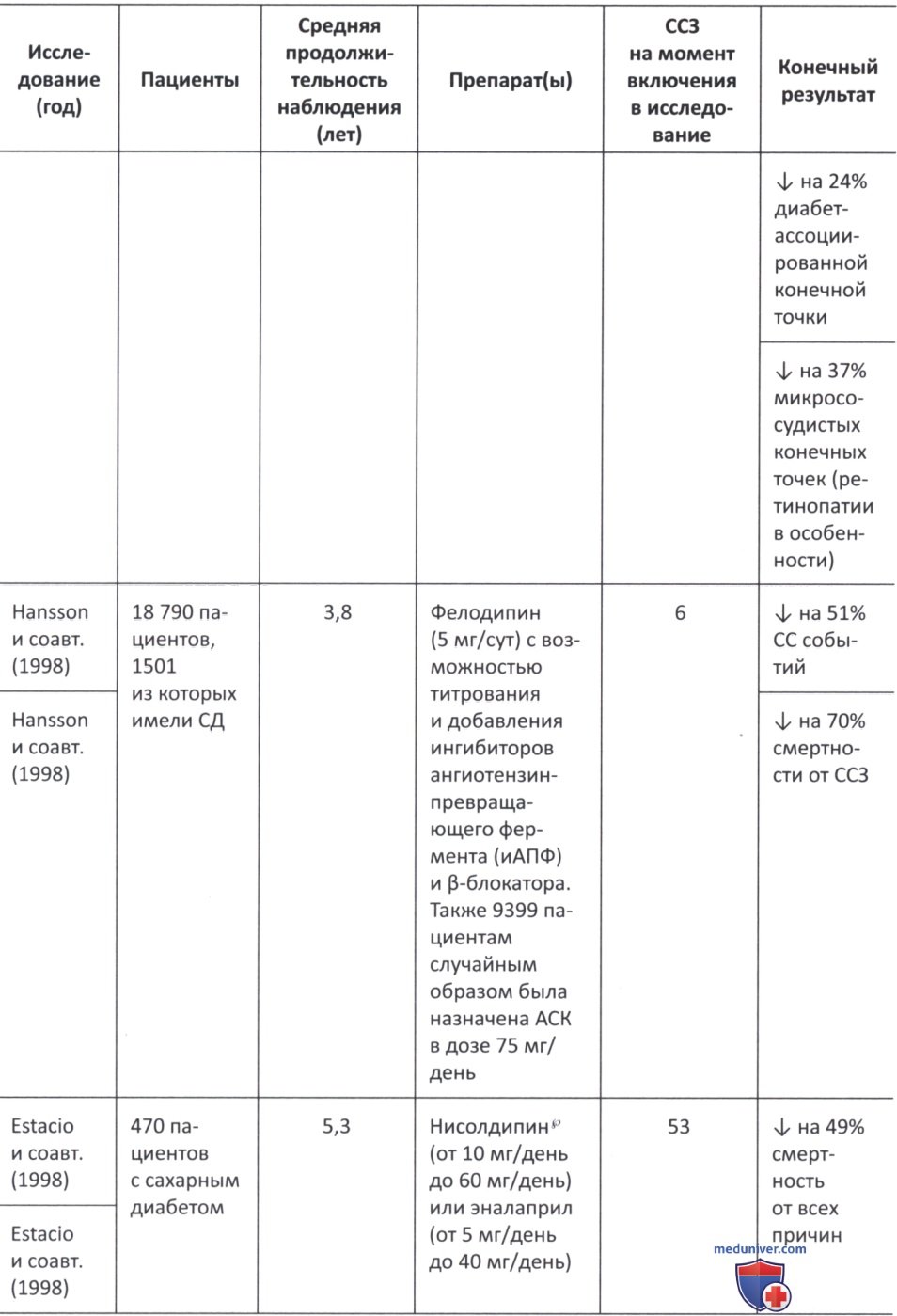
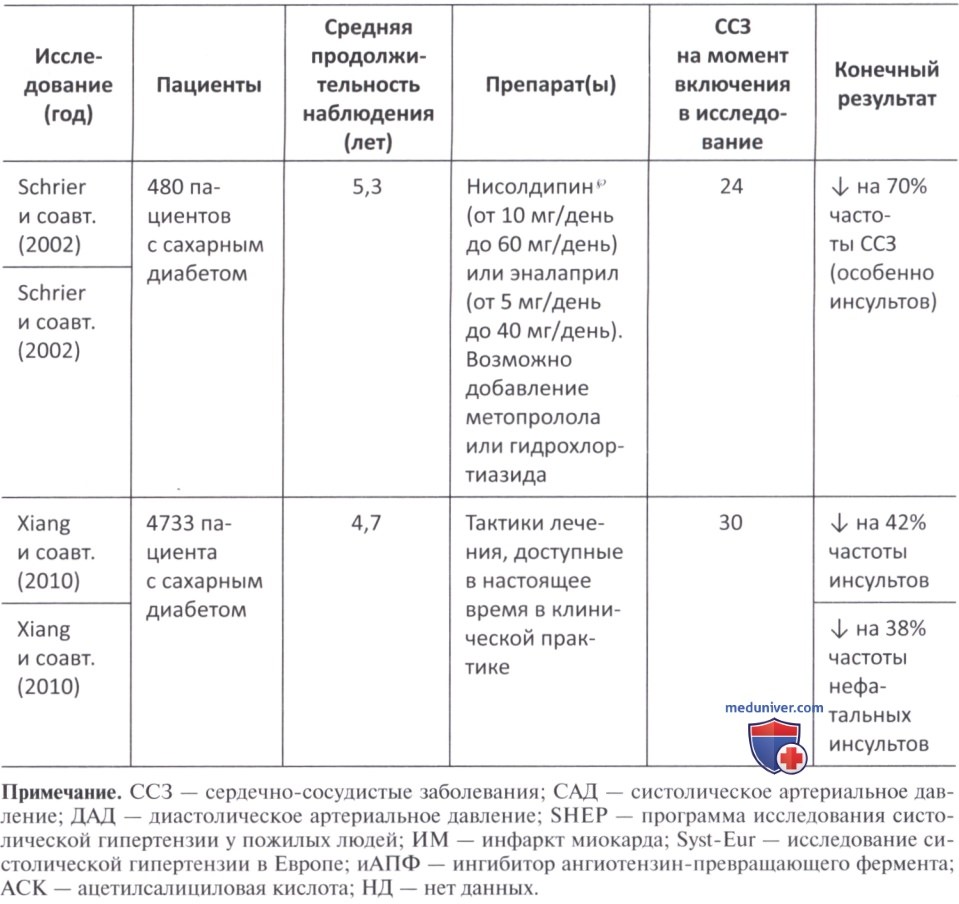
По данным исследования UKPDS 36, уровень систолического АД >120 мм рт.ст. приводит к постоянно повышенному СС риску (Adler и соавт., 2000). В исследовании UK.PDS 38 более 1000 пациентов с артериальной гипертензией и СД 2-го типа были случайным образом распределены на две группы по целевым значениям АД (<150/85 мм рт.ст. или <180/105 мм рт.ст.) с последующим наблюдением в течение 8,4 лет.
Было показано, что жесткий контроль АД у этих пациентов привел к клинически значимому снижению риска смерти и развития осложнений диабета, а также прогрессирования диабетической ретинопатии и ухудшения остроты зрения (1998).
В исследовании оптимального лечения гипертонии (НОТ) 18 790 пациентов с артериальной гипертензией были случайным образом распределены по трем целевым значениям диастолического АД (<90 мм рт.ст., <85 мм рт.ст. или <80 мм рт.ст.), при этом снижение частоты возникновения сердечно-сосудистых событий на 51% было обнаружено при показателях в диапазоне между 80 и 90 мм рт.ст., особенно среди пациентов с СД 2-го типа (Hansson и соавт., 1998). Несмотря на то, что это наблюдение было получено в результате субанализа основных результатов исследования, большое количество добровольцев и значимые показатели влияния на риск сердечно-сосудистых событий легли в основу рекомендуемого порогового уровня АД у пациентов с сахарным диабетом <130/80 мм рт.ст.
В любом случае проблема заключается в том, что клинические данные, демонстрирующие снижение показателей систолического АД, были получены в исследованиях, в которых пациенты рандомизировались по нижней границе целевых значений диастолического АД. Более того, жесткий контроль повлек за собой увеличение количества назначаемых антигипертензивных препаратов и частоты посещений врача; поэтому вероятнее всего было бы ожидать неудачи в достижении вышеупомянутых целей, в основном из-за недостаточной приверженности к лечению.
Однако в других исследованиях предпринималась попытка подтвердить данные, полученные в исследованиях UK.PDS 38 и НОТ. В исследовании «Действие при сахарном диабете и сосудистых заболеваниях: контролируемая оценка применения претеракса и диамикрона с модифицированным высвобождением» (ADVANCE) в течение 4,3 лет наблюдались более 100 000 пациентов с СД 2-го типа, которые были рандомизированы в группу, получающую лечение фиксированной комбинацией индапамид + периндоприл, или в группу плацебо. Среднее значение АД составляло 135/75 мм рт.ст. в группе индапамид + периндоприл и 140/77 мм рт.ст. в группе плацебо. В группе индапамид + периндоприл отмечалось снижение основных макрососудистых или микрососудистых событий на 9%, случаев смерти от сердечно-сосудистых заболеваний на 18% и случаев смерти от всех причин на 14% (Patel и соавт., 2007).
Напротив, в анализе подгрупп из 6400 пациентов с сахарным диабетом, гипертонией и ишемической болезнью сердца из Международного исследования верапамила, трандолаприла (INVEST) не было обнаружено никаких других преимуществ среди пациентов с уровнем систолического АД <130 мм рт.ст. (Patel и соавт., 2007). Кроме того, было отмечено увеличение риска сердечно-сосудистых событий у пациентов с систолическим АД >140 мм рт.ст., еще более высокий риск был выявлен у пациентов с систолическим АД <115 мм рт.ст. (Patel и соавт., 2007). Принимая во внимание все эти данные, с конца 1990-х до начала 2000-х гг. в рекомендациях по ведению сахарного диабета и гипертонии указывалось целевое значение АД <130/85 мм рт.ст. для пациентов без диабета и <130/80 мм рт.ст. для пациентов с диабетом. Целевые показатели для пациентов с сахарным диабетом были пересмотрены после публикации результатов исследования «Действия по контролю сердечно-сосудистого риска при диабете и артериальном давлении» (ACCORD-BP).
В этом исследовании, включавшем более 4000 пациентов, впервые было изучено целевое значение систолического АД (<120 мм рт.ст. или <140 мм рт.ст.) и было показано снижение значений АД в группе интенсивной терапии за период наблюдения 4,7 года. Более того, не было продемонстрировано никаких различий в отношении первичной конечной точки (нефатальный инфаркт миокарда, нефатальный инсульт и смерть от всех сердечно-сосудистых причин), смертности от сердечно-сосудистых заболеваний и смертности от всех причин, но отмечалось снижение частоты инсультов, в том числе без смертельного исхода. Несмотря на эти преимущества, в группе интенсивного лечения было выявлено большое количество побочных эффектов, таких как гипотония, гиперкалиемия, обморок, аритмия, ангионевротический отек и почечная недостаточность.
В свете этого исследования авторы пришли к выводу, что наибольшая польза может быть получена при достижении целевого систолического АД <140 мм рт.ст.
Именно поэтому данная рекомендация была оперативно внесена во все международные руководства. Кроме данных исследования ACCORD-BP, следует принимать во внимание некоторые противоречия. Во-первых, порог увеличения риска для пациентов составлял 120 мм рт.ст., а не 130 мм рт.ст. Во-вторых, рекомендованный порог АД (140 мм рт.ст.) был достаточно далек от значений, достигнутых в исследовании (119,3 мм рт.ст. в группе интенсивной терапии и 133,5 мм рт.ст. в стандартной группе). В-третьих, не было найдено оптимальное значение систолического АД, так как в исследовании ACCORD-BP не было сделано выводов относительно снижения риска развития сердечно-сосудистых заболеваний при значении АД в диапазоне между 125 и 135 мм рт.ст. Еще одним доказательством служат результаты апостериорного анализа исследования ACCORD-BP, позволившие сделать иные выводы. В частности, риск первичного исхода (основных сердечно-сосудистых событий) был ниже в группах интенсивного сахароснижающего, антигипертензивного лечения или того и другого по сравнению со стандартным комбинированным лечением гипертонии и гликемии, в то время как для вторичных исходов в обеих группах интенсивной терапии была продемонстрирована более низкая частота инсульта и инфаркта миокарда; большинство других соотношений рисков были сопоставимы или указывали в пользу групп интенсивного лечения.
После публикации результатов исследования ACCORD-BP было проведено несколько метаанализов для определения оптимальных целевых показателей АД у пациентов с диабетом. Bangalore и соавт. проанализировали 13 исследований с участием 37 736 человек, страдающих сахарным диабетом, нарушением гликемии натощак и/или имеющих нарушение толерантности к глюкозе, за которыми наблюдали в течение I года. У пациентов, у которых происходило интенсивное снижение АД, наблюдалось снижение смертности от всех причин на 10%, снижение частоты возникновения инсульта на 17% и увеличение серьезных побочных эффектов на 20%, тогда как исходы для других макрососудистых и микрососудистых событий были аналогичны таковым при стандартном снижении уровня АД. Более интенсивное снижение АД (<130 мм рт.ст.) привело к уменьшению числа инсультов, не повлияв на частоту других событий.
В любом случае, согласно мета-регрессионному анализу, наблюдалось дальнейшее снижение риска инсульта при достижении АД <120 мм рт.ст., однако при уровне АД <130 мм рт.ст. было выявлено увеличение на 40% серьезных нежелательных явлений при отсутствии позитивного влияния на другие исходы. В мета-анализе 31 экспериментального исследования Ребольди (Reboldi) и соавт. изучили 73 913 пациентов, страдающих сахарным диабетом. У пациентов с более жестким контролем АД риск инсульта снижался на 31%, при этом статистически значимого снижения риска инфаркта миокарда выявлено не было. В другом мета-регрессионном анализе отмечено снижение риска инсульта на 13% при снижении систолического АД на каждые 5 мм рт.ст. и на 11,5% при снижении диастолического АД на каждые 2 мм рт.ст.; между риском инфаркта миокарда и степенью снижения АД отмечено не было. McBrien с коллегами включили в свой мета-анализ 5 исследований с участием 7312 пациентов, сравнив заранее заданные целевые значения АД и оценивая один из исходов: смертность, инфаркт миокарда или инсульт.
Целевое АД <130/80 мм рт.ст. (интенсивное лечение) было связано с более низким риском инсульта по сравнению с достижением АД <140—165/85—100 мм рт.ст. (стандартное лечение), но абсолютная разница в риске между группами была очень небольшой; статистически значимых различий в риске смерти или инфаркта миокарда также не было обнаружено. Исследование McBrien и соавт. отличалось от предшествующих мета-анализов тем, что в него были включены только испытания, сравнивающие пациентов по достигнутому уровню АД, а не по заранее назначенному лечению; таким образом польза от снижения АД может быть связана, в частности, с исходным систолическим АД, а не с выбранными целевыми показателями.
Более того, в этом мета-анализе учитывались результаты крупнейшего исследования ACCORD-BP, в котором участвовало 65% всего населения, и, как известно, в этом исследовании интенсивная терапия приводила к повышению частоты серьезных побочных эффектов. В 2013 г. Arguedas и соавт. подготовили мета-анализ, включающий те же 5 рандомизированных испытаний, рассмотренных Макбрайеном, набрав в общей сложности 7314 участников со средним сроком наблюдения 4,5 года. Фактически исследователи независимо друг от друга провели исследования, в которых пациентам устанавливались разные целевые значения систолического или диастолического АД. В группе с более низким значением систолического АД единственным наблюдаемым преимуществом являлось снижение частоты инсультов; но так или иначе попытки достичь более низкого целевого АД увеличивали количество серьезных побочных эффектов. У участников с меньшим значением диастолического АД была обнаружена тенденция к снижению общей смертности, в основном из-за тенденции к более низкой смертности, не связанной с ССЗ; не было обнаружено различий в отношении инсульта, инфаркта миокарда или застойной сердечной недостаточности.
В 2015 г. было продемонстрировано, что сахароснижающий препарат эмпаглифозин обладает антигипертензивным эффектом. В исследовании EMPA-REG ВР оценивалось лечение эмпаглифозином, ингибитором Na+/ глюкозного котраспортера 2-го типа (иЕ1ГЛТ-2), в течение 12 нед, при этом было продемонстрировано клинически значимое улучшение показателей суточного систолического и диастолического АД по сравнению с плацебо с одновременным снижением как дневного, так и ночного АД, среднечасового амбулаторного и офисного АД. Более того, эмпаглифозин, более выражение снижая дневное АД по сравнению с ночным, не влиял на его циркадный ритм. Было показано, что эффекты снижения АД сохраняются независимо от количества принимаемых антигипертензивных препаратов и использования диуретиков или ингибиторов АПФ/блокаторов рецепторов ангиотензина. Было также исследовано влияние эмпаглифозина на снижение риска сердечно-сосудистых заболеваний в исследовании «Эмпаглифозин, сердечно-сосудистые исходы и смертность при диабете 2-го типа» (EMPA-REG OUTCOME).
В течение 3,1 года 7028 пациентов с СД 2-го типа и высоким риском сердечно-сосудистых заболеваний получали эмпаглифозин в дозе 10 или 25 мг. Первичный исход, включающий нефатальный инфаркт миокарда, нефатальный инсульт или смерть от сердечно-сосудистых причин, развивался у 10,5% пациентов, получавших эмпаглифозин, по сравнению с 12,1% пациентов в группе плацебо. Кроме того, были продемонстрированы более низкие показатели госпитализации по поводу сердечной недостаточности, смертности от всех причин и смерти от сердечно-сосудистых причин. В другом анализе исходов, связанных с функцией почек, исследованиями ЕМ PA-REG OUTCOME было описано снижение частоты заранее заданных исходов в виде развития или прогрессирования нефропатии. Это значительное снижение сердечно-сосудистых событий у пациентов с сахарным диабетом может происходить в результате снижения АД, гликированного гемоглобина, массы тела, висцерального ожирения, мочевой кислоты и альбуминурии. В частности, различия в результатах объясняются скорее гемодинамическим, а не метаболическим механизмом из-за короткого времени воздействия (недели). Способность всех препаратов группы иНГЛТ-2 снижать АД — известное явление. В рандомизированных исследованиях степень снижения АД варьируется от 3 до 5 мм рт.ст. для систолического АД и от 1 до 3 мм рт.ст. для диастолического АД по сравнению с плацебо или другими сахароснижающими препаратами.
Возможно, это связно с умеренным натрийуретическим и мочегонным эффектом этого класса препаратов из-за комбинации частичного ингибирования реабсорбции Na+ в проксимальных канальцах и повышенной глюкозурии, оказывающей мягкий осмотический эффект в почечных канальцах. Другими упоминаемыми механизмами являются подавление секреции ренина из-за небольшого увеличения концентрации Na+ в канальцах в области плотного пятна и перехода от окисления глюкозы к окислению жирных кислот, что приводит к увеличению уровней кетонов, то есть бета-гидроксибутирата.
Наконец, было обнаружено, что иНГЛТ-2 снижают пульсовое давление, среднее артериальное давление и двойное произведение по сравнению с плацебо, возможно, действуя на некоторые сигнальные молекулы и медиаторы артериальной ригидности, но без компенсаторного увеличения частоты сердечных сокращений. Для эмпаглифозина, применяемого в дозе 25 мг в течение 8 нед у пациентов с сахарным диабетом 1-го типа без осложнений, во время эугликемического и гипергликемического клэмп-теста было показано снижение скорости распространения каротидно-лучевой пульсовой волны без индукции рефлекторной симпатомиметической активности. Chilton и соавт. продемонстрировали, что эмпаглифозин значительно снижает систолическое АД по сравнению с плацебо в группе «дипперов» и в группе «нон-дипперов» с высоким риском, не влияя на среднее систолическое АД во время сна у «нондипперов» и не изменяя ни частоту сердечных сокращений, ни суточный ритм АД как у «дипперов», так и у «нон-дипперов». На данный момент совершенно ясны две концепции.
Во-первых, любое повышение АД в значительной мере и напрямую связано со смертностью от сосудистых причин (инсульт, ишемическая болезнь сердца и другие сосудистые заболевания) у взрослых пациентов, начиная с уровня АД 115/75 мм рт.ст. Во-вторых, было доказано, что снижение АД действительно уменьшает риск сердечно-сосудистых осложнений, но при достижении очень низких значений АД как у пациентов с гипертонией, получающих лечение, так и у тех пациентов, кто его не получает, было зарегистрировано увеличение смертности от сердечно-сосудистых заболеваний и серьезные побочные эффекты. Эти идеи способствовали развитию гипотезы о J-образной кривой АД, то есть о возможной J-образной, а не линейной зависимости степени снижения АД и возникновения сердечно-сосудистых событий. Споры о J-образной кривой АД все еще продолжаются и, похоже, закончатся не скоро. Согласно последним данным, гипотеза J-образной кривой нуждается в переформулировке после оценки того, может ли восходящая часть кривой являться результатом снижения АД, вызванного применением лекарственных средств (Mancia и Grassi, 2014). Более того, разные нижние границы АД строго зависят от характеристик пациента (например, ишемическая болезнь сердца до или после проведения реваскуляризации).
Также важно учитывать, что антигипертензивная терапия может вернуть способность кровеносной системы к саморегуляции и привести к нормотонии, но при сердечно-сосудистых заболеваниях риск снижения АД ниже предела саморегуляции кровообращения может быть выше. J-образная взаимосвязь между снижением АД и сердечно-сосудистыми событиями наблюдалась в большом количестве обсервационных исследований, при этом было продемонстрировано, что агрессивный подход к снижению АД не только не приводил к дополнительным положительным эффектам, но и вызывал снижение или исчезновение зависимого от уровня АД защитного воздействия на сердечно-сосудистую систему.
Интересно, что феномен J-кривой наблюдается не только в отношении фатальных и нефатальных событий, но также в отношении серьезных сердечно-сосудистых заболеваний (сердечная недостаточность, инфаркт миокарда, инсульт) и почечных осложнений (серьезное ухудшение функции почек или терминальная стадия почечной недостаточности). Следует учитывать некоторые ограничения, касающиеся J-образной кривой. Во-первых, количество пациентов и событий в подгруппах с самым низким АД часто очень невелико, и поэтому возможно некоторое смещение относительно истинных значений. Более того, нет никаких доказательств, что снижение АД легче достигается у пациентов с высоким риском сердечно-сосудистых заболеваний, обычно наблюдается обратная ситуация. Во-вторых, во многих крупномасштабных исследованиях J-образная связь между целевыми значениями АД и сердечно-сосудистыми исходами была описана после корректировки некоторых исходных независимых переменных, что предполагает роль различных демографических и клинических характеристик, ассоциированных с риском. Наконец, противники гипотезы J-кривой напоминают, что не все ретроспективные анализы крупномасштабных исследований, таких как UKPDS и ACCORD, выявили повышенный риск сердечно-сосудистых событий у пациентов, у которых была применена агрессивная тактика лечения (1998; Xiang и соавт., 2010).
Наконец, уровень АД играет ключевую роль в перфузии органов, поэтому нет никаких сомнений в том, что значения АД, при которых перфузия недостаточна, существуют, а гипотеза о J-образной связи между АД и исходами сердечно-сосудистых заболеваний все еще актуальна. Как физиологические, так и наблюдательные исследования показали, что к появлению восходящей части J-кривой приводят значения АД, обусловленные антигипертензивной терапией, особенно у лиц с высоким риском сердечно-сосудистых заболеваний. Однако на основании этих исследований невозможно получить убедительные данные, поскольку только в рандомизированных исследованиях возможно окончательно установить, появляется ли J-образная кривая во время антигипертензивной терапии и когда (Mancia и Grassi, 2014). С практической точки зрения врачи должны рассматривать потенциальное появление J-образной кривой как основную проблему у пациентов с высоким риском сердечно-сосудистых заболеваний.
Эта проблема не обошла стороной также и последние европейские клинические рекомендации по лечению артериальной гипертензии, в которых целевые значения АД для пациентов с сахарным диабетом, сердечно-сосудистым событием в анамнезе и прогрессирующим заболеванием почек были увеличены с <130/90 до <140/90 мм рт.ст. (140/85 мм рт.ст. при сахарном диабете), а у пожилых пациентов значения систолического АД рекомендовано поддерживать в диапазоне от 140 до 150 мм рт.ст. (Mancia и соавт., 2013). В табл. 2.2 представлен обзор целевых показателей АД у пациентов с диабетом в соответствии с основными рекомендациями (2012; American Diabetes, 2017; James и соавт., 2014; Leung и соавт., 2016; Mancia и соавт., 2013; Weber и соавт., 2014).
Видео этиология, патогенез сахарного диабета, гипергликемии, кетоацидоза
- Вернуться в оглавление раздела "Эндокринология"
Редактор: Искандер Милевски. Дата обновления публикации: 7.12.2023
