Патогенез ВИЧ-инфекции желудочно-кишечного тракта
Исследования причины развития нарушений со стороны ЖКТ показали присутствие ВИЧ в слизистой оболочке кишечника у пациентов с кишечными расстройствами, а также у пациентов на бессимптомной стадии развития инфекции. Некоторые исследования продемонстрировали, что определенные изоляты ВИЧ-1 могут инфицировать клетки кишечника за счет CD4-независимого механизма.
В связи с этим важно отметить, что эпителиальные клетки содержат рецепторы к хемокинам и другие потенциальные структуры на клеточной мембране для связывания и возможного поглощения вирусов. Во многих случаях, особенно у людей с концентрацией CD4+-лимфоцитов выше 200 клеток/мкл, ВИЧ является единственным патогеном, который обнаруживается в кишечнике. Таким образом, вирус может «поселяться» в этом органе, так же как и в мозге. Комплемент может усиливать инфицирование эпителиальных клеток и участвовать в распространении вируса через кишечник и шейку матки.
Обращает на себя внимание присутствие ВИЧ в хромаффинных клетках слизистой кишечника. Эти цитокин- и гормон-продуцирующие клетки разбросаны на всем протяжении кишечного тракта и отвечают за нормальную моторику и функции кишечника.
ВИЧ-инфекция кишечника особенно ярко выражена в лимфоидных тканях ЖКТ. Содержание лимфоцитов в ЖКТ весьма велико; лимфоидные структуры ЖКТ называют GALT - gutassociated lymphoid tissue, т.е. ассоциированная с кишечником лимфоидная ткань, состоящая из фолликулов (пейеровы бляшки, индуктивный компонент) и лимфоцтитов собственной пластинки (Т-лимфоциты lamina propria, эффекторный компонент). Активированные антигенами CD4+-клетки экспрессируют CCR5 и мигрируют в базальную пластинку в качестве эффекторных Т-лимфоцитов кишечника. При уменьшении количества антигенов они превращаются в покоящиеся CCR5+-клетки.
Один из механизмов, обеспечивающих миграцию CD4 Т-клеток в стенку кишки, связан с экспрессией на лимфоцитах адгезивных молекул «аддрессинов к клеткам слизистой оболочки 1»; экспрессия этих адрессинов возрастает при развитии оппортунистических инфекций кишечника. Недавно проведенные исследования показали, что через несколько дней после острого инфицирования проникший R5-вирус связывается с активированными и покоящимися CCR5-экспрессирующими CD4+-Т-клетками памяти в базальной пластинке. Покоящиеся клетки, по-видимому, представляют собой недавно активированную популяцию клеток, которые вновь вернулись в состояние покоя (отрицательные по антигенам CD25 и Ki67).
Они экспрессируют достаточное количество CCR5-рецепторов, достаточный уровень нуклеотидов и активаторов транскрипции, в результате чего в них, в отличие от настоящих покоящихся CD4+-Т-клеток, поддерживается продуктивная ВИЧ-инфекция.
Как наблюдается при SIV-инфекции, в кишечнике происходит очень раннее инфицирование и разрушение CD4+-клеток R5 биотипом ВИЧ, которое продолжается на всем протяжении инфекции. Гибель CD4+-клеток в кишечнике, впервые описанная несколько лет назад, также может быть связана с апоптозом, индуцированным вирусами биотипа R5. В некоторых исследованиях наблюдали селективную передачу R5-виpyca на CD4+-клетки от эпителиальных клеток кишечника, экспрессирующих DC-SIGN и CCR5. Кишечная инфекция носит непрерывный характер в связи с постоянным поступлением CD4+-Т-клеток из кровотока.
Считают, что примерно 80% покоящихся CD4+-Т-клеток в кишечном тракте (в особенности в базальной пластинке) и в других тканях организма (в частности, в крови и лимфоидной ткани) разрушаются в течение 4-10 дней после проникновения вируса в организм. Эти клетки погибают вследствие прямого цитопатогенного действия вируса, убийства цитотоксическими Т-лимфоцитами или Fas/Fas-лиганд-зависимого апоптоза, который, скорее всего, активируется под действием белков оболочки вируса. Апоптозу в большей степени подвергаются CD4+-, но не CD8+-клетки.
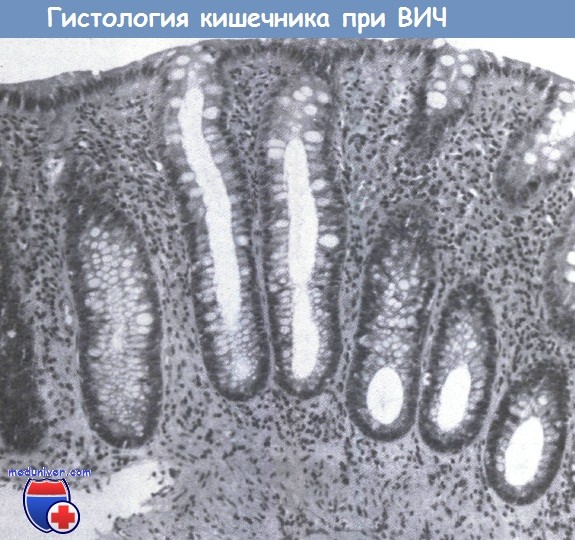
Биопсия толстой кишки ВИЧ-инфицированного пациента с хронической диареей на фоне отсутствия определяемых патогенов.
В образце, полученном при биопсии, наблюдаются только признаки умеренно выраженного хронического воспаления, без повреждения эпителиальных клеток или острого воспаления.
(Гематоксилин и эозин; оригинальное увеличение, х125.)
Гибель CD4+-клеток приводит к наиболее неблагоприятным последствиям в ЖКТ, поскольку большинство клеток базальной пластинки представляет собой покоящиеся клетки памяти. В этой ткани, как и в периферических лимфатических узлах, происходит гибель как инфицированных, так и неинфицированных клеток. Существенно уменьшается количество CCR5+-CD4+-T-клеток, экспрессирующих рецептор тропности к кишечнику интегрин а4b7; такие CD4+-клетки могут восстанавливаться при проведении противоретровирусного лечения. Гибель CD4+-клеток в кишечнике, возможно частично, отвечает за уменьшение вирусемии после стадии острой инфекции (вследствие уменьшения количества клеток-мишеней).
В результате действия вируса у обезьян с хронической SIV-инфекцией в слизистой оболочке содержится всего от 1 до 3% от нормального количества CD4+-Т-клеток; при развитии заболевания их число уменьшается до 0,5%. Эти данные, полученные на приматах, также говорят в пользу того, что в первые дни после инфицирования клеточный компонент иммунного ответа, который должен реагировать на попадания различных патогенов в организм, либо быстро блокируется, либо вообще не активируется. Аналогичные наблюдения недавно были сделаны при внутривлагалищной инокуляции SIV; противовирусная реакция CD8+-клеток развивалась существенно позже. В некоторых случаях при проведении исследований в кишечнике животных обнаруживаются оппортунистические инфекции. У обезьян с небольшим содержанием вируса в ЖКТ клинический прогноз заболевания был более благоприятным. Восстановление CD4+-клеток, которое, по-видимому, замедляется, может определять клинический исход заболевания.
Во многих случаях при хронической ВИЧ-инфекции в ЖКТ обнаруживается некоторое количество Т-клеток, но обычно CD4+-Т-клетки присутствуют там в очень небольшом количестве. Эти наблюдения говорят о том, что показатели периферической крови не всегда отражают реальное состояние клеток иммунной системы организма в целом. Как упоминали выше, уже известно, что количество циркулирующих в крови CD4+-клеток, среди которых клетки памяти составляют всего 15%, может не отражать ситуацию, наблюдающуюся в лимфатических узлах.
В настоящее время этот факт получил подтверждение в виде данных об интенсивности инфицирования лимфоидной ткани ЖКТ, в которой содержится большое количество CD4+-клеток памяти. Кроме того, небольшое содержание CD4+-Т-клеток не всегда связано с текущими процессами поступления, инфицирования и гибели CD4+-клеток.
Важно отметить, что не всегда возможно быстрое вторичное заселение CD4+-клеток в кишечник, даже после проведения HAART, несмотря на увеличение количества циркулирующих CD4+-клеток. Отчасти недостаточное восстановление CD4+-клеток объясняется продолжением репликации вируса в лимфоидной ткани кишечника, что, скорее всего, связано с недостаточным действием HAART в тканях слизистой оболочки.
При успешном проведении противоретровирусной терапии на ранних стадиях инфекционного процесса на модели SIV наблюдали полное восстановление лимфоидных тканей кишечника. Проведение HAART также приводит к уменьшению концентрации РНК ВИЧ и апоптоза, а также клинических симптомов вирусной инфекции в кишечнике.
Данные о гибели CD4+-клеток в кишечнике являются аргументом за раннее назначение антиретровирусного лечения при ВИЧ-инфекции (в течение первых дней после заражения), до серо-конверсии. В противном случае большую часть повреждений лимфоидных тканей кишечника, происходящих на ранней стадии, нельзя предотвратить. Кроме того, поскольку у пациентов, получающих HAART, не наблюдается существенного восстановления CD4+-Т-клеток в ЖКТ, крайне необходима разработка методов, позволяющих вернуть лимфоидные клетки в этот важнейший орган.
Некоторые исследователи считают, что в данном случае были бы особенно эффективны методы лечения, обеспечивающие защиту ССR5+-клеток. Этот вопрос требует дальнейшего изучения.
Несмотря на то, что CD4+-клетки базальной пластинки рассматриваются в качестве первичной мишени для ВИЧ в ЖКТ, некоторые исследования на человеке показали признаки ВИЧ-инфекции в макрофагах, в особенности при появлении симптомов со стороны кишечника. Моноциты крови мигрируют в слизистую оболочку, где происходит их дифференцировка в макрофаги базальной пластинки в присутствии факторов, выделяемых клетками стромы. Инфицированные макрофаги, несмотря на их небольшое содержание (0,06% от общего числа мононуклеарных клеток базальной пластинки), могут являться важным резервуаром вируса и источником некоторых токсичных цитокинов.
Скорее всего, они представляют собой клетки, сохранившиеся в ЖКТ после того, как произошло сильное уменьшение количества CD4+-клеток.
В поддержку этих данных, касающихся ВИЧ-инфицирования ЖКТ, были описаны штаммы ВИЧ кишечного происхождения, обладающие некоторыми особенностями, отличающими их от вирусов, выделенных из крови тех же пациентов. Как отмечали выше, эти вирусы обычно представляют собой R5-изоляты, обладающие сродством к макрофагам. Кроме того, в изолятах SIV, выделенных из кишечника и мозга одних и тех же обезьян, обнаруживались генетические особенности, позволяющие предполагать независимую эволюцию разновидностей вируса в этих органах организма животного. Такая же картина может быть характерна и для ВИЧ.
- Читать "Значение белков ВИЧ и цитокинов в поражении кишечника"
Оглавление темы "ВИЧ-инфекция":- Влияние ВИЧ на кишечник (желудочно-кишечный тракт)
- Патогенез ВИЧ-инфекции желудочно-кишечного тракта
- Значение белков ВИЧ и цитокинов в поражении кишечника
- Влияние ВИЧ на почки
- Влияние ВИЧ на сердце
- Влияние ВИЧ на легкие, суставы, надпочечники
- Резюме по влиянию ВИЧ на ткани и органы
- Врожденный иммунитет при ВИЧ инфекции
- TLR-рецепторы при ВИЧ инфекции
- Типы дендритных клеток и ВИЧ
