Резюме влияния ВИЧ на нервную систему
Поскольку определенные признаки поражения нервной системы (например, многоядерные клетки и вакуолярная миелопатия) непосредственно ассоциированы с ВИЧ-инфекцией, необходимо учитывать возможность того, что нейропатогенез обусловлен инфицированием мозга нейротропными штаммами ВИЧ.
Этоти варианты вируса образуются из циркулирующего вируса, способного к эффективной репликации в эндотелиальных клетках, и в особенности в астроцитах, что вызывает повреждение гематоэнцефалического барьера. Тем не менее до сих пор неясно, откуда в мозге появляются вирусы биотипа R5 со сродством к макрофагам, выступающие в качестве патогенного изолята, если эндотелиальные клетки мозга и астроциты инфицируются преимущественно вирусами биотипа Х4.
Предполагают, что R5-вирус не попадает в мозг при инфицировании гематоэнцефалического барьера, но проникает путем диапедеза инфицированных клеток или путем трансцитоза вирусов. Эволюция Х4-вирусов в мозге представляется менее вероятной, чем такое селективное проникновение. Активированные инфицированные CD4+-лимфоциты и макрофаги (например, CD163+) могут проникать в ЦНС и таким путем переносить вирус (скорее всего, R5) в мозг. Выделение R5-вирусов из ЦНС говорит в поддержку этого механизма.
Нарушение функции гематоэнцефалического барьера, вызванное ВИЧ-инфекцией, также приводит к развитию патологий ЦНС вследствие проникновения токсических продуктов, а также вируса и инфицированных клеток. Впоследствии в результате определенных мутаций появляются нейротропные штаммы, которые начинают хорошо реплицироваться в макрофагах и, возможно, в микроглие и других клетках мозга и продуцируют вирусные белки (например, gp120, gp41, Tat и Nef), которые могут быть токсичными для клеток.
Кроме того, эти вирусные продукты способны конкурировать с нейротропными факторами и вмешиваться в межклеточные взаимодействия. При ВИЧ-инфекции наблюдается гибель нейронов во фронтальной коре, которая возникает в результате как самой вирусной инфекции, так и ее последствий.
Вирусы R5, обладающие сродством к макрофагам, также могут легко проникать в другие клетки мозга, в частности в олигодендроциты, вырабатывающие миелин, который необходим для осуществления передачи сигнала по нервным волокнам. R5-вирусы, обладающие сродством к макрофагам, имеют специфические особенности, определяющие их нейровирулентные свойства.
Специфическое инфицирование макрофагов и других клеток мозга (например, астроцитов) также может приводить к усилению выработки токсических клеточных факторов, которые повреждают другие клетки мозга и миелин. ВИЧ-инфицирование астроцитов может вызывать множество последствий, приводящих к поражению нервной системы, поскольку эти клетки играют важную роль в обезвреживании токсических веществ в ЦНС.
Таким образом, роль этих клеток, обеспечивающих механизмы неспецифической резистентности к инфекциям, в заболеваниях мозга заслуживает особого внимания. Кроме того, исследователи изучают возможную роль комплемента в предотвращении ВИЧ-инфицирования мозга или обострения нейропатогенеза. Существенно, что все воздействия, направленные на ограничение репликации и распространение ВИЧ, должны приводить к уменьшению неврологической симптоматики.
Такие результаты были получены в ранних исследованиях у пациентов, получавших противовирусное лечение; выраженность симптомов деменции при СПИДе существенно уменьшалась, по крайней мере на некоторое время. Эти обнадеживающие результаты были приписаны действию HAART, направленному против ВИЧ, и/или против выработки цитокинов. Тот факт, что деменция обратима при использовании одного только азидотими-дина, говорит о том, что по крайней мере на начальных стадиях инфекционного процесса ВИЧ его белки и индуцируемые инфекцией цитокины нецитотоксичны. С помощью HAART можно частично ослабить воздействие инфекции на мозг, по крайней мере на период времени, в течение которого препараты хорошо проникают через гематоэнцефалический барьер.
Тем не менее заболевания ЦНС все еще встречаются, хотя и с меньшей частотой, но случаи нарушения мозговых функций у пациентов, получающих HAART, учащаются.
Аутоантитела также, по-видимому, участвуют в развитии некоторых неврологических расстройств, особенно периферических нейропатий, как показывают методы иммуногистохимического окрашивания, и успешно лечатся с помощью плазмафереза. Роль других вирусов в поражении нервной системы, если и не первична, то тем не менее присутствует и может быть существенна. Наконец нарушение метаболизма витамина В12 при ВИЧ-инфекции также позволяет предположить, что некоторые патологические изменения в нервной системе связаны с его дефицитом.
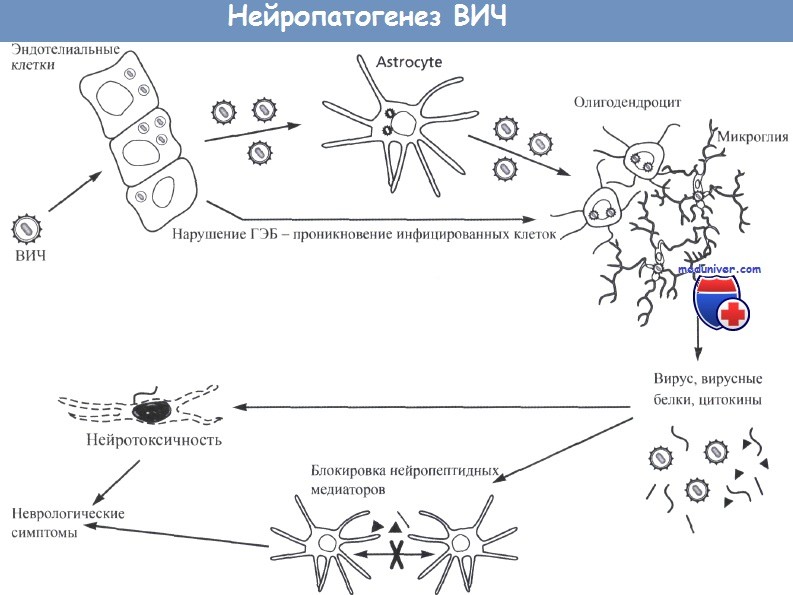
Предположительно вирус инфицирует эндотелиальные клетки капилляров мозга и проникает через базолатеральную поверхность этих клеток к астроцитам, выстилающим гематоэнцефалический барьер (ГЭБ).
Инфицирование обоих типов клеток приводит к нарушению целостности ГЭБ и проникновению в мозг инфицированных Т-клеток и макрофагов.
В результате этого осуществляется ВИЧ-инфицирование других клеток мозга (например, олигодендроцитов и микроглии).
Затем начинается продукция ВИЧ и вирусных белков, а также высвобождение различных цитокинов (в частности, TNF и низкомолекулярных веществ).
Эти вещества могут вызывать нарушение межклеточной передачи сигнала, блокируя действие нейротропных факторов.
Прямое инфицирование клеток, а также высокая концентрация вирусных белков (например, гликопротеинов оболочки, Tat, Nef) и цитокинов оказывают прямое токсическое действие на нервные клетки, повреждая их мембрану.
- Вернуться в оглавление раздела "Инфекционные болезни"
Оглавление темы "Поражение нервной системы при ВИЧ":- Влияние белка gp120 ВИЧ на нервную систему
- Влияние белка Tat ВИЧ на нервную систему
- Влияние белков gp41 и Nef ВИЧ на нервную систему
- Влияние белка TNF ВИЧ на нервную систему
- Влияние цитокинов на нервную систему при ВИЧ
- Влияние макрофагов на нервную систему при ВИЧ
- Влияние астроцитов на нервную систему при ВИЧ
- Влияние аутоиммунных процессов на нервную систему при ВИЧ
- Влияние ЦМВ на нервную систему при ВИЧ
- Резюме влияния ВИЧ на нервную систему
