Лучевая терапия плоскоклеточного рака. Влияние быстрых электронов на плоскоклеточный рак
Нахождение оптимальных режимов фракционированного облучения является одним из основных путей дальнейшего повышения эффективности лучевой терапии. Между тем до настоящего времени остается не решенным вопрос, насколько существен вклад того или иного временного параметра в лечебный эффект ионизирующих излучений при лучевой терапии злокачественных новообразований.
Цель настоящей работы — изучение влияния числа фракций на терапевтический эффект быстрых электронов при облучении плоскоклеточного рака мышей.
Эксперименты были поставлены на 105 мышах-самцах линии СС57 Br. В качестве опухолевого штамма использовался перевиваемый плосклеточный рак преджелудка. Общепринятым методом опухоль преджелудка перевивали в мышцу бедра правой задней конечности. На 10-й день после перевивки, когда опухоли достигали в диаметре 9—10 мм, животных разделяли на группы и начинали локальное облучение быстрыми электронами, которые генерировались линейным ускорителем ЛУЭ-25. Опухоли облучались в проходящем пучке электронов с энергией 22 Мэв при мощности дозы 100—120 рад/мин. Для облучения использовался десятисекционный радиалыю-симметричпый станок, изготовленный из плексигласа (толщиной нижней стенки 1 см). Мыши с перевитыми в заднюю конечность опухолями привязывались за лапки к центру станка таким образом, чтобы опухоли плотно прилегали друг к другу. Для улучшения распределения дозы по облучаемому объему под станок помещали парафин толщиной 3 см.
При таком способе облучения все опухоли располагались в зоне 90% изодозы. Каждый сеанс облучения электронами контролировался ионизационной камерой (монитором) дозиметра «автомат-доза». Общая ошибка в измерении дозы равнялась ±3%, Я неоднородность распределения дозы но облучаемому объему не превышала 10%, что соответствует рекомендациям Международной комиссии по радиационным единицам и защите (ICRV, report 10, 1962). На рисунке представлена схема экспериментов, а подробная характеристика испытанных в этой работе режимов облучения приведена в таблице.
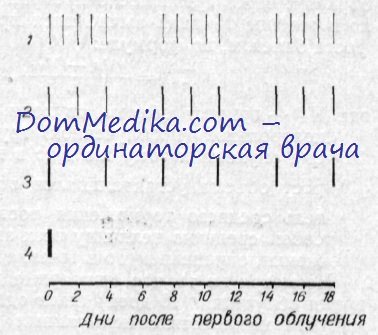
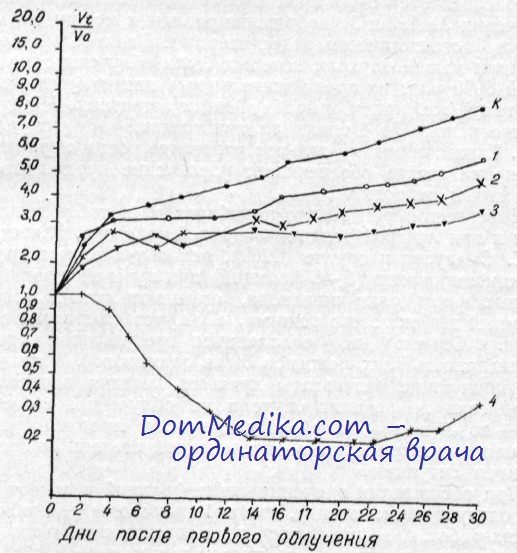
Терапевтическая эффективность режимов облучения оценивалась по средней продолжительности жизни животных-опухоленосителей и по изменению объема опухолей. Последнее определялось отношением Vt/V0 , где V0 —объем опухоли перед облучением, Vt — объем опухоли к определенному дню опыта. За критерий количественной оценки противоопухолевого эффекта применялся показатель среднего торможения роста (%). который определялся следующим образом: через сутки после прекращения облучения ежедневно в течение 10 дней вычислялся процент торможения (ПТ) роста бластом, по формуле: ПТ=(Vk-Vоп) /Vk 100%, где VK — прирост объема опухоли к определенному дню в контрольной (нсоблученной) группе, Von — прирост объема опухоли к тому же дню в подопытной группе. Прирост объема устанавливался отношением Vt/V0.
Показатель среднего торможения роста опухолей представлял собой среднюю величину всех значений процента торможения, определяемого в течение 10 дней. Несмотря на то, что суммарные дозы (6000 рад) и общее время облучения (18 дней) были одинаковыми, реакция преджелудка на действие испытанных режимов была довольно различной. При анализе кривых прироста объема опухолей и показателей среднего торможения опухоли преджелудка можно отметить определенную закономерность, выражающуюся в том, что с уменьшением числа фракций возрастает ингибпрующее действие быстрых электронов на плоскоклеточный рак. Так, при режиме № 4 (облучение одной фракцией) не наблюдалось не только прироста объема опухоли, но даже наступила выраженная регрессия. При режиме № 3 (6 фракций) с 11-го дня После начала облучения и до 25-го преджелудок практически не увеличивался. При режимах же № 1 и 2, где суммарная доза отпускалась соответственно 15 и 9 фракциями, прирост объема опухоли продолжался, хотя и медленнее по сравнению с необлученными опухолями.
Следует отметить, что ранее аналогичная зависимость противоопухолевого эффекта быстрых электронов от числа фракции была получена при облучении опухоли Эрлиха (А. П. Козлов и др., 1973).

Однако лечебный эффект лучевой терапии не обусловливается только реакцией опухоли на воздействие ионизирующего излучения. Она скорее характеризует радиочувствительность бластомы. Общеизвестно, что лучевая чувствительность и лучевая излечимость опухоли — понятия неидентичные (Fletcher, 1965). Именно поэтому, эффективность того или иного метода лучевого или какого-либо другого вида лечения определяется, в первую очередь, по срокам продолжительности жизни больного. В связи с этим, мы также использовали критерии средней продолжительности жизни мышей-опухоленосителей для оценки терапевтического эффекта быстрых электронов при облучении опухоли преджелудка.
Оказалось, что при облучении плоскоклеточного рака режимом № 1 мыши жили в среднем 48,1 ±2,4 дня, при режиме № 2 — 50,0±2,1, при режиме № 3 —45,3±2,5 и при режиме № 4 — 38,0±3,4, животные контрольной группы — 36,6± ±3,4 дня. Следовательно, продолжительность жизни мышей-опухоленосителей была практически одинаковой при режимах облучения № 1,2 и 3 (небольшие различия между режимами № 2 и 3 статистически недостоверны). Значительно меньше прожили мыши, опухоли которых были облучены однократно дозой 6000 рад; их продолжительность жизни была фактически такой же, как и у необлученных животных. Между тем, именно режим № 4 оказывал наибольший эффект на опухоль. Таким образом, сильное угнетение роста опухолей еще далеко не всегда обеспечивает увеличение продолжительности жизни животного.
Интересно отметить, что подобного рода наблюдения имеются и при лучевой терапии опухолей человека. В частности, А. С. Смагулов и другие (1969), используя режим крупного фракционирования (5—6 фракций) при лучевой терапии запущенных форм рака пищевода, отмечают лучший непосредственный эффект этого режима, чем курса ежедневного облучения. Однако но отдаленным результатам лечения эффективность этих режимов была одинаковой. Если учесть, что ближайшие результаты лучевого лечения определяются фактически по реакции опухоли па облучение, а отдаленные — по 3- или 5-летней выживаемости, то можно увидеть, что наши эксперименты в определенной степени моделируют сходную ситуацию.
При обсуждении значения числа фракций в лучевой терапии следует иметь в виду, что в большинстве радиобиологических работ, где учитывается повреждающее действие радиации, будь то выживаемость клеток в культуре Elkind, Sutton, 1960) или реакция кожи (Fowler и др., 1963), уменьшение числа фракций приводит к повышению эффекта. При этом обнаруживается прямая зависимость между биологическим эффектом суммарной дозы и числом фракций. Последнее дает основания Fowler считать, что число фракций и, следовательно, доза за фракцию играют большую роль в биологическом действии ионизирующего излучения, чем общее время облучения. Судя по нашим экспериментальным данным, это положение вполне правильно в отношении реакции опухоли на облучение. Однако в отношений такого интегрального показателя, как продолжительность жизни, число фракций не играет такой определяющей роли.
Это, вероятно, связано с тем, что продолжительность жизни животного-опухоленосителя (или выживаемость человека со злокачественным новообразованием), подвергающегося лучевому лечению, обусловлена не только действием радиации на опухоль, по и реакцией нормальных тканей, а также существующим взаимоотношением опухоль—организм. В связи с этим не исключено, что на продолжительность жизни большее влияние оказывает общее время облучения, чем число фракций. Для выяснения этого вопроса необходимы дальнейшие исследования по определению зависимости терапевтического эффекта ионизирующих излучений от общего времени облучения разных режимов фракционирования дозы.
- Читать "Анатомия лучевой терапии. Ткани под действием лучевой терапии"
Оглавление темы "Лечение злокачественных опухолей":- Реанимация онкологических больных. Остановка сердца во время операции в онкологии
- Лимфоузлы при раке пищевода. Телегамматерапия при раке пищевода
- Регрессивные изменения опухоли под влиянием телегамматерапии. Предоперационная телегамматерапия
- Лучевая терапия при раке пищевода. Лимфоузлы после лучевой терапии
- Значение бензпирена в экологии. Бензпирен в городе Андижан
- Стимуляция гемопоэза при химиотерапии. Ферант и НК-5 в ходе лучевой терапии
- Мегавольтная лучевая терапия при раке. Оптимальная доза лучевой нагрузки
- Оптимальный план лучевой терапии. Лучевая терапия при раке пищевода и легкого
- Лучевая терапия плоскоклеточного рака. Влияние быстрых электронов на плоскоклеточный рак
- Анатомия лучевой терапии. Ткани под действием лучевой терапии
