Актиновый цитоскелет и фокальные контакты трансформированных опухолевых клеток
Для трансформированных клеток характерными являются дефектное формирование актиновых микрофиламентов и стресс-фибрилл, а также серьезные структурные и функциональные изменения в фокальных контактах.
Нарушения фокальных контактов охватывают все компоненты последних: интегриновые рецепторы, цитоплазматические белки и цитоскелетные элементы, связанные с фокальными контактами.
Трансформация чаще всего сопровождается ослаблением экспрессии и/или снижением аффинности определенных интегринов к их лигандам во внеклеточном матриксе, а также утратой их способности к кластерообразованию.
Молекулы, участвующие в формировании фокальных контактов — интегрины, FAK, винкулин, паксиллин, являются мишенями для гиперфосфорилирования онкобелками (продуктами онкогенов), обладающими тирозинкиназной активностью, в частности белком онкогена SRC. Гиперфосфорилирование приводит к нарушению связей между отдельными белками фокального контакта, снижению способности актиновых микрофиламентов к «заякориванию», что в свою очередь ослабляет их центростремительное натяжение и препятствует образованию стресс-фибрилл.
Гиперфосфорилирование цитоплазматического домена интегрина, возможно, лежит в основе снижения аффинности у интегриновых рецепторов и утраты ими способности к кластерообразованию. Это касается, например, рецептора a5b1 к фибронектину.
Описанные нарушения ведут к дефектности формирования фокальных контактов и ослаблению адгезии трансформированных клеток к определенным компонентам внеклеточного матрикса. Снижение адгезии усугубляется тем, что трансформированные клетки частично или полностью утрачивают способность к синтезу определенных белков матрикса, например фибронектина или коллагена.
Нарушения фокальных контактов при трансформации касаются не только их адгезивных функций, но также функций трансдукторов внутриклеточных сигналов.
Многие ключевые белки, участвующие в передаче митогенных сигналов от «задействованных» интегриновых рецепторов или рецепторов факторов роста, являются продуктами протоонкогенов. Они представляют все уровни митогенной Ras — Raf — МАР-киназной сигнальной цепи: рецепторы факторов роста (например, рецептором эпидермального фактора роста EGF служит продукт протоонкогена ERBB; рецептором так называемого рассеивающего фактора HGF/SF — продукт протоонкогена МЕТ), подмембранная тирозинкиназа Src (продукт протоонкогена SRQ, белки семейства Ras (продукты протоонкогенов K-RAS, H-RAS и N-RAS), цитоплазматические киназы Raf (продукты протоонкогена RAF) и ряд транскрипционных факторов.
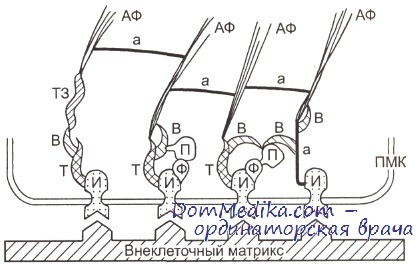
ПМК — плазматическая мембрана клетки; И — интегриновый рецептор; Т — талин; Ф — протеинкиназа фокального контакта; П — паксиллин; В — винкулин; ТЗ — тензин; а — а-актинин; АФ — пучки актиновых микрофиламентов.
В результате мутационного превращения протоонкогенов в онкогены одно или несколько звеньев митогенной сигнальной цепи становятся перманентно сверхактивными. Непрерывная генерация ими сигналов делает постоянно активированными и последующие звенья сигнального пути. Снимается блокировка митогенного сигнала на уровне одной из промежуточных МАР-киназ, и клетки продолжают пролиферировать, даже будучи не прикрепленными к внеклеточному матриксу.
Свой вклад вносит также инактивация (в результате мутации или делеции) гена — опухолевого супрессора KIP1, ингибирующего вхождение клеток в S-фазу цикла.
Следствием всех этих событий является перманентная стимуляция пролиферации клеток, независимая от связывания интегриновых рецепторов с внеклеточным матриксом или от связывания растворимых факторов роста с их рецепторами на поверхности клеток. Трансформированные клетки, таким образом, утрачивают субстратную зависимость размножения и приобретают способность генерировать внутри себя постоянные пролиферативные сигналы, в норме исходящие от внешних стимулов.
Одновременно с этим трансформированные клетки избегают аноикиса. Это достигается в результате инактивации (мутацией или делецией) апоптогенного опухолевого супрессора ТР53 и/или благодаря гиперэкспрессии онкогена RAS в антиапоптогенной сигнальной цепи Ras — Akt.
Таким образом, независимость выживания и размножения опухолевых клеток от их прикрепления к внеклеточному матриксу и от воздействия растворимых факторов роста достигается:
а) перманентной активацией митогенного сигнального пути;
б) отменой блокировки митогенного сигнала при откреплении клеток от матрикса;
в) инактивацией генов — опухолевых супрессоров ТР53 и/или KIP1;
г) гиперэкспрессией онкогена RAS и перманентной активацией антиапоптогенного сигнального пути Ras — Akt.
«Уход» от аноикиса обеспечивает выживание опухолевым клеткам в условиях их циркуляции в лимфо- или кровотоке.
Нарушения в трансдукции внутриклеточных сигналов приводят также к изменениям в регуляции актинового цитоскелета. Проявлением этого является резкий дефицит стресс-фибрилл в трансформированных клетках, что ослабляет центростремительное натяжение и снижает степень распластывания клеток. В результате трансформированные клетки приобретают характерную «поджатую» конфигурацию.
Таким образом, в результате нарушений в формировании фокальных контактов и их функционировании в качестве адгезионных структур и трансдукторов внутриклеточных сигналов трансформированные клетки приобретают характерную морфологию, утрачивают субстратную зависимость размножения, становятся менее зависимыми от растворимых факторов роста и избегают аноикиса. Эти их свойства играют важную роль в прогрессии опухолей, в частности в способности к инвазии и метастазированию.
- Читать "Локомоция клеток - стадии, механизмы"
Оглавление темы "Адгезия клеток":- Микротрубочки - структура, функции
- Стадии распластывания нормальных клеток - механизмы
- Особенности распластывания трансформированных опухолевых клеток - механизмы
- Функции актинового цитоскелета и фокальных контактов нормальных клеток
- Актиновый цитоскелет и фокальные контакты трансформированных опухолевых клеток
- Локомоция клеток - стадии, механизмы
- Особенности локомоции трансформированных опухолевых клеток
- Топографические реакции клеток - виды
- Особенности топографических реакций трансформированных опухолевых клеток
- Адгезионные взаимодействия клеток друг с другом - механизмы
