Цисплатин и карбоплатин - механизм действия препаратов платины
Противоопухолевая активность этого класса соединений была случайно открыта В. Rosenberg при изучении действия электрического поля на рост бактерий.
Платина относится к переходным металлам, т. е. элементам, атомы которых имеют незавершенные внутренние электронные оболочки (в случае платины d-оболочки), вследствие чего они способны образовывать комплексы с различными лигандами (анионами, нейтральными молекулами). Комплексы платины — одни из наиболее прочных комплексных соединений; их пространственное строение зависит от степени окисления платины (II или IV). Комплексы двухвалентной платины Pt(II) имеют плоское строение с атомом платины в центре квадрата, в углах которого располагаются четыре лиганда.
Биоактивные комплексы платины электронейтральны (так называемые комплексы-неэлектролиты), что облегчает их транспорт в клетку. Лиганды в комплексах в зависимости от их способности к замещению подразделяют на два типа: лиганды-носители, которые не замещаются молекулами воды и многими другими лигандами и относительно инертно связаны с платиной, и уходящие лиганды, связанные с платиной лабильно, замещаемые в водных растворах молекулами воды (реакция акватации), вследствие чего образуется связь Pt(II) с биомолекулами.
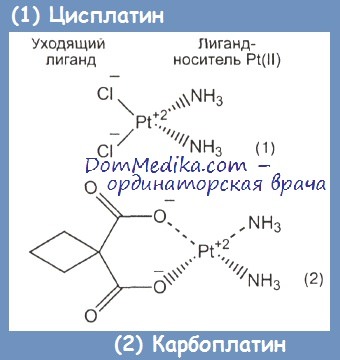
В структуре цисплатина лигандами-носителями являются молекулы аммиака, а уходящими лигандами — анионы хлора.
В онкогематологии применяют два препарата этого класса — производные Pt(II) — цисплатин и карбоплатин.
Цисплатин (син.: DDP, cis Pt(II), Platiblastin, Platinol, платидиам)
Карбоплатин (син. CBDCA)
Цисплатин — первый из препаратов комплексных соединений платины — нашел широкое применение в химиотерапии опухолей. Карбоплатин относят ко второму поколению производных Pt(II), нашедших клиническое применение.
По структуре карбоплатин отличается от цисплатина природой уходящего лиганда — вместо атомов хлора в нем присутствует анион циклобутан-1,1-дикарбоновой кислоты, который связан с платиной через атомы кислорода обеих карбоксильных групп.
Биологическая активность платиновых препаратов тесно связана с их химическими свойствами. Относительно высокая концентрация хлоридионов в цитоплазме препятствует замещению хлора в цисплатине на воду; однако в клеточном ядре, где концентрация хлорида существенно ниже, происходит акватация — постадийное замещение хлоридионов молекулами воды. В результате образуются заряженные аквакомплексы. Например, первая стадия акватации:
cis-[Pt(NH3)2Cl2] + Н2О = cis-[Pt(NH3)2(H2О)Cl]+ + Сl.
Далее происходит встраивание платинового комплекса в ДНК, вода при этом замещается основаниями ДНК, образующими связь с платиной через атомы азота. Расстояние между сшиваемыми платиной N7-смежных гуанинов или гуанина и аденина в одной нити ДНК хорошо соответствует геометрии именно цис-изомера — в обоих случаях это порядка 3,3 А. Инертный шестичленный цикл в карбоплатине практически не способен к акватации. Превращение карбоплатина в соединения, активно реагирующие с ДНК, происходит более интенсивно в клетках, чем в плазме крови, что указывает на участие клеточных эстераз в разрушении дикарбоксилатного лиганда препарата.
Механизм противоопухолевого действия карбоплатина практически тот же, что и у цисплатина, поэтому далее их биологические эффекты будут рассмотрены вместе.
Не выявлено специфических трансмембранных переносчиков для платиновых препаратов, их поступление в клетку происходит в силу химических свойств молекулы. В клетке комплексы платины (II) трансформируются в заряженные аквакомплексы, способные образовать две ковалентные связи платины с двумя нуклеофильными атомами (с повышенной электронной плотностью) биомакромолекул (ДНК, РНК, белков), образуя сшивки между участками макромолекул, где находятся эти атомы. В ДНК связывание платины происходит через атомы азота нуклеиновых оснований, которые могут находиться в одной нити ДНК — внутринитевые сшивки или в разных нитях — межнитевые сшивки (interstrand-linking).
В этом отношении комплексы Pt(II) подобны бифункциональным алкилирующим агентам. Сшивки белок-Pt(II)-ДНК также наблюдаются в клетках, но считается, что эти повреждения играют несущественную роль в противоопухолевом действии этих препаратов.
Лиганды-носители в структуре платиновых аналогов — важный фактор, определяющий индивидуальное для каждого препарата взаимодействие с белками, узнающими платиновые повреждения ДНК, и ДНК-полимеразами. Кроме того, лиганды-носители участвуют в дополнительном связывании с ДНК за счет образования водородных связей атомами водорода при азоте с атомами кислорода ДНК (вероятно, с О6 пуринов, фосфатным кислородом). Образование водородных связей обоими лигандаминосителями является ключевым фактором для наличия цитостатических свойств у комплекса. Уходящий лиганд влияет на реактивность препарата, его токсичность и скорость выведения из организма.
Основной внутриклеточной мишенью, повреждение которой четко коррелирует с гибелью клеток, является ДНК. Благодаря повышенной электронной плотности (высокой нуклеофильности) на атоме азота в положении 7 (N7) гуанина (Г) и аденина (А) цисплатин связывается предпочтительно именно с N7 этих пуриновых оснований, преимущественно гуанина. Цисплатин и карбоплатин формируют примерно одинаковые повреждения в ДНК, но время образования этих повреждений для цисплатина короче, чем для карбоплатина. Основные повреждения ДНК при действии цисплатина выявлены в виде внутринитевых сшивок ДНК (98 %) и только менее 2 % в виде межнитевых сшивок ДНК.
Эти поврежденные участки ДНК узнаются специальными белками, и при высоком уровне дефектов или невозможности их репарации включается механизм апоптоза. Апоптоз может происходить как по зависимому, так и независимому от ТР53 пути, что и объясняет высокую противоопухолевую эффективность цисплатина. Индукция апоптоза в эпителиальных клетках проксимальных почечных канальцев человека, как и повреждение цитоскелета этих клеток, лежит в основе почечной токсичности цисплатина. Интересно, что основные типы сшивок, возникающие при действии препаратов платины (сшивки между смежными парами ГГ и АГ в одной цепи), при встраивании в геном кишечной палочки оказались примерно в равной мере цитотоксичными, но сшивки АГ вызывали на порядок больше мутаций.
Способность клеток к восстановлению поврежденных участков ДНК — важный фактор чувствительности опухолей к цисплатину и карбоплатину. Уменьшение активности или утрата репарирующих ДНК ферментов связаны с заметным увеличением числа клеток, погибших при действии цисплатина. Напротив, усиление активности системы удаления (эксцизии) поврежденных нуклеозидов и дефекты в системе репарации поврежденных участков часто наблюдаются вместе при развитии лекарственной устойчивости.
Идентифицированы и другие механизмы резистентности к платиновым препаратам. Несмотря на то что не были найдены специфические трансмембранные переносчики для этих препаратов, в устойчивых клетках выявлено снижение их внутриклеточной аккумуляции, что может быть следствием ингибирования препаратом различных мембранных белков. Внутри клетки снижение токсических платиновых продуктов происходит путем связывания с глютатионом и другими пептидами и белками, содержащими сульфгидрильные группы. Эти конъюгаты выводятся из клеток с помощью АТФ-зависимых транспортеров, поэтому увеличение внутриклеточного уровня глютатиона часто коррелирует с развитием устойчивости. В некоторых типах клеток мутации ТР53 также связаны с развитием устойчивости к платиновым препаратам.
Недавно установлено, что индукцию апоптоза платиновыми препаратами во многих типах опухолевых клеток можно модулировать некоторыми цитокинами. Например, ИЛ-6 тормозит индуцированный цисплатином апоптоз, а ИЛ-1а и ИЛ-1b усиливают чувствительность клеток к цисплатину. Экспрессия в клетках ИЛ-6 связана с внутриклеточным уровнем глютатиона. Антитела к ИЛ-6 снижают уровень глютатиона и восстанавливают чувствительность лейкозных клеток к цисплатину. Фактор некроза опухолей (ФНО) также несколько повышает чувствительность клеток к цисплатину, но не преодолевает устойчивость к нему.
В клетках лейкоза мышей L 1210 наблюдали перекрестную устойчивость к цисплатину и ФНО. Антитела к Fas-антигену обладают синергизмом с цисплатином в индукции апоптоза. Многие противоопухолевые препараты, блокирующие прохождение клеток через клеточный цикл или повреждающие систему репарации повреждений, могут увеличивать чувствительность клеток к цисплатину, что лежит в основе создания эффективных схем комбинированной химиотерапии. Цисплатин блокирует индуцированный паклитакселем апоптоз. Препараты, содержащие тиосульфатные группы, могут инактивировать платиновые препараты уже в крови. Амифостин инактивирует цисплатин преимущественно в нормальных тканях, не снижая его противоопухолевого эффекта.
Подобно другим ДНК-реактивным агентам, платиновые препараты обладают тератогенными и мутагенными свойствами, что связано с развитием вторичных лейкозов после химиотерапии. Эти препараты также повышают радиочувствительность опухолевых клеток.
Оба препарата выводятся из организма в основном через почки, небольшая часть их (10 %) удаляется с желчью.
- Читать "Антиметаболиты - механизм противоопухолевого действия"
Оглавление темы "Цитостатики":- Цисплатин и карбоплатин - механизм действия препаратов платины
- Антиметаболиты - механизм противоопухолевого действия
- Метотрексат - механизм действия антагонистов фолиевой кислоты
- Цитозин-арабинозид (син.: Ara-C, Arabinosyl cytosine, цитозар, цитарабин, алексан) - механизм действия
- Гемзар (син.: гемцитабин, Gemcitabine hydrochloride) - механизм действия
- 6-меркаптопурин (6-МП) и 6-тиагуанин (6-ТГ) - механизмы действия
- Пентостатин (син.: 2-DCF, Дезоксикоформицин, 2-deoxycoformycin, Co-V, Co-Vidarabine) - механизмы действия
- Кладрибин (син.: 2-CdA, 2-хлордезоксиаденозин, леустатин) - механизм действия
- Флударабин (син.: флудара, Fludarabine phosphate) - механизм действия
- Гидроксимочевина (син.: Hydroxyurea, оксимочевина, гидреа, биосупрессин) - механизм действия
