Острый миелоидный лейкоз (ОМЛ) у детей. Диагностика и лечение
На долю острого миелоидного лейкоза (ОМЛ) приходится 11 % общего числа лейкозов у детей в США; ежегодно регистрируется около 380 новых случаев этого заболевания среди детей. Один из вариантов ОМЛ — острый проми-елоцитарный лейкоз — получил в ряде стран наибольшее распространение, частота других вариантов ОМЛ примерно одинакова. Ряд генетических аномалий характерен для ОМЛ, однако его четкие экзогенные или генетические факторы отсутствуют.
Характерным клиническим признаком острого миелоидного лейкоза (ОМЛ) служит наличие более 30 % бластных клеток с признаками миелоидного ростка кроветворения в стернальном пунктате и мазках-отпечатках биопсийного материала. Наиболее распространенной классификацией ОМЛ служит система FAB. Несмотря на то что указанная классификация учитывает только морфологические критерии клеток, современная диагностика опухоли включает поточную цитофлюометрию для выявления поверхностных антигенов, а также хромосомные и молекулярно-генетические методы исследования.
Симптомы острого миелоидного лейкоза (ОМЛ) по аналогии с острым лимфобластным лейкозом (ОЛЛ) обусловлены замещением костного мозга опухолевыми клетками с последующей недостаточностью костного мозга. Таким образом, для больных с ОМЛ характерны все проявления ОЛЛ, обусловленные подавлением функции костного мозга. Кроме того, ОМЛ имеет собственные клинические признаки: подкожные узелки, симптом «оладьев с черникой» (красные, коричневые или фиолетовые узлы в сочетании с геморрагической сыпью), инфильтрация десен, лабораторные проявления ДВС-синдрома, наиболее характерного для острого промиелоцитарного лейкоза, а также изолированные опухолевидные образования — лейкемиды (хлорома, или гранулоцитарная саркома).
В ряде случаев лейкемиды развиваются и без поражения костного мозга у больных с М2-вариантом острого миелоидного лейкоза (ОМЛ) по классификации FAB или с транслокацией t(8;21).
Диагностика острого миелоидного лейкоза (ОМЛ)
В стернальном пунктате и трепанобиоптате у больных с острым миелоидным лейкозом (ОМЛ) повышено количество клеток костного мозга. С помощью реакции на миелопероксидазу можно выделить некоторые варианты лейкоза, а также подтвердить миелогенное происхождение этих клеток.
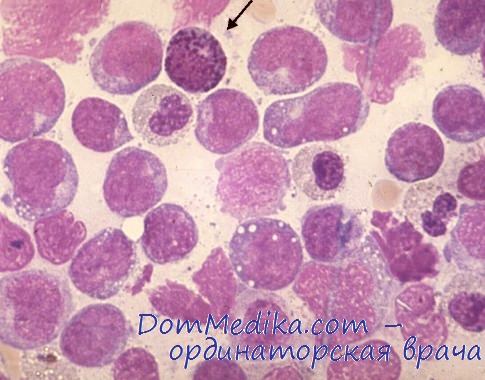
Лечение острого миелоидного лейкоза (ОМЛ)
Высокодозная полихимиотерапия позволяет добиться ремиссии в 80 % случаев. Около 10 % больных ОМЛ погибает от инфекционных осложнений или кровотечения в процессе лечения. Трансплантация красного костного мозга или стволовых клеток крови от близких родственников после завершения полихимиотерапии позволяет добиться длительной безрецидивной выживаемости у 60-70 % детей.
При отсутствии подходящего донора костного мозга эффективность длительной химиотерапии значительно снижается, однако в ряде случаев и она способна привести к излечению больных.
Острый промиелоцитарный лейкоз с перестройкой гена рецептора ретиноевой кислоты высоко чувствителен к комбинированной терапии ретиноевой кислотой и антрациклинами. Данное обстоятельство делает необязательной трансплантацию костного мозга при достижении первой ремиссии.
Поддерживающее лечение острого миелоидного лейкоза (ОМЛ) проводят по тем же принципам, что и ОЛЛ. Длительная высо-кодозная полихимиотерапия способна привести к тяжелому угнетению кроветворения с последующими инфекционными осложнениями.
Синдром Дауна повышает риск развития острого лейкоза в 14 раз. Соотношение числа детей, страдающих ОЛЛ и ОМЛ, среди больных с синдромом Дауна аналогично таковому для основной популяции. Кроме того, эффективность лечения ОЛЛ у детей с синдром Дауна не отличается от таковой у остального контингента соответствующего возраста. К сожалению, указанная генетическая аномалия повышает чувствительность больных к метотрексату и другим антиметаболитам, поэтому доза этих препаратов в процессе полихимиотерапии должна быть снижена. Прогноз больных с ОМЛ и синдромом Дауна значительно лучше по сравнению с лицами без генетических аномалий; безрецидивная выживаемость этих пациентов составила более 80 %.
Кроме того, по завершении первого этапа — индукции ремиссии — поддерживающая химиотерапия требует меньших доз препаратов.
У новорожденных с синдромом Дауна часто развивается транзиторный лейкоз или миелопролиферативный синдром с лейкоцитозом, властными клетками в периферической крови, а также анемией, тромбоцитопенией и гепатоспленомегалией. Эти клинические признаки самостоятельно разрешаются через несколько дней или недель. В ряде случаев новорожденным с миелопролиферативным синдромом назначают трансфузию препаратов крови, однако химиотерапия им не показана. Вместе с тем указанная категория новорожденных требует систематического наблюдения врача, поскольку у 20-30 % лиц в течение первых нескольких лет жизни развивается типичный острый лейкоз.
- Вернуться в раздел "онкология"
Оглавление темы "Опухоли детей":- Диагностика опухолей у детей. Клиника рака у ребенка
- Гистология опухоли у детей. Беседа с родителями больного раком ребенка
- Принципы лечения опухолей у детей. Терапия детского рака
- Химиотерапия у детей. Принципы
- Хирургическое лечение опухолей у детей. Лучевая терапия
- Побочные эффекты лечения опухолей у детей: ранние и поздние
- Острый лимфобластный лейкоз (ОЛЛ) у детей. Причины
- Диагностика острого лимфобластного лейкоза у детей. Дифференциация
- Лечение острого лимфобластного лейкоза у детей. Прогноз
- Острый миелоидный лейкоз (ОМЛ) у детей. Диагностика и лечение
