Методы лечения рака влиянием на теломеры и теломеразу
Иммунотерапия. Поскольку теломераза присутствует в большинстве опухолевых клеток, она является хорошим кандидатом на роль антигена, ассоциированного с опухолями. При функционировании теломеразы в клетке фрагменты теломеразной обратной транскриптазы экспонируются на поверхности клетки и могут служить мишенью для иммунного ответа. Возможно усиление иммунного ответа, если фрагменты белка hTERT будут появляться на поверхности антигенпредставляющих клеток (АПК) пациента, прежде всего на дендритических клетках и макрофагах. Для этого белок, мРНК или соответствующую ДНК вводят в выделенные АПК ex vivo.
Установлен ряд пептидов (фрагменты белка hTERT), которые связываются с антигенами главного комплекса гистосовместимости 1-го класса (HLA-A2.1), представленными на поверхности значительной доли лимфоцитов, в результате чего происходит специфическое усиление иммунных реакций против антигенного пептида. В модельных системах наблюдали выраженное цитотоксическое действие. Потенциальным достоинством такой процедуры является отсутствие длительного периода ожидания в отличие от методик подавления теломеразы. Пока недостаточно данных об эффективности и специфичности подобной процедуры. Кроме того, неясно, насколько значительными могут быть повреждения здоровых стволовых клеток, которые также обладают теломеразной активностью.
Использование промоторов теломеразы (hTERT и hTR). Пока не найдены препараты, способные эффективно подавлять экспрессию генов теломеразы, однако разработаны подходы к лечению, при которых используется сам факт активной работы промоторов теломеразы в опухолевых клетках.
Конструкция, включающая промотор hTERT и ген тимидинкиназы вируса герпеса простого, специфически повышает чувствительность опухолевых клеток к ганцикловиру. Конструкция, содержащая ген бактериальной нитроредуктазы под промотором hTERT, активирует соединение СВ1954, которое становится токсичным.
Разработаны конструкции, селективно вызывающие апоптоз: промотор hTERT + ген, кодирующий Вах, промотор hTERT+ген каспазы-8, промотор hTERT+ген каспазы-6, промотор hTERT+ ген, кодирующий домен смерти, ассоциированный с FAS.
Опробована система, экспрессирующая ген дифтерийного токсина А под промоторами hTR и hTERT. Сделана попытка проведения селективной радиационной терапии. После введения в клетки злокачественной глиомы гена — транспортера норадреналина под промотором hTR, злокачественные клетки стали избирательно накапливать радиоактивный метайодбензилгуанидин [(l3lI) MIBG] и погибать от радиационного повреждения.
Достоинством методов, в которых используют активность промотора hTERT, является отсутствие длительного периода ожидания в отличие от различных методик подавления теломеразы. Однако активности промоторов hTERT в популяции опухолевых клеток сильно различаются, что снижает эффективность всей процедуры.
Быстрый запуск репликативного старения. Существуют опухолевые клетки, в которых механизмы репликативного старения сохранены, но не функционируют из-за наличия разнообразных онкогенов. Блокирование этих онкогенов должно привести к индукции пролиферативного старения, так как обычно опухолевые клетки имеют сильно укороченные теломеры. Большинство карцином шейки матки человека экспрессируют белки Е6 и Е7 вируса папилломы человека. Установлено, что инфицирование этих клеток рекомбинантным вирусом, экспрессирующим белок Е2 вируса папилломы быка, подавляет экспрессию Е6 и Е7. Через 12 ч отмечаются подавление синтеза ДНК, индукция ТР53, mdm2, р21, р105, р107 и р130, развивается типичная картина клеточного старения.
Методы подавления теломеразы. Все методы подавления теломеразы имеют один очень серьезный недостаток: эффект наступает с большой задержкой, поскольку должно пройти достаточно времени для того, чтобы в отсутствие теломеразы длина теломер уменьшилась в результате недорепликации. Это время может составлять десятки клеточных циклов.
Модифицированные нуклеозиды и нуклеотиды. Поскольку теломераза относится к обратным транскриптазам и характеризуется низкой требовательностью к субстратам (сравнительно с другими клеточными полимеразами), возможно применение различных модифицированных нуклеозидов с целью прекратить теломеразный синтез. Наиболее известны попытки подавить функцию теломеразы с помощью азидотимидина. Существуют достаточно эффективные модифицированные нуклеозидтрифосфаты, способные в наномолярных концентрациях (в экстракте) подавлять теломеразу. Однако такие соединения с трудом проникают в клетки и быстро гидролизуются. Основной проблемой является токсичность нуклеозидов, прежде всего по отношению к митохондриальной полимеразе.
Ненуклеотидные мелкие молекулы — ингибиторы теломеразы. Наиболее активным соединением, подавляющим теломеразу, является теломестатин, выделенный из Streptomyces anulatus. Он подавляет теломеразную активность в концентрации 5 нМ. Возможно, механизм его действия состоит в стабилизации квадруплексов (G4). Однако теломестатин подавляет также разнообразные обратные транскриптазы, не связанные с 04-структурами. Стоит отметить другое, недавно полученное соединение — BIBR 1532, которое обладает более выраженной специфичностью и активно в концентрациях ниже 100 нМ. BIBR 1532 активен на клетках и нетоксичен. Это вероятный кандидат для внедрения в клиническую практику. В 2004 г. показано, что BIBR 1532 не снижает пролиферативный потенциал гемопоэтических стволовых клеток в культуре.
Антисмысловые стратегии. Антисмысловые стратегии основаны на взаимном узнавании (гибридизации) нуклеиновых кислот внутри клетки. Вводимые антисмысловые последовательности соединяются со смысловыми (необходимыми для функционирования теломеразы) и блокируют их.
Первыми были проведены опыты по введению в клетки гена, кодирующего антисмысловую последовательность, к РНК-компоненту теломеразы. Однако даже при работе с малыми количествами клеток в культуре часто возникают их резистентные формы.
Более эффективным может быть введение в клетки олигонуклеотидов, комплементарных РНК-компоненту теломеразы. Обычно применяют олигонуклеотиды, направленные против матричного района теломеразной РНК; используют также олигонуклеотиды с фосфоротиоатными связями (для увеличения устойчивости к нуклеазам), пептидные нуклеиновые кислоты (для увеличение стабильности гибрида), 2'-0-метил-РНК и 2'-метоксиэтокси-РНК. Эти соединения характеризуются повышенной устойчивостью к нуклеазам и специфичностью. Главное в разработке таких соединений — уменьшить размер молекулы, с тем чтобы она могла легче проникнуть в клетки, сохранив при этом достаточно сильное и специфическое связывание с мишенью.
Антисмысловые олигонуклеотиды можно использовать для специфического разрушения РНК-компонента теломеразы путем активации эндогенных эндорибонуклеаз. Принцип метода состоит в следующем. В клетки вводят олигодезоксирибонуклеотид с присоединенной к 5'-концу 2'-, 5'-олигоаденилатной (3-4 аденозина) группой. После «узнавания» олигонуклеотидом своей мишени 2'-, 5'-олигоаденилат активирует эндогенные эндорибонуклеазы — РНКазу L и РНКазу Н, которые атакуют одноцепочечную РНК-мишень.
В экспериментах с культурами клеток проводили трансфекции олигонуклеотидов каждые 24 ч в течение нескольких дней и добивались того, что большинство опухолевых клеток погибало, однако с каждым днем эффективность процедуры снижалась. Эффективность повышалась при комбинировании введения 2'-, 5'-А-олигонуклеотидов с другими методами: лечением цисплатином и введением гена белка ТР53 дикого типа (в случаях изменения собственного ТР53).
Олигонуклеотид может быть соединен с рибозимом (РНК-ферментом), обладающим эндорибонуклеазной активностью (так называемый молоткоголовый рибозим). После присоединения к мишени рибозим разрушает ее. В экспериментах с конструкциями, направленными против различных районов мРНК hTERT и теломеразной РНК, изначально наблюдали укорочение теломер и некоторое замедление роста клеток, но их гибели не отмечали.
В последние несколько лет широко распространился метод специфического разрушения матричных РНК с помощью явления интерференции РНК. Короткие (21—25 нуклеотидов) двуцепочеч-ные РНК (siRNA), несущие на З'-конце 2 неспаренных нуклеотида, вызывают в клетке образование сложного комплекса, в котором происходит разворачивание двуцепочечной РНК. После этого комплекс в состоянии специфично узнавать РНК-мишень и вызывать ее деградацию с помощью входящей в комплекс эндогенной рибонуклеазы.
siRNA могут образовываться различными путями: их можно синтезировать химически или с помощью транскрипции in vitro, они могут возникать в клетке из более длинных двуцепочечных РНК после их разрезания эндогенным ферментом Dicer (разновидность РНКазы III). Наконец, клетки можно трансфицировать ДНК-векторами, кодирующими либо непосредственно siRNA, либо короткие шпилечные РНК (shRNA), которые затем превращаются в siRNA. Подавление теломеразы с помощью siRNA вызывает потерю теломеразной активности, укорочение теломер, остановку пролиферации и массовый апоптоз в клетках аденокарциномы.
Олигонуклеотидные стратегии являются самыми специфичными и малотоксичными. Основной проблемой является доставка олигонуклеотидов в клетки.
Перспективный метод введения «самотрансфицирующегося» олигонуклеотида появился в 2005 г. Тиофосфороамидатный 13-членник, направленный против теломеразной матрицы, конъюгировали с остатком пальмитиновой кислоты. Соединение оказалось способным достаточно эффективно проникать в разнообразные клетки тела мыши при внутриперитонеальном введении и подавлять метастазирование.
Блокирование сборки теломеразы. Введение гена доминантно-негативного мутанта теломеразной обратной транскриптазы в экспериментах является наиболее эффективным способом подавления теломеразы.
При введении такого гена его продукт конкурирует за теломеразную РНК с нормальным геном. В результате происходит сборка дефектной теломеразы, что ведет к подавлению теломеразной активности, укорочению теломер и индукции апоптоза.
Воздействие на теломеры. Препараты, стабилизирующие квадруплексы. До сих пор нет прямых свидетельств существования квадруплексов in vivo, однако разнообразные соединения, взаимодействующие с квадруплексами in vitro, подавляют теломеразную активность, в том числе в клетках. Установлено, что имеется корреляция между способностью вещества вызывать термальную стабилизацию С4-структур и подавлять теломеразную активность. Флюоресцентные пробы на G-4-структуры могут служить ингибиторами теломеразы. Разработаны G-4-лиганды, подавляющие теломеразную активность в концентрациях порядка 10 нМ.
Помимо веществ, вызывающих стабилизацию G-4-структур, разработаны соединения, избирательно повреждающие ДНК на границе с G-4-структурами. Комбинация олигонуклеотида 5'-(GGGTTA)4 с металлопорфирином вызывает окислительное повреждение на границе G-4-структур. Недостатком соединений, стабилизирующих квадруплексы, является их токсичность. Они воздействуют на разнообразные процессы, помимо подавления теломеразы.
- Читать "Теломеризация клеток - не ведет к злокачественной трансформации"
Оглавление темы "Онкогенез":- Метилирование генов-супрессоров как причина гемобластозов - опухолей крови
- Теломераза - синтез, функции
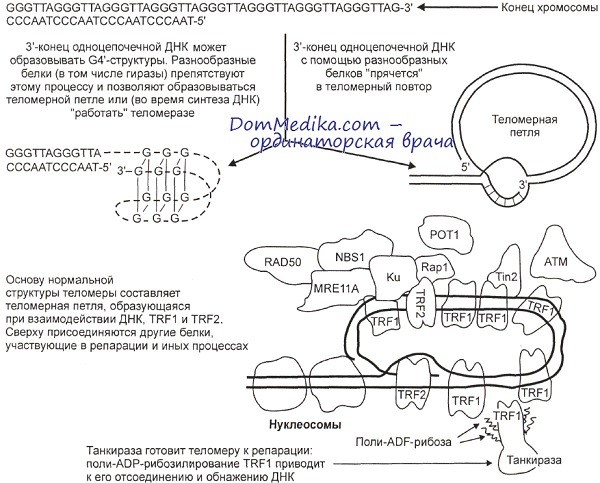
- Теломера - молекулярная структура
- Что такое теломерный эффект положения?
- Альтернативные способы удлинения теломер у человека - иммортализация
- Значение теломеразы в диагностике опухолей
- Методы лечения рака влиянием на теломеры и теломеразу
- Теломеризация клеток - не ведет к злокачественной трансформации
- Адгезия клеток - последствия нарушения адгезивных взаимодействий
- Актиновые микрофиламенты - структура, функции
