Классический путь активации комплемента. Элементы классического пути активации комплемента
Инициация процесса связана с образованием комплекса антиген-антитело. Только два класса антител: IgG и IgM—обеспечивают активацию благодаря наличию в их молекулах эффекторных центров для Clq — первого субкомпонента первого компонента системы.
Прежде чем перейти к детальному рассмотрению вопроса о механизме активации комплемента с участием комплекса антиген-антитело, представляется целесообразным изложить в схематической форме современные взгляды на процесс активации комплемента по классическому пути в хорошо изученной системе: эритроцит — IgG-антитело кролика.
Согласно схеме первоначально к комплексу антиген (S)-антитело (А) присоединяется комплекс С1, состоящий из трех компонентов: Clq, Clr, Cls. В результате образуется фермент — Cl-эстераза (Cls). Под действием Cl-эстеразы возникает энзиматически активный комплекс четвертого и второго компонентов комплемента (С4, 2), обозначаемый также как С3-конвертаза. Этот фермент расщепляет третий компонент комплемента— С3 на два фрагмента: С3а, обладающий свойствами анафилатоксина (см. ниже) и хемотактической активностью, и С3b, способный взаимодействовать с С4,2.
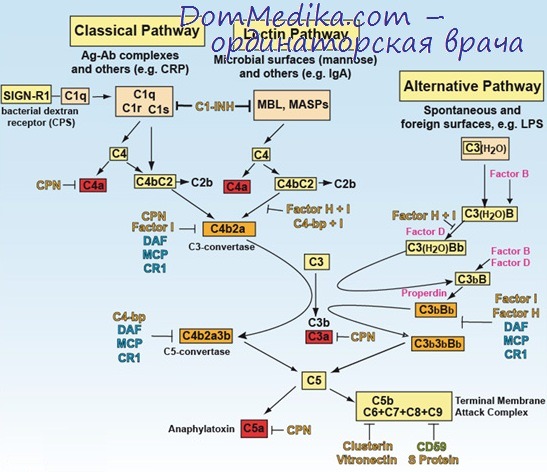
В результате образуется фермент с активностью пептидазы, действующий на С5. Комплекс С4, 2,3, находящийся на поверхности клетки, обеспечивает фиксацию на клеточной мембране активированного пятого компонента комплемента, а затем С6 и С7. Эти три компонента, действующие как одна функциональная единица, способствуют фиксации С8 и С9. После присоединения первого из них эритроцит становится высокочувствительным к осмотическому лизису. Действие С8 усиливает С9, вызывающий необратимые повреждения структуры мембраны.
Головной компонент классического пути активации — Clq представляет собой один из интереснейших по строению белков. Он имеет молекулярную массу 400 000 и образован 18 полипептидными цепями. В каждой цепи около 200 аминокислотных остатков, но первичная структура их хотя и сходна, но не идентична. Их можно разделить на три типа: А, В и С. Аминоконцевые половины каждой из цепей подобны по структуре коллагену, так как образованы повторяющимися аминокислотными триплетами X—У—Gly.
Лишь короткий отрезок цепи непосредственно в районе аминоконцевого остатка не имеет подобной структуры. С-концевая часть каждой цепи (103—108 остатков) имеет третичную структуру, характерную для глобулярного белка. По данным электронной микроскопии, все полипептидные цепи сформированы в шесть субъединиц, причем вся молекула напоминает по внешнему виду тюльпан. Шесть лепестков (или головок) образованы С-концевыми глобулярными областями цепей, а коллагеноподобные участки скручены в каждой субъединнце в трехспиральную структуру. Все вместе они образуют структуру, подобно стеблю (stulk), будучи объединены непосредственно в районе аминоконцевого участка межцепьевымн дисульфидными связями.
- Читать "Взаимодействие комплемента с иммуноглобулинами. Активация С4 с помощью С1"
Оглавление темы "Активация комплемента иммунной системы":1. Продукты распада иммуноглобулинов и воспаление. Влияние фрагментов иммуноглобулинов на воспаление
2. Комплемент. Химия комплемента
3. Классический путь активации комплемента. Элементы классического пути активации комплемента
4. Взаимодействие комплемента с иммуноглобулинами. Активация С4 с помощью С1
5. Активация С2 иммуноглобулина. Мембранатакующий комплекс
6. Альтернативный путь активации комплемента. Пропердин
7. Фактор В при активации комплемента. Механизм инициации альтернативного пути активации комплемента
8. Факторы альтернативной активации комплемента. Регуляторные белки системы комплемента
9. Бета-1-Н белок активации комплемента. Биологически активные пептиды
10. Эффекторные функции системы комплемента. Иммунное прикрепление
