Симптомы сахарного диабета
Сложно кратко описать разнообразные клинические проявления СД. Обсудим только наиболее характерные его признаки. Раньше считали, что СД типа I развивается преимущественно у пациентов в возрасте до 18 лет, но в настоящее время известно, что СД типа I может развиться в любом возрасте. В течение первых двух лет после развития явного СД типа I потребность в экзогенном инсулине может быть минимальной благодаря продолжающейся секреции эндогенного инсулина.
После этого резервные возможности b-клеток истощаются, и потребность в инсулине резко возрастает. Несмотря на то что разрушение b-клеток — длительный процесс, переход от нарушения толерантности к глюкозе к явному СД может быть внезапным. Часто его провоцируют различные состояния, например инфекции, которые также сопровождаются увеличением потребности в инсулине.
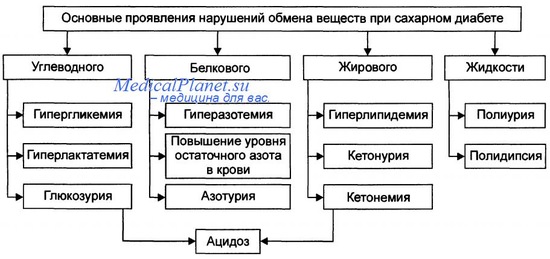
Начало явного СД определяют по наличию таких признаков, как полиурия, полидипсия, полифагия, а в тяжелых случаях — кетоацидоз, возникающий в результате нарушения обмена веществ. Поскольку инсулин является главным анаболическим гормоном, его дефицит приводит к катаболическому состоянию, которое затрагивает не только обмен глюкозы, но и метаболизм жиров и белков. В этих метаболических нарушениях определенную роль также играет относительное повышение секреции противоинсулярных гормонов (глюкагона, гормона роста, адреналина).
Усвоение глюкозы мышцами и жировой тканью резко снижается или вообще отсутствует. В печени и мышцах не только прекращается накопление гликогена, но и истощаются его запасы вследствие гликогенолиза. Возникающая в результате этих процессов гипергликемия повышает порог реабсорбции глюкозы почками, что приводит к глюкозурии. Глюкозурия индуцирует осмотический диурез и полиурию, которая, в свою очередь, приводит к избыточной потере жидкости и электролитов. Потеря жидкости в сочетании с гиперосмолярностью, возникающей в результате повышения уровня глюкозы в крови, истощает внутриклеточные запасы воды, что стимулирует осморецепторы центра жажды в головном мозге, и развивается сильная жажда (полидипсия).
Из-за недостатка инсулина обмен сдвигается от инсулин-опосредованного анаболизма к катаболизму белков и жиров. Происходит протеолиз, а аминокислоты, образовавшиеся в результате глюконеогенеза, печень утилизирует и использует в качестве блокаторов глюкозы. Катаболизм белков и жиров приводит к отрицательному энергетическому балансу, что повышает аппетит (полифагия). Так формируется классическая диабетическая триада: полиурия, полидипсия и полифагия. Несмотря на повышенный аппетит, преобладающий катаболизм приводит к снижению массы тела и мышечной слабости. Сочетание полифагии и снижения массы тела является парадоксальным состоянием, при котором практически всегда следует заподозрить СД.

а) Диабетический кетоацидоз — серьезное осложнение СД типа I, которое может развиваться и при СД типа II, хотя и не так часто и в менее выраженной форме. У пациентов с этим осложнением отмечается значительный дефицит инсулина, а секретируемый адреналин блокирует все эффекты инсулина и стимулирует секрецию глюкагона. Дефицит инсулина в сочетании с избытком глюкагона приводят к снижению утилизации глюкозы периферическими тканями, а глюконеогенез усиливается, тем самым усугубляя гипергликемию (уровень глюкозы в плазме крови обычно колеблется от 500 до 700 мг/дл).
Гипергликемия вызывает осмотический диурез и дегидратацию, характерные для кетоацидоза. Вторым эффектом нарушения соотношения инсулин/ глюкагон является активация кетоногенных механизмов. Дефицит инсулина стимулирует липопротеинлипазу, что приводит к нарушению отложения жиров и увеличению уровня свободных жирных кислот. Когда свободные жирные кислоты достигают печени, они эстерифицируются с образованием комплекса «жирная кислота-ацетил-коэнзим А». В результате окисления этого комплекса в митохондриях гепатоцитов образуются кетоновые тела (ацетоуксусная кислота и b-гидроксимасляная кислота). Скорость, с которой кетоновые тела образуются, может превышать скорость их утилизации периферическими тканями, что приводит к кетонемии и кетонурии.
Если дегидратация нарушает выделение кетонов с мочой, развивается системный метаболический кетоацидоз. Высвобождение кетогенных аминокислот при катаболизме белков усугубляет это состояние.
СД типа II также может проявляться полиурией и полидипсией, но в отличие от СД типа I наблюдается обычно у лиц старше 40 лет, страдающих ожирением. Однако в настоящее время в связи с широкой распространенностью ожирения и малоподвижного образа жизни СД типа II все чаще выявляют у детей и подростков. В некоторых случаях пациенты обращаются за медицинской помощью из-за необъяснимой слабости или снижения массы тела. Однако чаще диагноз ставят после рутинного исследования крови или мочи у пациентов без каких-либо симптомов. Редкость развития кетоацидоза и умеренно выраженные другие клинические проявления при СД типа II, вероятно, обусловлены более высоким уровнем инсулина по сравнению с больными СД типа I, что препятствует неконтролируемому окислению жирных кислот и ограничивает процесс образования кетоновых тел.
При декомпенсации у таких пациентов может развиться гиперосмолярная некетоиовая кома вследствие тяжелой дегидратации, возникающей в результате постоянного осмотического диуреза (особенно у пациентов, не получающих достаточного количества воды для компенсации ее потерь из-за хронической гипергликемии). Обычно такими пациентами являются пожилые люди, которые из-за инсульта или инфекции не способны употреблять адекватное количество воды. Кроме того, отсутствие кетоацидоза и его симптомов (тошноты, рвоты, нарушения дыхания) не позволяет вовремя диагностировать СД вплоть до тяжелой дегидратации и комы. В табл. 24.7 перечислены некоторые клинические, генетические и морфологические признаки, позволяющие отличить СД типа I от СД типа II.
При обоих типах СД возможны отдаленные осложнения, которые приводят, помимо острых метаболических состояний, к инвалидизации и существенно повышают смертность от заболевания. В большинстве наблюдений такие осложнения развиваются через 15-20 лет с момента появления гипергликемии.
б) Осложнения, обусловленные макроангиопатией, например инфаркт миокарда, почечная недостаточность сосудистого генеза и инсульт, являются самыми частыми причинами смерти при длительном СД. Среди лиц, страдающих СД, поражение коронарных артерий наблюдается в 2-4 раза чаще, а риск летального исхода от сердечно-сосудистых осложнений выше в 4 раза по сравнению с лицами без СД. СД часто сопутствуют заболевания, которые способствуют развитию осложнений со стороны сердечно-сосудистой системы. Так, 75% лиц с СД типа II имеют артериальную гипертензию, которая усиливает влияние гипергликемии и инсулинорезистентности на эндотелиальную дисфункцию и атеросклероз. Другим фактором риска развития сердечно-сосудистых заболеваний у лиц с СД является дислипидемия, которая характеризуется увеличением уровня триглицеридов и липопротеинов низкой плотности и снижением уровня «хороших» липопротеинов высокой плотности.
Считается, что инсулинорезистентность также способствует развитию диабетической дислипидемии за счет увеличения синтеза в печени атерогенных липопротеинов и подавления захвата циркулирующих липидов периферическими тканями. Кроме того, у пациентов с СД повышен уровень ингибитора активатора плазминогена типа 1, который является ингибитором фибринолиза и действует как прокоагулянт при формировании атеросклеротических бляшек.
в) Диабетическая нефропатия — главная причина терминальной стадии почечной недостаточности в США. Клинические проявления диабетической нефропатии наблюдаются у 30-40% пациентов с СД, однако лишь у небольшого количества пациентов с СД типа II диабетическая нефропатия прогрессирует до терминальной стадии почечной недостаточности. В связи с тем что СД типа II является очень распространенным заболеванием, пациенты с диабетической нефропатией составляют более 50% всех лиц с СД, которым начинают проводить гемодиализ. На частоту диабетической нефропатии в США большое влияние оказывает принадлежность к определенной популяции. Например, коренные жители США, представители негроидной расы и испаноязычной этнической группы имеют более высокий риск развития терминальной стадии почечной недостаточности по сравнению с лицами с белым цветом кожи, страдающими СД типа II.
Самый ранний признак диабетической нефропатии — появление в моче небольшого количества альбумина (> 30 мг/сут, но < 300 мг/сут), т.е. микроальбуминурия. Важно отметить, что микроальбуминурия у пациента с СД типа I или II также является маркером развития у него сердечно-сосудистого заболевания, поэтому всех пациентов с микроальбуминурией необходимо обследовать на наличие у них макроангиопатии и по результатам назначить необходимое лечение. Без специфической терапии у « 80% пациентов с СД типа I и у 20-40% пациентов с СД типа II через 10-15 лет разовьется выраженная нефропатия с макроальбуминурией (> 300 мг/сут), обычно сопровождающаяся гипертензией. Длительность прогрессирования заболевания от выраженной нефропатии до терминальной стадии почечной недостаточности значительно варьирует.
В течение 20 лет у > 75% лиц с СД типа I и у 20% лиц с СД типа II с выраженной диабетической нефропатией разовьется терминальная стадия почечной недостаточности и понадобится гемодиализ или трансплантация почек.
Нарушения зрения, иногда в виде полной слепоты, — одно из наиболее страшных для пациента отдаленных последствий СД. В течение 15-20 лет с момента постановки диагноза «сахарный диабет» у 60-80% пациентов развивается та или иная форма диабетической ретинопатии. Основное патологическое изменение при диабетической ретинопатии — образование новых сосудов (неоваскуляризация), которое является следствием гиперэкспрессии VEGF в сетчатке, индуцированной гипоксией. Современное лечение этого состояния подразумевает интравитреальное (внутрь стекловидного тела) введение антиангиогенных препаратов. Диабетическая ретинопатия представляет собой совокупность изменений, по которым офтальмолог диагностирует это заболевание. Лица с СД имеют предрасположенность к развитию глаукомы и катаракты, которые также способствуют нарушению зрения при СД.
г) Диабетическая нейропатия, вызывающая разнообразные клинические синдромы, поражает структуры ЦНС, периферические сенсомоторные нервы и вегетативную нервную систему. Самое частое проявление — дистальная симметричная полинейропатия нижних конечностей, которая характеризуется нарушением двигательной функции и чувствительной функции (чаще). Со временем в процесс могут вовлекаться и верхние конечности с развитием характерной полинейропатии по типу «перчаток и носков». Другие формы диабетической нейропатии — вегетативная нейропатия, которая приводит к нарушениям функции кишечника, мочевого пузыря и даже к импотенции, и диабетическая мононейропатия, которая может проявиться внезапным синдромом свисающей стопы или свисающей кисти либо изолированными параличами черепных нервов.
Лица, страдающие СД, имеют высокую предрасположенность к развитию инфекционных заболеваний кожи, а также туберкулезу, пневмонии и пиелонефриту. Все эти инфекции в совокупности являются причиной смерти 5% лиц с СД. У пациентов с диабетической нейропатией незначительная инфекция пальца стопы может стать первым звеном длинной цепи осложнений (гангрена, бактериемия, пневмония), которые в конечном итоге и приведут к смерти. Высокая предрасположенность к развитию перечисленных осложнений обусловлена множеством факторов, включая снижение функциональной активности нейтрофилов (хемотаксиса, адгезии к эндотелию, фагоцитоза и бактерицидной активности) и нарушением продукции цитокинов макрофагами. Поражения сосудов снижают поступление к очагу воспаления циркулирующих клеток и молекул, необходимых для обеспечения иммунной защиты.
В последние годы малоподвижный образ жизни и особенности пищевого поведения все больше способствуют широкому распространению во всем мире СД и ожирения. В настоящее время СД и ожирение наблюдаются даже у детей из-за употребления ими так называемой «мусорной» пищи и отсутствия адекватной физической нагрузки. Термин «метаболический синдром» (ранее этот синдром называли синдромом X) используют для обозначения состояний, когда абдоминальный тип ожирения и инсулинорезистентность сочетаются с факторами риска развития сердечно-сосудистых заболеваний, например с нарушением липидного профиля. Пациентам с метаболическим синдромом необходимо изменить свой образ жизни, в т.ч. диету, и снизить массу тела. Те же рекомендации актуальны для лиц с выраженным СД типа II. В США в связи со снижением количества инфекционных заболеваний и увеличением общей продолжительности жизни СД становится главной проблемой здравоохранения и остается одним из 10 так называемых болезней-«убийц».
American Diabetes Association установила, что в США суммарные издержки при СД составляют 132 млрд долларов ежегодно, включая 92 млрд долларов прямых медицинских затрат и 40 млрд долларов непрямых затрат, например вследствие нетрудоспособности, потери работы и преждевременной смерти. Остается надяться, что роль первичной профилактики СД типа II путем изменения образа жизни и характера питания, а также профилактики развития диабетических осложнений с помощью строгого гликемического контроля будет постоянно возрастать. Кроме того, разработка методов лечения стволовыми клетками и иммуномодуляторами, а также трансплантация клеток островков Лангерганса помогут в лечении пациентов с СД типа I.
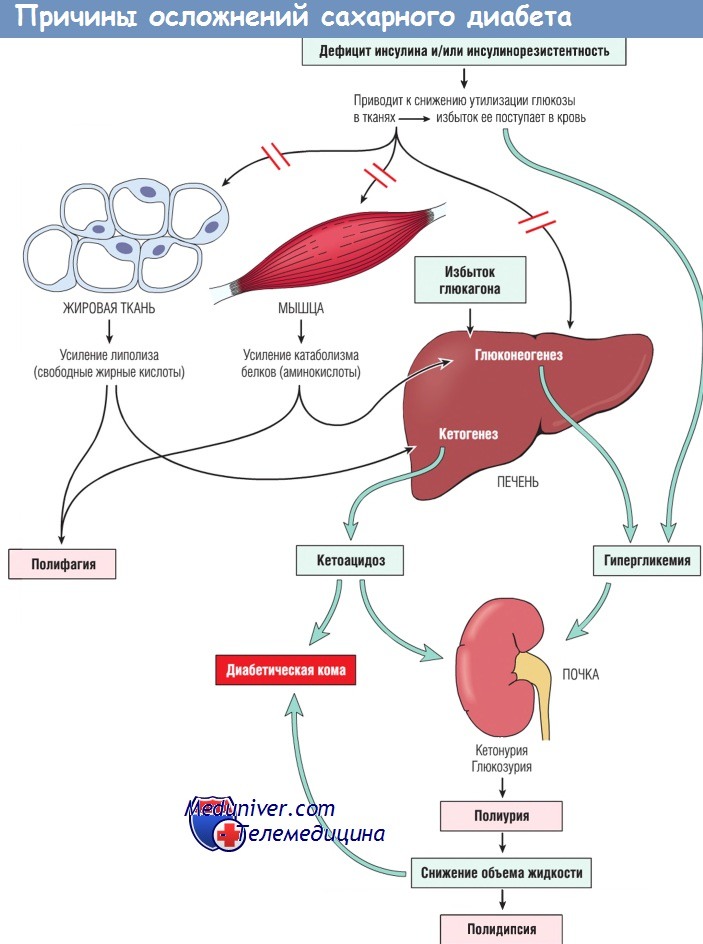
Абсолютный дефицит инсулина приводит к развитию катаболического состояния, кульминацией которого являются кетоацидоз и тяжелое обезвоживание.
Это приводит к нарушению функций ЦНС (коме, а при отсутствии лечения — к летальному исходу).
- Читать "Классификация эндокринных опухолей поджелудочной железы"
Оглавление темы "Патогенез эндокринных болезней":- Причины и механизмы развития осложнений сахарного диабета
- Морфология осложнений сахарного диабета
- Симптомы сахарного диабета
- Классификация эндокринных опухолей поджелудочной железы
- Причины и механизмы развития гиперинсулинизма (избытка инсулина)
- Причины и механизмы развития синдрома Золлингера-Эллисона
- Строение и функции надпочечников
- Причины и механизмы развития гиперфункции коры надпочечников - гиперкортицизма
- Причины и механизмы развития гиперальдостеронизма
- Причины и механизмы развития адреногенитального синдрома
