Патогенез лимфоцитарного хориоменингита (ЛХМ)
Патогенетические особенности различных форм лимфоцитарного хориоменингита зависят от ряда факторов: штамма вируса, возраста животного, способа заражения и дозы вируса. Именно поэтому мы рассмотрим изменения в организме зараженных взрослых и новорожденных мышей, на которых проводились исследования (Cole, Nathanson).
Инфекция у взрослых мышей
В результате внутримозгового введения высоких доз вируса через 5 дней у животных развивается заболевание, характеризующееся описанными выше признаками острого лимфоцитарного хориоменингита и завершающееся к 6— 8-му дню их гибелью. За 2 сут до гибели в сосудистом сплетении, эпендиме и мягких мозговых оболочках нарастает количество воспалительного экссудата, содержащего лимфоциты и моноциты.
Эти события сопровождаются начинающимся с первого дня увеличением в мозговой ткани титра вируса, достигающего к 4-му дню максимума на уровне 107 ЛД50/г. С помощью МФА установлено, что заражение ограничено лишь певральными мембранами (Cole е. а., Gilden е. а.).
Изучение патогенеза лимфоцитарного хориоменингита у крыс подтвердило основные закономерности, полученные в многочисленных опытах на мышах. У крыс внутримозговое введение вируса приводило к различной степени поражения вещества головного мозга в зависимости от использованного штамма и от возраста заражаемых животных.
В мозге взрослых крыс максимальное накопление вируса наступало на 5-й день и достигало 108ЛД50/г (Lohler е. а.).
Наиболее выраженным симптомом поражения мозга вирусом являлась гипоплазия мозжечка. Вирус поражал в первую очередь активно пролиферирующие участки мозговой ткани. Морфологическим отражением развивающихся патологических процессов служила также мононуклеарная инфильтрация ткани мозжечка. Эту инфильтрацию можно рассматривать как показатель иммунологической атаки. Введение лимфоидных клеток от иммунных к вирусу сингенных животных вызывало поражение мозжечка даже у тех крыс, которым вирус вводили уже в период возрастного приобретения резистентности (Моnjan е. а.).
Совершенно иную картину наблюдают при внутрибрюшин-ном введении вируса лимфоцитарного хориоменингита в организм мышей. После такого заражения развивается ограниченный патологический процесс, характеризующийся минимальными титрами вируса в крови, низким уровнем его репродукции в ретикулоэндотелиальной ткани, почках и печени, не затрагивающим центральной нервпой системы (Cole, Nathanson, 1974).
Инфекция у новорожденных мышей
Уже 40 лет назад было установлено, что зараженные вскоре после рождения мыши становятся вирусоносителями, и в колониях таких животных осуществляется вертикальная передача вируса (Traub).
Специальное изучение процента смертности в зависимости от возраста заражаемых мышей было проведепо Hotchin, который показал, что в наибольшей степени эта зависимость выражена до первых 14 дней жизни животного. Так, если заражение однодневных мышей вызывает 10% гибели от лимфоцитарного хориоменингита, то заражение трехдневных — уже около 30 %, 6-дневных — около 40% и 7-дневных — около 60%. В более поздние сроки эта зависимость выражена менее резко: заражение 2-недельных животных вызывает 70% гибель, 3-недельных — 85%, 5-недельных — 95% и 10-недельных — 100%.
На основании полученных данных Hotchin предложил метод экспериментального получения вирусоиосителой путем заражения новорожденных мышей (если это однодневные животные, то процент вирусоносителей теоретически соответствует 90).
Долгое время считали, что персистешщя вируса протекает благоприятно и не наносит ущерба персистентно инфицированному организму в силу сложившегося в этом случае «совершенного паразитизма» (Traub). Только сравнительно недавно было обнаружено, что столь долгое время казавшаяся благополучной бессимптомная инфекция сопровождается рядом патологических состояний.
Так, с помощью МФА удалось установить, что инфицированность новорожденных или врожденная инфекция, вызванная вирусом лимфоцитарного хориоменингита, заметно отличаются от инфекции, развивающейся в организме животных более старшего возраста, своей интенсивностью и распространенностью.
В патологический процесс широко вовлекаются и невральная паренхима, и мембраны; по мере старения животных число клеток, содержащих вирусоспецифический антиген, снижается и в паренхиме, и в мембранах (Gilden е. а.). Высокие титры вируса в крови, достигающие 105ЛД50/мл сыворотки, сочетаются с интенсивным заражением большинства внутренних органов вскоре после рождения, однако уровни зараженности с возрастом могут снижаться. В реакциях связывания комплемента или нейтрализации не удается обнаружить циркулирующих антител (Colo, Nathanson).
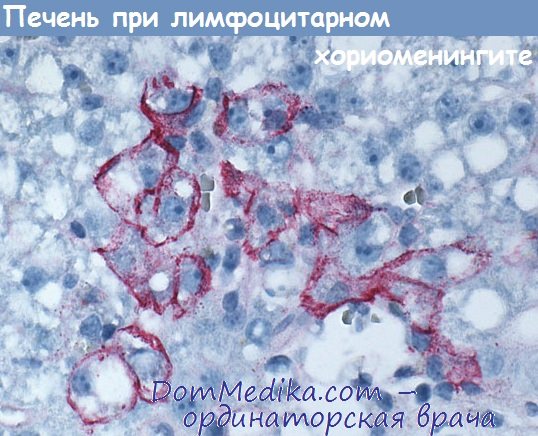
У таких скрыто инфицированных мышей обычно не ранее 6-месячиого возраста может развиться заболевание, характеризующееся сгорбленностью, взъерошенностыо шерсти, блефаритом и другими дегенеративными изменениями, позднее ведущими к смертельному исходу. Hotchin, впервые описавший эту болезнь, в связи со сроками ее развития назвал ее «поздней болезпыо», которая, как показывает гистологическое изучение, сопровождается развитием хронического гломерулонефрита, очаговыми некротическими поражениями печени и появлением интерстициальных круглоклеточных инфильтратов, особенно в почках, печени и легких.
У мышей-гнотобионтов линии Haas, врожденно инфицированных вирусом лимфоцитарного хориоменингита, в случаях развития заболевания также обнаруживали гломерулонефрит, лимфоидную инфильтрацию внутренних органов, повышение уровня сывороточных глобулинов. Гпотобионты оказались толерантными к максимальным субтоксическим дозам циклофосфамида, летальным для обычных животных, и обработка мышей такими повышенными дозами циклофосфамида предотвращала развитие поражений у молодых животных и вызывала обратное их развитие у взрослых (Sharon, Pollard).
Инфекция в клеточных культурах
Представления в патогенезе лимфоцитарного хориоменингита были значительно дополнены результатами изучения инфекционного процесса в модельных опытах in vitro.
Чувствительность различных клеточных культур к вирусу лимфоцитарного хориоменингита рассмотрена в разделе «Возбудитель», где указывалось на возможность формирования в таких системах острой или латентной инфекции.
Острая (продуктивная) инфекция штаммом WE легко воспроизводится в культурах перевиваемых клеток L мышиных эмбрионов обычных мышей или мышей инбредных линий СВА/Са, DBA/2, C3H/He, C57BL/6. Во всех культурах титр вируса достигал максимума к 42 ч (около 104 ЛД50 на клетку), находился на этом уровне до 60 ч, что совпадало со временем начала дегенеративных изменений в культурах. Комплементсвязывающий антиген определяли спустя 30 ч после заражения (Von Boehmer е. а.). МФА предлагается в качестве метода экспресс-диагностики лимфоцитарного хориоменингита, учитывая возможность обнаружения вирусоспецифического антигена в ткани в течение 24—48 ч, легкость выполнения и снижение риска заражения обслуживающего персонала.
Спустя 16 ч после заражения клеток L ультраструктура ядра в основном оставалась неизменной, тогда как цитоплазма и плазматическая мембрана претерпевали существенные изменения: увеличивалась плотность митохондрий; наблюдали образование мембранных структур, состоящих из многослойных концентрически упакованных пластинок или беспорядочных витков. Интересно, что к этому же времени в цитоплазме появлялись единичные или образующие скопления гранулы, которые по морфологии напоминали характерные гранулы, обнаруживаемые внутри частиц аренавирусов. Эти гранулы состоят из гранулярных и (или) палочковидных субъединиц (Mannweiler, Lehmann-Grube).
Персистентная форма инфекции была подробпо изучена при заражении штаммом Са1371 культуры клеток BHK-21/13S (Staneck е. а.). Инфицированные культуры прослежены на протяжении более 300 пассажей. В течение всего времени наблюдения культура сохраняла постоянное время генерации, идентичное контролю. На протяжении первых 2—4 пассажей после заражения наблюдали наивысшую продукцию внеклеточного вируса (13 БОЕ на клетку), при этом более 90% клеток популяции формировали инфекционные центры. При последующих 50 пассажах в культуре постепенно снижался урожай внеклеточного вируса и число инфекционных центров.
В этот период отмечались периодические колебания кривой инфекционности с резкими подъемами и снижениями. После 54-го субкультивирования инфекционность культуральной среды была ничтожно малой (менее 10 БОЭ в 1 мл и менее 10 инфекционных центров на 2*106 клеток). Такой характер инфекции культура сохраняла до 350-го субкультивирования (срок наблюдения). Несмотря на практическое отсутствие синтеза инфекционного вируса, более 90% клеток популяции содержали вирусоспецифический антиген, располагающийся в цитоплазме и на поверхности клеток в виде рассеянных гранул.
Hotcuin на модели персистентиой инфекции культуры клеток L показал сходные закономерности; через 72 ч после заражения количество антигенсодержащих клеток достигало 90% и титр внеклеточного вируса равнялся 107 БОЕ/мл, после чего количество светящихся клеток быстро снижалось до 10%, и в среде обнаруживалось лишь незначительное количество инфекционного вируса. Клонирование культур сразу после инфицирования выявило 15% клонов, продуцирующих вирус, тогда как при клонировании персистентно инфицированной культуры 18-го пассажа вирусная продукция обнаружена менее чем в 1% клонов.
Автор приходит к выводу, что механизм персистенции вируса лимфоцитарного хориоменингита в клетках связан с его супрессией и носит циклический характер. Во всех случаях имеет место чередование инфекции и рефрактерности клеток, которые излечиваются от вирусной инфекции, после чего процесс повторяется вновь. Механизм этого эффекта связывают с изменением в лизосомах инфицированных клеток (Holchin). Представляет интерес сообщение Simon, описавшего гомологичную интерференцию вируса лимфоцитарного хориоменингита. При заражении штаммом WE3 культуры клеток обезьяньей почки с высокой множественностью выход вируса оказывался непропорционально низким, а культураль-ная среда содержала фактор, подавляющий репродукцию гомологичного штамма. Это явление не было обусловлено интерфероном.
Инфицированный титр вируса в культурах достигал максимума через 48 ч после заражения, а интерферирующая активность возрастала до 120 ч (время наблюдения).
Обнаруженный феномен, по мнению Simon, вызван накоплением дефектных вируспых частиц.
Фактором, определяющим патогенетические особенности лимфоцитарного хориоменингита, могут быть также биологические различия между штаммами вируса. Они могут существенно влиять на процент зараженных новорожденных мышей, которые выживут и станут вирусоносителями (Hotchin е. а.). Так, например, штамм Е-350 при впутримозговом заражении вызывает почти 100% гибель животных, тогда как другие штаммы в зависимости от дозы — 30—90% гибель (Lehmann-Grube). Штамм Е-350, пассировавшийся на мозговой ткани животных, оказывается безвредным при параневральном способе инокуляции.
Наоборот, после внутрибрюшинной инъекции висцеротропные штаммы могут интенсивно репродуцироваться в центральной нервной системе и вызывать смертельный лимфоцитарный хориоменингит либо иммунологически опосредованное заболевание внутренних органов, сопровождающееся плевральными и перитонеальными экссудатами и поражениями легких, печени и почек (Rowe).
При сравнении реакции нескольких штаммов инбредных мышей на заражение вирусом лимфоцитарного хориоменингита М. Ю. Кочеровская отметила существенные различия: наиболее чувствительными к вирусу оказались мыши линии Сс57Пг, СВА и AKR, животные линии Balb/c и DBA/2 оказались более резистентными. Oldstone и McDevitt (цит. по Cole, Nathanson) показали, что различия в тяжести течения иммунологи чески опосредованного заболевания могут зависеть от функциональных различий генов иммунной реакции, сцепленных с Н-2-локусом гистосовместимости.
- Читать "Иммунитет при лимфоцитарном хориоменингите (ЛХМ) - исследования in vivo"
Оглавление темы "Медленные вирусные инфекции":- Иммунитет при врожденной краснухе
- Эпидемиология врожденной краснухи - распространенность
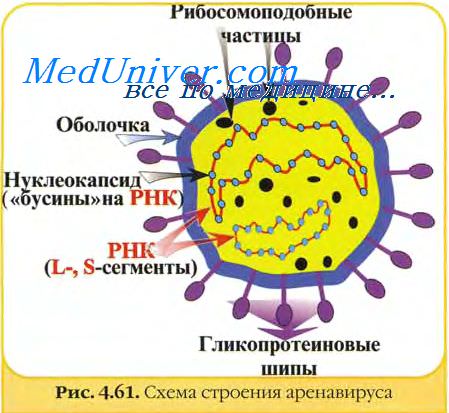
- Вирус лимфоцитарного хориоменингита (ЛХМ) - структура, характеристика
- Клиника лимфоцитарного хориоменингита (ЛХМ) - проявления
- Патогистология лимфоцитарного хориоменингита (ЛХМ)
- Патогенез лимфоцитарного хориоменингита (ЛХМ)
- Иммунитет при лимфоцитарном хориоменингите (ЛХМ) - исследования in vivo
- Иммунитет при лимфоцитарном хориоменингите (ЛХМ) - исследования in vitro
- Эпидемиология лимфоцитарного хориоменингита (ЛХМ) - распространенность
- Возбудитель лихорадки Ласса - структура, характеристика
