Патогенез подострого склерозирующего панэнцефалита (ПСПЭ)
Патогенез подострого склерозирующего панэнцефалита (ПСПЭ) до сих пор недостаточно ясен. Первый вопрос, который требует ответа, состоит в следующем: способен ли вирус кори персистировать в организме после перенесенного заболевания?
По-видимому, на этот вопрос следует дать утвердительный ответ, во-первых, потому, что подострый склерозирующий панэнцефалит (ПСПЭ) возникает (и иногда спустя много лет) либо после перенесенной кори, либо после вакцинации живой противокоревой вакциной (Schneck); во-вторых, еще в 1965 г. Enders-Ruckle сообщила о выделении инфекционного вируса кори из трипсинизированной селезенки и лимфатических узлов внешне здорового 46-летнего мужчины, погибшего от несчастного случая. Помимо этого, автору удалось показать возможность сохранения до 2 мес вируса кори в организме обезьян.
Признание возможности поддержания длительной латентной коревой инфекции после перепесенного заболевания (или вакцинации живой вакциной) хорошо объясняет также длительность и прочность противокоревого иммунитета. Однако при этом возникает и другой вопрос: если корью, за редким исключением, переболевают почти все и, следовательно, вирус кори персисти-рует в организме у подавляющего большинства людей, то почему же, к счастью, столь редки случаи подострого склерозирующего панэнцефалита (ПСПЭ)?
Пока нет однозначного ответа на этот вопрос, и хотя его обсуждение продолжается до сегодняшнего дня, современные представления могут быть даны в нескольких главных концепциях.
Первая и, наверное, самая ранняя из них опирается на результаты большого экспериментального материала, посвященного моделированию персистентной коревой инфекции в клеточных культурах (Rustigian, Winston е. а.,). Уже давно было отмечено, что выжившие после заражения вирусом кори клетки дают начало новой популяции, поддерживающей персистентную инфекцию (Rustigian). Позднее обнаружили, что развитие такой формы инфекции оказывается связанным с селекцией варианта вируса, характеризующегося низкой вирулентностью для клеток (Rnstigian).
Отсюда понятно мнение многих исследователей, предположивших, что способность вируса кори индуцировать персистентную инфекцию в условиях in vitro и особенности возникающих при этом взаимоотношений вируса с клеткой могут отражать те взаимоотношения между вирусом кори и организмом, которые приводят к развитию подострого склерозирующего панэнцефалита (ПСПЭ) (Adels е. а., Johnson, HortaRarbosa е. а.). Это мнение в последующем подкреплялось результатами исследований in vitro и in vivo (Greonham е. a., Rurnstein, e. a.).
Dnbois-Dalcq с соавт. провели сравнительное изучение продуктивной и латентной инфекции в клетках Vero, инфицированных вирусом кори, выделенным от больного подострого склерозирующего панэнцефалита (ПСПЭ). При продуктивной инфекции наблюдали выраженный ЦПЭ, инфицированные клетки адсорбировали эритроциты обезьян, в культу-ральной жидкости обнаруживали гемагглютинин, в цитоплазме клеток выявлялись массивные скопления вирусного антигена. В клетках присутствовали как включения, содержащие вирусные нуклеокапсиды, так и зрелые вириопы.
В латентно инфицированных культурах наблюдали только очаговые слияния клеток. Вирусный антиген выявляли только в гигантских клетках и притом в небольшом количестве. Культуры не обладали гемад-сорбирующей и гемагглготипирующей активностью. В клетках не обнаруживали зрелых вирусных частиц, хотя в цитоплазме имелись зрелые нуклеокапсиды, включения не обнаружены, реакция с коревыми антителами в пероксидазном тесте отрицательная.
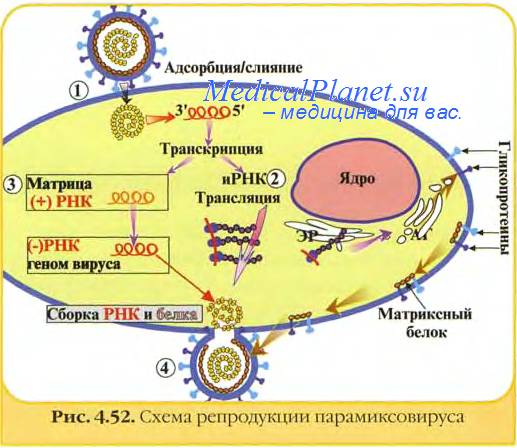
Авторы приходят к выводу о весьма вараженпом сходстве между латентной инфекцией в культуре и процессом, который имеет место в мозговой ткани человека при подострого склерозирующего панэнцефалита (ПСПЭ) (Dubois-Dalcq е. а.).
В свете этих представлений следует вспомнить данные Winston с соавт., показавших, что вирус кори, выделенный из персистентно инфицированных клеток, отличается от вируса, выделяемого при продуктивной инфекции, меньшим удельным содержанием низкомолекулярных образцов РНК.
Анализ событий в клетках, латентно инфицированных вирусом кори, выделенным от больных подострым склерозирующим панэнцефалитом (ПСПЭ) (Doi е. а., Dubois-Dalcq е. а.), и в мозговых клетках больных подострым склерозирующим панэнцефалитом (ПСПЭ), обследованных сразу (Dubois-Dalcq е. а.) или культивируемых in vitro (Oyanagi е. а.), показал, что процессы созревания вируса приостановлены на уровне клеточпых мембран, вследствие чего вирус формируется не полностью. Учитывая все эти данные, многие исследователи объясняют развитие подострого склерозирующего панэнцефалита (ПСПЭ) образованием и накоплением в мозговой ткапи дефектных вирионов вируса кори (Freeman, Dubois-Dalcq е. а., Meulen).
Именно дефектностью вирионов объясняли Zeman и Kolar трудности выделения инфекционного вируса кори из секционного материала лиц, погибших от подострого склерозирующего панэнцефалита (ПСПЭ).
Katz и Koprowski, обсуждая причины неудач при выделении инфекционного вируса, высказывали предположение, что для патогенеза подострого склерозирующего панэнцефалита (ПСПЭ) не требуется полный вирус. По их мнению, персистируюнщй в мозговой ткани дефектный вирус кори реализует свою раннюю функцию, которая выражается в синцитиогенном действии. Дефектпый вирус кори, вызывая слияние клеток, способствует медленному распространению в мозговой ткани другого вируса из группы папова, который сам по себе не способен переходить из клетки в клетку и существует в тканях хозяина, не вызывая заболевания (Iwasaki, Koprowski). При достаточном распространении последнего вируса и развиваются симптомы заболевания.
Yamamoto и Koprowski исследовали влияние двух вирусов группы папова на течение энцефалита, вызываемого вирусом, выделенным от больных подострым склерозирующим панэнцефалитом (ПСПЭ). Для этого сирийских хомяков заражали в разные сроки (от рождения до 3 нед) и наблюдали в течение 50—60 дней. Оказалось, что чувствительность животных к энцефалиту после заражения только одним вирусом от больных подострым склерозирующим панэнцефалитом (ПСПЭ) снижается по мере увеличения возраста зараженных хомяков. При комбинированном заражении вирусом от больных подострым склерозирующим панэнцефалитом (ПСПЭ) и одним из паповавирусов в зависимости от времени введения последних наблюдали либо ингибирование заболевания, либо более прогрессивное его течение.
Некоторые авторы, основываясь на результатах сравнительного апализа свойств вируса, выделенного от больных типичной корью, и вирусов, выделенных от больных подострым склерозирующим панэнцефалитом (ПСПЭ), считают их различными и предпочитают называть вирус, выделенный от больных подострым склерозирующим панэнцефалитом (ПСПЭ), «агент ПСПЭ», или «кореподобный вирус» (Oyanagi е. а., Meulen е. а., Payne, Baublis). Эти исследователи рассматривают возбудитель подострого склерозирующего панэнцефалита (ПСПЭ) как вариант, или мутант, коревого вируса, который либо возникает в организме, либо селекционируется под действием специфических антител.
Последняя возможность кажется вполне реальной в связи с известной высокой частотой вовлечения в инфекционный процесс при кори центральной нервной системы (Ghelman, Ghelman, Purdham, Batty).
Наиболее значительными отличиями «агента подострого склерозирующего панэнцефалита (ПСПЭ)» Meulen с соавт. считают замедленный характер репродукции штаммов подострого склерозирующего панэнцефалита (ПСПЭ) в системах in vitro, низкий урожай инфекционного вируса, значительные количества дефектных частиц, присутствие нуклеокапсидов в составе больших внутриядерных включений в виде гладких нитей диаметром 150—170 им или гранулярных нитей диаметром 22—25 нм в цитоплазме вдали от клеточной мембраны. Вирус от больных подострым склерозирующим панэнцефалитом (ПСПЭ), в отличие от вируса кори, вызывает энцефалит у хорьков, хомяков и других животпых.
В. И. Хозинский и И. А. Карасева, подробно анализируя вопрос о принадлежности «агента подострого склерозирующего панэнцефалита (ПСПЭ)», в первую очередь отмечают, что первые три из перечисленных выше особенностей характерны для супрессированного вируса кори в персистентно инфицированных клеточных культурах и были отмечены еще Riistigian. Характер локализации клеточных включений зависит от времени выделепия штамма (Enders-Ruck1е) и наиболее редко встречается у аттенуировапных вариантов, а количественные изменепия во внутриклеточной локализации пуклеокапсида нередко связаны с изменением типа цитопатического действия (М. Б. Королев и др.).
Штаммы, выделяемые от больных корью и больных подострым склерозирующим панэнцефалитом (ПСПЭ), идентичны в антигенном отношении, все они образуют внутриядерные и внутрицитоплазматические включения, синцитий в клеточных культурах, нуклеокапсиды их имеют одинаковую структуру, а вирионы почкуются на клеточной поверхности Все это дает основание считать, что отмеченные рядом авторов особенности носят лишь количественный характер.
В. И. Хозинский и И. А. Карасева справедливо возражают против представления, что «агент ПСПЭ» является мутантом коревого вируса, ибо при этом следовало бы допустить '«осуществление однозначных и направленных мутаций во всех случаях заболевания ПСПЭ».
Действительно, нельзя не признать, что ПСПЭ - очень редкое заболевание. Сопоставляя эту особенность ПСПЭ и почти убиквитарное распространение вируса кори, Payne допускает, что в подобной ситуации или больной, или окружающая его среда, или инфицирующий вирус, по-видимому, являются необычными. Вирус кори, однако, обладает очень низкой частотой спонтанной мутации, поэтому более вероятно, что ПСПЭ может быть редким результатом инфекции нормального индивидуума нормальным штаммом вируса кори в окружающей среде (клетке), которая оказывается необычной. Автор предполагает присутствие вирусного генома в мозговой ткани больного ПСПЭ, которое не сопровождается образованием инфекционного вируса, что может быть связано с блоком поздних этапов вирусной репродукции.
При пассировании неразведенпого вируса кори накапливается большое число дефектных частиц, которые интерферируют с репродукцией инфекционного вируса. РНК таких интерферирующих структур имеет копстапту седиментации, соответствующую 18S, тогда как константа седиментации РНК инфекционного вируса равна 50S (Martin).
Интересна роль ядра в репродукции вируса ПСПЭ, который размножается в содержащих ядра клетках BSC-1 до более высоких титров, чем обычный вирус кори. В безъядерных же клетках BSC-1 вирус ПСПЭ формирует урожай в 100 раз меньший, хотя все полипептиды, синтезируемые в заражепных вирусом ПСПЭ ядерных клетках, появляются и в безъядерных (Follett е. а.).
Так или иначе, но независимо от степени родства вируса ПСПЭ с вирусом, вызывающим обычную корь, дефектность возбудителя ПСПЭ кажется очевидной. На эту дефектность или супрессироваппость вируса указывали еще Horta-Barbosa с соавт., выделившие супрессированный вирус из лимфатического узла больного ПСПЭ. Вместе с тем степень такой супрессии вируса в организме больных ПСПЭ, по-видимому, неодинакова. По мнению Katz и Koprowski, об этом свидетельствует неодинаковая эффективность выделепия возбудителя из проб биопсии мозговой ткани, а также непостоянное обнаружение вирусоспецифического антигена с помощью МФА. Кроме того, из проб биопсии мозга больных легко удается получить культуры перевиваемых клеток.
Такого же рода клеточные культуры формируются под действием вируса кори (Webb е. а., Gibson, Bell), что свидетельствует о его цитопролиферативной и трансформирующей активности.
Наконец, недавно получены данные, позволяющие по-новому подойти к оценке возможных механизмов патогенеза ПСПЭ. Прежде всего исследовали механизм персистенции вируса кори в хронически инфицированной культуре фибробластов куриного эмбриона. С помощью МФА вирусоспецифический антиген обнаруживали в 10—15% клеток, в культуральной жидкости инфекционная активность не определялась и была очень низкой в клеточных гомогенатах. Вместе с тем в освобожденных от митохондрий цитоплазматических экстрактах обнаружены рибонуклеопротеидные структуры с константой седиментации 200S и плавучей плотностью в градиенте хлорида цезия, равной 1,31 г/мл.
На этом основании для выяснения собственно механизмов вирусной персистенции были предприняты опыты молекулярной гибридизации вирионной РНК и ДНК хронически инфицированных клеток. Показано, что ДНК незаражеиных куриных фибробластов практически не содержат участков, гомологичных вирусу кори, в то время как у ДНК из хронически инфицированных клеток гомология с вирионной РНК была весьма выражоппой (Zhdanov, Parfanofich, М. И. Парфанович).
Естественно, что полученные результаты обосновывают необходимость проведения опытов молекулярной гибридизации вирионной РНК с ДНК мозговых клеток людей, погибших от ПСПЭ. Однако уже сегодня, учитывая ряд общих черт между хронически инфицированными культурами клеток и мозговыми клетками больных ПСПЭ (обнаружение нуклеокапсидов, вирусоспецифического антигена, при отсутствии инфекционного вируса, выявление которого затруднено и требует кокультивирования клеток), можно предполагать, что интеграция генома коревого или кореподобного вируса с геном мозговых клеток в форме ДНК-транскрипта определяет особенности патогенеза ПСПЭ.
Правда, доказательство подобной возможности еще не будет означать объяснения патогенеза ПСПЭ, ибо останется неясным, является ли развитие ПСПЭ результатом интеграции геномов вируса и геномов клетки или активации вируса, уже находящегося в супрессированном состоянии. Последняя возможность кажется нам более вероятной.
- Читать "Иммунитет при подостром склерозирующем панэнцефалите (ПСПЭ)"
Оглавление темы "Подострый склерозирующий панэнцефалит (ПСПЭ) и врожденная краснуха":- Возбудитель подострого склерозирующего панэнцефалита (ПСПЭ) - вирус кори
- Клиника подострого склерозирующего панэнцефалита (ПСПЭ) - проявления
- Патогистология подострого склерозирующего панэнцефалита (ПСПЭ)
- Патогенез подострого склерозирующего панэнцефалита (ПСПЭ)
- Иммунитет при подостром склерозирующем панэнцефалите (ПСПЭ)
- Эпидемиология при подостром склерозирующем панэнцефалите (ПСПЭ)
- Возбудитель врожденной краснухи - вирус краснухи
- Клиника врожденной краснухи - проявления
- Патогистология врожденной краснухи
- Патогенез врожденной краснухи
