Методы хемилюминесценции для оценки антиоксидантной активности (АОА). Метод инициированного окисления углеводородов
Использование достаточно разбавленных растворов липидов дает возможность исключить влияние на скорость окисления дополнительного генерирования свободных радикалов, образующихся из липидов.
Таким образом, антиокислительная активность липидов, определяемая этим методом, является мерой количества природных антиоксидантов, содержащихся в них.
Вообще говоря, более строгой модификацией этого метода является определение общей скорости окисления метилолеата по поглощению кислорода. В этом случае можпо исключить влияние веществ липидного происхождения, способпых разрушать гидроперекиси.
К сожалению, классические методы определения активности антиоксидантов очень длительны, трудоемки и малочувствительны, хотя и дают общую характеристику антиокислительпой активности. В связи с этим в последние годы для оцопки антиокислительных свойств липидов все чаще используются более точные и оперативные методы хемилюминесценции (ХЛ), которые успешно применяются в химии для определения констант элементарных стадий окисления.
Работы в области применения ХЛ методов для изучения активности липидов ведутся в основном в двух направлениях. С одной стороны, усиленно изучается собственное свечение липидов и их фракций, с другой — создаются и разрабатываются новые ХЛ модели, на которых изучается активность липидов, их фракций и веществ биологического происхождения.
Однако во многих работах не учитывается сложпый, многокомпонентный состав липидов, отдельные составляющие которых могут выполнять как роль активаторов, так и роль тушителей свечения, а по отношению к окислению быть инициаторами или ингибиторами. Поэтому для изучения свойств липидов особенно важна разработанность ХЛ моделей, изучение природы свечения и химических реакций, ответственных за возникновение свечения.
Метод инициированного окисления углеводородов
Для примера разберем ХЛ модель инициироваппого окисления углеводородов, разработаппую в ИХФ АН СССР в лаборатории В. Я. Шляпиптоха. Эта модель широко применяется для определения активности синтетических ингибиторов.
При иницированном окислении углеводородов хемилюминесценция возникает при рекомбинации перекисных радикалов, поскольку только эти реакции достаточно экзотермичны для возбуждения свечения в видимой области. Рекомбинация радикалов практически не требует энергии активации (Е = = 3 ккал/моль), а тепловой эффект, оцененный как разпость разрывающихся и образующихся связей, составляет пе менее 100 ккал/моль. В результате рекомбинации перекиспых радикалов образуются возбужденные молекулы ацетофепопа, способные испускать свечение в видимой части опектра. Интенсивность свечения процорциональна квадрату концентрации перекиспых радикалов. Поэтому все факторы, влияющие на концентрацию и состав порекисных радикалов (температура опыта, концентрация реагентов, добавки инициаторов или ипгибиторов, катализаторов), должны влиять на интенсивность свечения.
Механизм действия различных добавок на свечение может быть как физическим, так и химическим. Физический механизм действия связан с тушением возбужденных состояний, с появлением в системе в результате переноса энергии повых излучающих частиц, с влиянием сроды на вероятность оптических переходов и дезактивации.
Для физических тушителей зависимость иптенсивпости свечения от концентрации введенного вещества определяется уравнением Штерна-Фольмера: I/I0=1+Kqt[Q], где I и I0 — интенсивность свечения системы в присутствии тушителя и без пего, т — время жизни возбужденной молекулы в отсутствие тушителя, [Q] — концентрация тушителя.
Химический механизм тушения проявляется в изменении концентрации свободных радикалов в системе и в большинстве случаев связан с изменением скорости процесса окисления или с заменой одного типа радикалов другим. Поскольку скорость окисления может быть измерена другими методами (например, по поглощению кислорода или но накоплению гидроперекисей), то корреляция кинетических кривых изменения интенсивности свечения и скорости окисления является доказательством химического механизма действия добавок. Только при этом условии по ХЛ данным можпо определить способность веществ реагировать со свободными радикалами.
В этом случае кинетические кривые изменения интенсивности свечения имеют S-образную форму в могут быть охарактеризованы следующими параметрами: минимальной интенсивностью свечения в момент введения вещества (I), периодом индукции (т), т. е. отрезком времени, в течение которого сохраняется мипимальная интенсивность свечения, и наклоном касательной (dI/I0dt)max,, проведенной в точке перегиба, величина которого пропорциональна максимальной скорости расходования ингибитора.
Величина константы скорости реакции (к7) может и по величине максимальной скорости изменения интенсивности свечения, экстраполированном к пулевой концентрации введенного вещества:
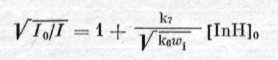
и по величине максимальной скорости изменения интенсивности свечения, экстраполированном к пулевой концентрации введенного вещества:
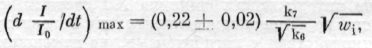
где I и I0 — интенсивность свечения системы в присутствии исследуемого вещества и без него, w1 —скорость зарождения в системе свободных радикалов, [InН]0 — концентрация введенного вещества.
Если радикалы, образующиеся из молекулы ингибитора, достаточно активны, чтобы участвовать в реакции 10 продолжения цепи, то стехиометрический коэффициент реакции для такого ингибитора будет ниже двух. В этом случае константы к7, вычисленные по формуле (5), будут иметь заниженные значения, так как схема расчета, примененная в данном случае, не предусматривает протекание реакции 10. Значения к7, вычисленные по формуле, не зависят от принятой схемы расчета и являются истинными значениями к7.
Изучение эффективности индивидуальных химических веществ разного строения показало, что только при сопоставлении различных параметров свечения можно определить активность соединений. Если активность изучаемых соедипопий вычислять только по изменению интенсивности свечения, то можно получить заниженные значения констант к7. Правильная интерпретация ХЛ даппых возможна только при наличии проверки механизма тушения свечения. Описанным методом была изучена активность некоторых природных аптиоксидаптов: стероидных гормонов, токоферола, некоторых производных госсипола и пирокатехина. Оказалось, что перечисленные вещества имеют довольно высокие значения констант к7, которые на 1—2 порядка превышают зпачепие к7 для наиболее распространенных синтетических ингибиторов радикальных процессов. Кроме того, такие соединения, как токоферол и некоторые пирокатехины, имеют стехиометрический коэффициент ингибирования, превышающий два, т. е. одпа молекула ингибитора обрывает более двух цепей окисления.
При совместном действии двух ингибиторов на ХЛ систему форма кинетических кривых свечения зависит от наличия взаимодействия между ними. В том случае, когда ингибиторы действуют независимо друг от друга, кривые свечения можно разбить па два участка, соответствующие расходованию каждого ингибитора в отдельности. Сначала расходуется ипгибитор с более высоким значением к7, затем — более слабый. Так, при изучении действия смесей аминов тт феполов была обнаружена новая форма синергизма: фонолы восстанавливают радикалы, образующиеся из молекул амина, тем самым усиливая эффективность их действия.
Изменение интенсивности свечения ХЛ системы может быть вызвано не только изменением концентрации перокисных радикалов при взаимодействии о ингибиторами, но изменением состава радикалов системы. Так, например, интенсивность свечения резко мепяется при замене алкильных радикалов на перекисные, на чем основан метод кислородного последствия.
Интенсивность свечения может меняться при образовании в системе нового сорта перекисных радикалов. В этом случае в системе появляются две повые реакции рекомбинации с другими выходами свечения. Так, добавление к этилбензолу циклогексана уменьшает, а дифенилметана увеличивает свечение. Кроме того, интенсивность свечения по-разному зависит от концентрации того вещества, которое является субстратом окисления.
Как видно из изложенного, применение ХЛ методов к изучению активности индивидуальных химических соединений требует определенной осторожности в интерпретации опытных данных, поскольку необходимо учитывать возможное изменение состава ХЛ системы и протекание побочных реакций. Задача во много раз усложняется при изучении ХЛ методами таких сложных многокомпонентных систем, как липиды.
- Читать "Методы электрохемилюминесценции (ЭХЛ). Значение ЭХЛ в определении антиоксидантной активности (АОА)"
Оглавление темы "Оценка антиокислительной активности антиоксидантов в онкологии":- Антиоксиданты. Что такое антиоксиданты?
- Общая антиокислительная активность (АОА). Антиокислительная активность липидов
- Пути торможения окисления. Оценка антиоксидантной активности (АОА)
- Определение антиокислительной активности (АОА) веществ. Определение активности липидов
- Окисление метилового эфира олеиновой кислоты. Влияние температуры на антиоксиданты
- Методы хемилюминесценции для оценки антиоксидантной активности (АОА). Метод инициированного окисления углеводородов
- Методы электрохемилюминесценции (ЭХЛ). Значение ЭХЛ в определении антиоксидантной активности (АОА)
- Модель окисленной олеиновой кислоты. Влияние антиоксидантов на окисление олеиновой кислоты
- Изучение процесса окисления липидов. Окисление ненасыщенных жирных кислот
- Определение активности липидов по методу Глевинда. Различия антиокислительной и антирадикальной активности
