Нарушения свертываемости крови и тромбоэмболии после инсульта: причины, признаки, диагностика, лечение
а) Введение. Рассмотрим физиологический гемостаз. Нормальный гемостаз, состояние между двумя крайними его проявлениями - кровотечением и тромбозом, обеспечивается сложным взаимодействием между сосудистой стенкой, клетками крови и факторами плазмы. Изменения в сосудистой стенке инициируют процесс свертывания крови, при котором тромбоциты, а также лейкоциты, взаимодействуя с гликопротеиновыми рецепторами (например, интегрином). «прилипают» к поврежденному эндотелию или обнаженным субэндотелиальным структурам (например, коллагену).
Происходит активация клеток, приводящая к изменениям в мембранах эндотелия, тромбоцитов и лейкоцитов; при этом отрицательно заряжающаяся поверхность фосфолипопротеинов, обладающая прокоагулянтным свойством, обеспечивает оптимальный процесс свертывания плазмы (который по существу инициируется «тканевым фактором»).
Вещества, которые при этом высвобождаются, и синтезированные медиаторы вовлекают в процесс другие клетки крови и ускоряю! образование фибрина. Возникающий конгломерат клеток стабилизируется образующимся параллельно фибрином, при этом существует положительная обратная связь между образованием тромбина и фибрина в плазме, а также аккумуляцией и активацией тромбоцитов и лейкоцитов.
Динамика образования фибрина и его количество модулируются в основном концентрацией и активностью клеточных компонентов, факторов и ингибиторов свертывания. Активная ретракция кровяного сгустка и реактивный фибринолиз (который в свою очередь регулируется активаторами и ингибиторами свертывания крови) параллельно с заживлением поврежденной сосудистой стенки вызывают процесс растворения сгустка, который направлен на восстановление просвета сосуда (рис. 1).
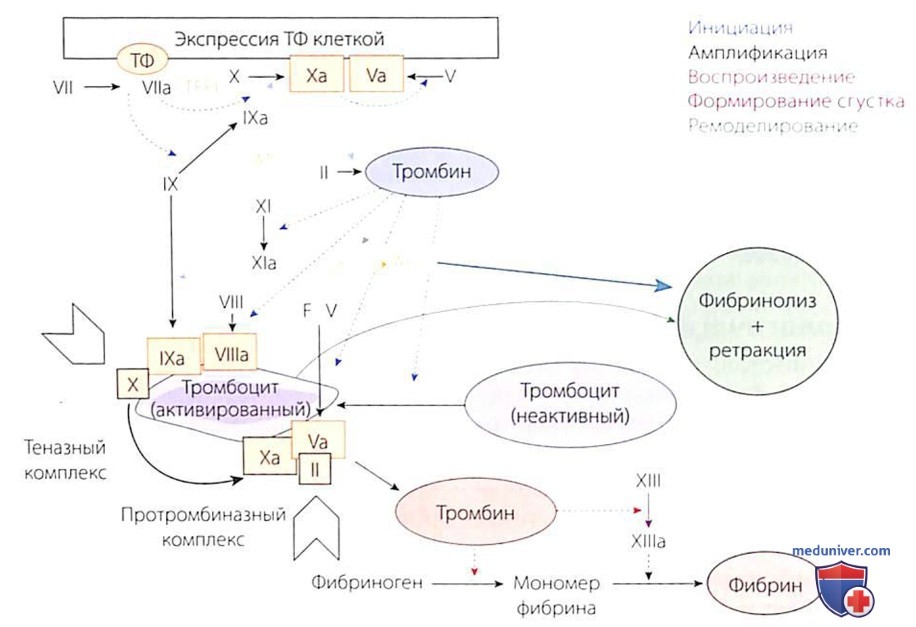
АРС - активированный белок С; AT III - антитромбин III; FV - фактор свертывания V; PC - протеин С; TFPI - ингибитор пути тканевого фактора.
Компоненты и медиаторы, участвующие в процессе свертывания крови, модулируют также функцию других плазматических каскадных систем. Качественные и количественные изменения отдельных компонентов гемостаза не проявляются клинически кровотечением или тромбозом, пока активность процесса свертывания не снизится по меньшей мере на 30% или не увеличится на 150%. Легкие функциональные нарушения отдельных факторов не регистрируются с помощью рутинных методов диагностики, однако во взаимодействии с какими-либо эндогенными или экзогенными токсическими веществами могут способствовать декомпенсации баланса гемостаза и приводить к тромбозу или кровотечению.
Взаимодействие различных компонентов гемостаза в норме регулируется таким образом, что подпороговые отклонения его как в направлении снижения свертывания, так и его повышения быстро подавляются и система вновь возвращается в стабильное исходное положение.
P.S. Лечение тромбогенных нарушений. В распоряжении больных с риском тромбогенных нарушений имеется множество средств для антитромботической терапии. Возможности больных с риском кровоизлияний в этом отношении весьма ограничены.
б) Геморрагические осложнения и геморрагические диатезы. Различные кровотечения у пациентов после перенесенного инсульта являются частой причиной вызова платных бригад скорой помощи Скороздрав в Москве. Диагностика и экстренная помощь при кровотечении определяются клиническими симптомами и специфическим анамнезом.
При значительном кровотечении, опасном для жизни, следует на время отменить противотромботические препараты. При этом можно не дожидаться результатов назначенных исследований для оценки гемостаза (см. ниже).
P.S. Источник и остановка кровотечения. Первоочередной задачей при лечении больного с кровотечением является идентификация источника кровотечения и его остановка с помощью локальных мер.
Для идентификации источника кровотечения и его остановки применяют нс только методы эндоскопической диагностики и лечения, но и оперативное вмешательство, а также рентгенологические методы исследования (например. КТ, ангиографию) и рентгенохирургические вмешательства.
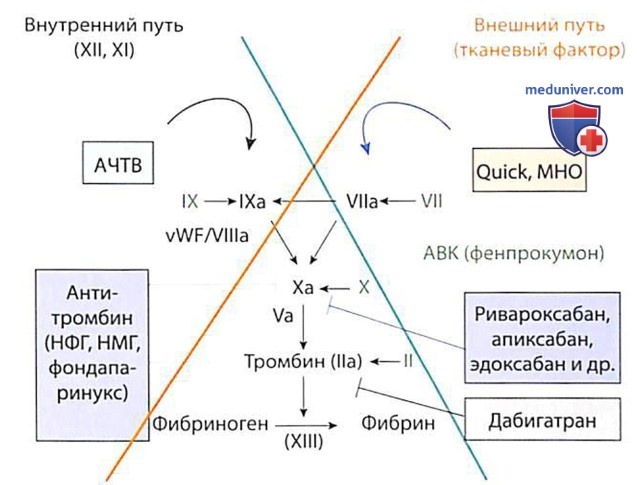
АВК - антагонисты витамина К; НФГ - нефракционированный гепарин; НМГ - низкомолекулярный гепарин; vWF - фактор фон Виллебранда.
Для лабораторного исключения или подтверждения выраженных нарушений гемостаза используются следующие показатели (рис. 2):
• АЧТВ;
• тромбопластиновое (протромбиновое) время, протромбиновый индекс, МИО;
• количество тромбоцитов (общий анализ крови);
• анализ «по месту лечения» (технология «point of саге») позволяет дать оценку показателей гемостаза и в дальнейшем контролировать лечение.
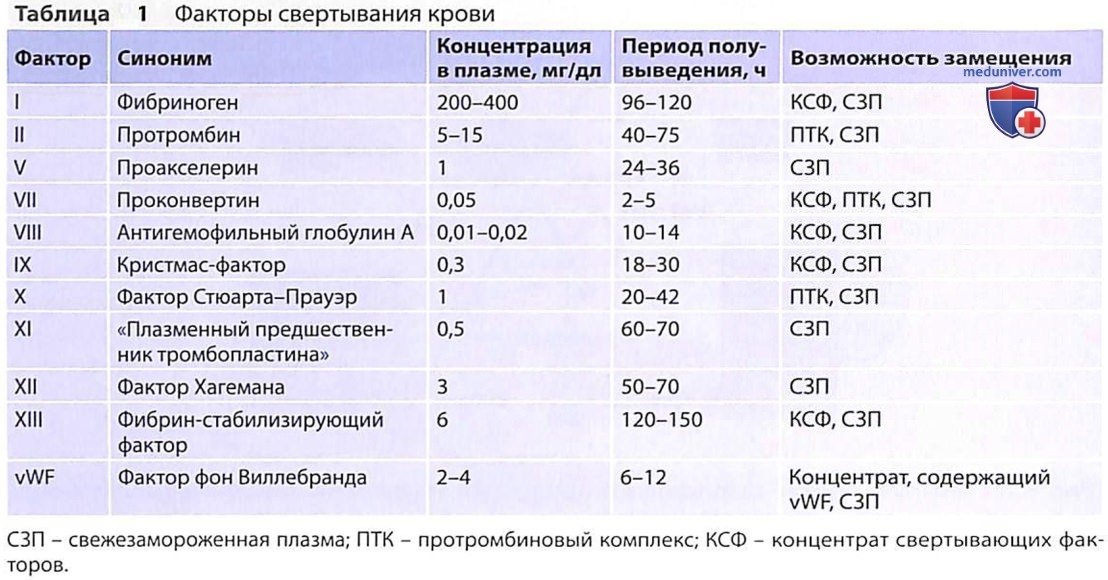
1. Нарушения плазменного гемостаза. Дальнейшая дифференциальная диагностика основана на результатах общих анализов и охватываемых ими показателях свертываемости (см. рис. 2; табл. 1). При необходимости прицельно определяют активность отдельных факторов. Особо следует упомянуть недостаточность фактора XIII, которую можно подтвердить или исключить с помощью специального анализа.
Иногда причиной удлинения плазменного времени свертывания служат ингибиторы (приобрегенные ауто- или аллоангитела), которые могут приводить к уменьшению активности различных факторов (например, фактора VIII при приобретенной гемофилии) или нарушению процесса свертывания in vitro (например, при наличии в крови волчаночного антикоагулянта). Наличие этого ингибитора можно подтвердить или исключить, смешивая образец плазмы крови больного с нормальной плазмой.
P.S. Внимание! Если показатели плазменных тестов находятся в пределах референтных значений (соответствуют норме), это не позволяет с уверенностью исключить клинически значимые нарушения гемостаза!
При спонтанных кровоизлияниях в результатах плазменных тестов свертывания, таких как АЧТВ, выявляются отклонения, что служит основанием для проведения дальнейшей диагностики. При послеоперационных и носправматических кровотечениях, напротив, нарушения гемостаза выражены минимально, и результаты анализов могут существенно отличаться от «нормальных» показателей для подобных состояний, которые, как правило, сопровождаются кровотечением.
P.S. Внимание! В основе минимальных, но верифицируемых отклонений от референтных значений могут лежать значительные нарушения гемостаза!
- Прагматическая терапия. До тех пор пока не удастся подтвердить или исключить нарушения свертываемости и назначить специфическое лечение, следует восполнить недостаток циркулирующей крови, обусловленный кровотечением. Для этого применяется, в частности, эритроцит-ная масса в сочетании с плазмозаменителя-ми, например свежезамороженной плазмой в соотношении 1:1, если отмечаются изменения в АЧТВ.
В качестве крайней меры для «неспецифической» остановки кровотечения могут применяться десмопрессин, протромбиновый комплекс, активированный протромбиновый комплекс или рекомбинантный активированный фактор VII (rhFVIIa - табл. 2), если их можно получить в кратчайшее время; они способствуют тромбообразованию в области раны или подавляют фибринолиз.

Значительно чаще наблюдаются комплексные нарушения свертывания крови, которые характеризуются недостаточностью нескольких компонентов гемостаза. Они нередко бывают обусловлены применением препаратов или являются симптомом системного заболевания или поражения какого-либо органа. Склонность к спонтанным кровоизлияниям возникает в этих случаях только при выраженных нарушениях. Анамнез больного, в том числе семейный, но геморрагическим диатезам не отягощен.
2. Антикоагулянты. При лечении кровотечения на фоне приема антикоагулянтов следует учитывать тип препарата. особенности кровотечения, а также основное заболевание.
P.S. Внимание! Резкая отмена антикоагулянта может вызвать клинические проявления сосудистого заболевания, по поводу которого был назначен препарат!
Вводимые подкожно гепарины или фондапаринукс практически не имеют препаратов-антагонистов. Поэтому следует дождаться уменьшения концепт рации препарат а в плазме, применяя при этом симптоматическое и/или гемостатическое лечение. Это в основном касается и новых пероральных антикоагулянтов прямого действия. Концентрацию дабигатрана и, возможно, эдоксабана в плазме можно существенно уменьшить с помощью гемодиализа. Всасывание новых пероральных антикоагулянтов прямого действия в ЖКТ и их энтерогепатическую циркуляцию можно ограничить с помощью перорального приема активированного угля.
Препарат в виде концентрата протромбинового комплекса для быстрой и эффективной нормализации гемостаза доступен только для антагонистов витамина К. Однако вопрос о том, улучшает ли его применение результат лечения при угрожающем жизни кровотечении и имеет ли он преимущества по сравнению с более медленно действующим витамином К и свежезамороженной плазмой, остается открытым.
3. Тромбоцитопения. Определение. Под тромбоцитопенией подразумевается снижение количества тромбоцитов в периферической крови до уровня менее 150 000/мкл.
Однако только при количестве тромбоцитов менее 50 000-30 000 в 1 мкл возникает спонтанное кровотечение. Если клинические признаки кровотечения при выраженном снижении количества тромбоцитов отсутствуют, следует иметь в виду псевдотромбоцитопению - ошибочное определение количества тромбоцитов за счет феномена агглютинации в этилендиаминтетрауксусной кислоте in vitro. Ее можно исключить, применяя альтернативные антикоагулянты (например, цитрат натрия или гепарин), и иногда, при неоднозначном результате, - путем исследования мазка из свежевзятой (нативной) крови.
Приобретенная тромбоцитопения может развиваться после гипотермии, обширных травм мягких тканей или венозного стаза, а также вследствие массивного разрушения и разведения тромбоцитов, наблюдаемого при гемотрансфузии или применении экстракорпорального кровообращения. Кроме того, она наблюдается при миелопролиферативных или миелодиспластических синдромах, лейкозах пли инфильтрации костного мозга опухолью. Клиническое значение имеет и тромбоцитопения, обусловленная поражением костного мозга ионизирующим облучением и миелосупрессивными препаратами.
P.S. Усиленный распад тромбоцитов. Разрушение тромбоцитов клинически проявляется, только если оно не компенсируется образованием новых тромбоцитов. В этом случае период полураспада тромбоцитов, в том числе и вводимых при трансфузии, уменьшается до нескольких часов.
Лечение. При проявляющейся клинически склонности к кровотечениям показана трансфузия тромбоконцентрата. Трансфузия повышает количество тромбоцитов в периферической крови примерно на 50 000/мкл, после чего оно вновь снижается до исходных показателей в течение 36-72 ч. На фоне иммунотромбопении, спленомегалии или ускорения обмена веществ (например, при коагулопатии потребления или сепсисе) биологический период полураспада иногда значительно сокращается.
P.S. Снижение эффективности трансфузии. При увеличении количества вводимого при трансфузии тромбоконцентрата следует опасаться снижения эффекта из-за образования аллоантител (развитие рефрактерности). Это необходимо учитывать, если предстоят повторные трансфузии тромбоконцентрата.
Иммунотромбоцитопения развивается вследствие образования антитромбоцитарных алло- или аутоантител, которые часто бывают ассоциированы с инфекционными агентами или препаратами, но может возникать и спонтанно. Время жизни аутологичных тромбоцитов после трансфузии очень короткое. Клиническое значение имеет идиопатическая/аутоиммунная тромбоцитопеническая пурпура.
К развитию иммунотромбоцитопении может привести прием целого ряда препаратов. Тщательно собранный фармакологический анамнез, а также отмена «подозрительных» препаратов или замена их альтернативными средствами являются важнейшими диагностическими и терапевтическими мероприятиями при этом состоянии. Для получения дополнительных сведений о лечении иммунотромбоцитопении мы отсылаем читателя к руководствам по внутренним болезням.
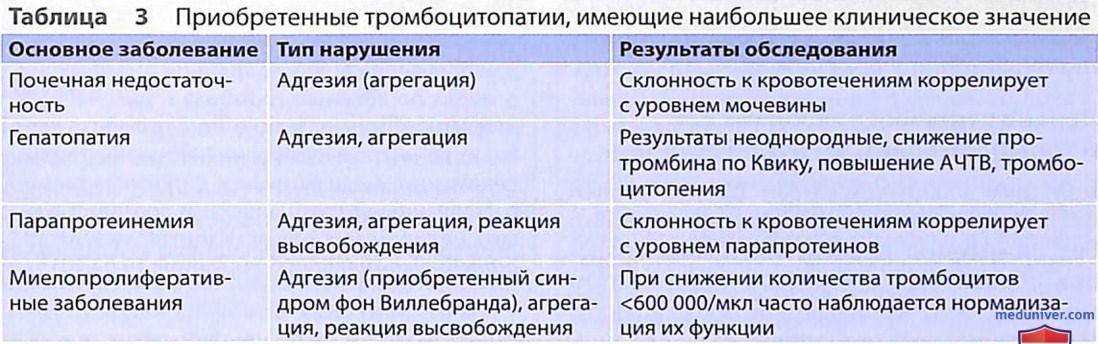

4. Тромбоцитопатия. Нарушения функции тромбоцитов и их диагностика недостаточно стандартизованы. Наследственные тромбоцитопатии характеризуются, как правило, снижением активности тромбоцитов, что клинически проявляется кровотечением тромбоцитарного типа на фоне достаточно высокого числа тромбоцитов. Приобретенные тромбоцитопатии развиваются при различных заболеваниях и патологических состояниях (табл. 3), часто в сочетании с другими нарушениями гемостаза. Значительно чаще среди них наблюдаются нарушения функции тромбоцитов, вызванные приемом препаратов (табл. 4).
Большинство препаратов, назначаемых с целью подавления функции тромбоцитов, угнетают ее на длительное время. Они повышают таким образом риск кровотечений в случае травмы и оперативного вмешательства. В качестве лечения применяют тромбоконцентрат, гемостатические препараты (см. табл. 2).
P.S. Препараты подавляют функцию тромбоцитов. Повышение концентрации в плазме лекарственных препаратов и их метаболитов подавляет функцию вводимых при трансфузии тромбоцитов и таким образом уменьшает их терапевтический эффект!
в) Тромбофильные диатезы. Триада Вирхова. Патофизиологической основой тромбогенеза является триада Вирхова:
• повреждение стенки сосуда (травма, операция, гипоксия, эндотоксины, цитокины и т.д.);
• нарушения кровотока (стаз вследствие иммобилизации, сердечной недостаточности, варикозного расширения вен, сдавления магистральных вен извне и т.д.);
• изменения состава крови (гиперкоагуляция), особенно вследствие:
- повышения прокоагулянтных факторов,
- снижения активности ингибиторов свертывания,
- подавления фибринолиза и/или
- изменения реологических свойств (при повышенной вязкости, тромбоцитозе, полиглобулии и т.д.).
1. Тромбоз глубоких вен и тромбоэмболия легочной артерии. Тромбоз глубоких вен — частое осложнение после инсульта. Обычно тромбоз возникает преимущественно в нижних конечностях, но при наличии локальных повреждающих факторов (например, катетер в центральной вене, инфильтрация опухолью) может иметь иную локализацию. Отрыв фрагментов тромба от основной его массы или от венозной стенки приводит к тромбоэмболии легочной артерии. Это состояние диагностируется с помощью соответствующих методов у 20-50% больных с тромбозом глубоких вен. однако клинические признаки выявляются менее чем у 5%.
К последствиям тромбоэмболии легочной артерии относится посттромботический синдром, который выявляется спустя 5-8 лет примерно у 1/3 больных с тромбозом глубоких вен. а также хроническая тромбоэмболическая легочная гипертензия, развивающаяся после тромбоэмболии легочной артерии в 5% случаев.
Лечение тромбоза глубоких вен и тромбоэмболии легочной артерии. Больным с клиническими проявлениями острой тромбоэмболии легочной артерии без симптомов перегрузки правых отделов сердца, как и больным с тромбозом глубоких вен, назначают антикоагулянты. При стабильной гемодинамике после подтверждения диагноза антикоагулянтную терапию начинают с назначения низкомолекулярного гепарина фондапаринукса или ривароксабана. Только в исключительных случаях (например, при тяжелой почечной недостаточности) назначают нефракциони-рованный гепарин. Больных после инсульта желательно как можно раньше активизировать. Рекомендуется также раннее применение компрессионного лечения для снижения вероятности развития посттромботического синдрома.
P.S. Практический совет. Когда и как назначать антикоагулянты
Время начала антикоагулянтной терапии и выбор антикоагулянтов при инсульте зависят от размеров и локализации очага поражения, давности инсульта и его этиологии.
Лечение тяжелой тромбоэмболии легочной артерии в остром периоде. При острой перегрузке правых отделов сердца, нестабильной гемодинамике и в условиях отделения реанимации в дополнение к интенсивной терапии следует обсудить целесообразность проведения тромболитической терапии рекомбинантным тканевым активатором плазминогена или урокиназой. При этом (особенно в отношении больных, перенесших инсульт) необходимо учитывать возможные противопоказания и осложнения, особенно опасные для жизни. В качестве альтернативы в отдельных случаях выполняют оперативное вмешательство с целью восстановления кровотока в легких, в частности эмболэктомию с применением аппарата искусственного кровообращения.
Дополнительная информация. Для получения более подробной информации о мерах по лечению тромбоза и дальнейшей вторичной профилактике при тромбозе глубоких вен и тромбоэмболии легочной артерии рекомендуем ознакомиться с руководствами, составленными специалистами соответствующих медицинских обществ на сайте МедУнивер.
2. Тромбоцитоз и повышенная функция тромбоцитов. Под тромбоцитозом понимают повышение количества тромбоцитов в периферической крови до уровня более 350 000 в 1 мкл.
В клинической практике сравнительно часто наблюдается преходящий, реактивный тромбоцитоз, в том числе при хронических воспалительных заболеваниях или злокачественных опухолях, при недостаточности железа, а также после удаления селезенки или после шока. Нередко уже само подобное заболевание, вызывающее тромбоцитоз (например, злокачественная опухоль, коллагеноз), или его лечение (например, глюкокортикоидная терапия или послеоперационная корригирующая терапия) требуют назначения средств для профилактики тромбоэмболии.
У больных с повышенным риском развития артериосклероза (например, у страдающих сахарным диабетом, нарушением жирового обмена, артериальной гипертензией и у курящих) при лабораторном исследовании выявляется повышенная функция тромбюципюв, которой придается важное патогенетическое значение в возникновении и прогрессировании артериосклероза.
Геморрагический диатез при тромбоцитозе в большинстве случаев развивается при увеличении количества тромбоцитов до I млн и более в I мкл, иногда проявляясь спонтанными желудочно-кишечными кровотечениями, но чаще провоцируется оперативным вмешательством или приемом лекарственных препаратов и антитромботической терапией.
Лечение. Целью лечения является предотвращение тромбоэмболических и геморрагических осложнений. Больным, относящимся к группе риска, для нормализации количества тромбоцитов назначают гидроксимочевину и анагрслид. Параллельно проводят симптоматическое лечение венозной тромбоэмболии антикоагулянтами, а для лечения артериальных тромбозов и эмболий назначают антиагреганты.
г) Резюме. Анамнестические данные об имевших место эпизодах кровотечения или тромбоза, о принимаемых препаратах и сопутствующих заболеваниях являются основой целенаправленной диагностики нарушений системы гемостаза и вместе с результатами полного исследования функции плазменного свертывания и определения количества тромбоцитов дают возможность проводить гемостатическую терапию и лечить тромбоэмболию.
Менее распространенные методы исследования, которые иногда необходимы для более детальной диагностики нарушений свертываемости, в ургентных ситуациях, как правило, не требуются. Учет особенностей фармакокинетики препарата, принимаемого больным или назначаемого врачом, помогает свести к минимуму как риск тромбоэмболии при лечении препаратами с прокоагулянтным свойством, так и риск кровотечения при применении антитромботических средств.
Видео показатели коагулограммы и контроль лечения, профилактики тромбозов - профессор А.Б. Добровольский
- Читать "Ювенильная миоклоническая эпилепсия. Парциальные приступы у детей"
Редактор: Искандер Милевски. Дата публикации: 13.2.2023
