Сердечно-сосудистые болезни при мышечных дистрофиях Duchenne и Becker
Сердечно-сосудистые заболевания, возникающие вторично по отношению к неврологическим нарушениям, обусловлены либо непосредственным вовлечением сердца в патологический процесс, либо нейрогуморальными изменениями, влияющими на сердце. Поражение сердечно-сосудистой системы, развивающееся у пациента на фоне неврологической патологии, иногда ассоциируется с более высоким риском заболеваемости и смертности, чем собственно неврологическое заболевание. В данной статье рассмотрены именно такие неврологические заболевания.
Мышечные дистрофии представляют собой разнородную группу заболеваний, при которых возможна различная степень непосредственного вовлечения сердечной мышцы в патологический процесс. Мышечные дистрофии, сопровождающиеся вовлечением сердечно-сосудистой системы, классифицируют следующим образом:
1. Мышечные дистрофии Duchenne и Becker.
2. Миотонические дистрофии.
3. Мышечная дистрофия Emery-Dreifuss и ассоциированные расстройства.
4. Мышечные дистрофии плечевого и тазового поясов.
5. Плече-лопаточно-лицевая мышечная дистрофия.
а) Генетика. Мышечные дистрофии Duchenne и Becker являются рецессивными заболеваниями, сцепленными с Х-хромосомой, при которых генетический дефект представляет собой нарушение в системе гена дистрофина. Белок дистрофии и дистрофин-связанные гликопротеины обеспечивают структурное взаимодействие между цитоскелетом миоцитов и внеклеточным матриксом, осуществляющим связь контрактильных белков с клеточной мембраной.
РНК дистрофина экспрессирована главным образом в скелетных мышцах, гладких мышцах, в кардиомиоцитах и, в меньшей степени, в клетках головного мозга. Отсутствие дистрофина может привести к хрупкости мембраны, что вызывает некроз миофибрилл и в конечном итоге потерю мышечной ткани с развитием фиброза. Патология дистрофина и дистрофин-ассоциированных гликопротеинов обусловливает дегенерацию сердечной и скелетных мышц при некоторых наследственных миопатиях, в т.ч. при ДКМП, сцепленной с Х-хромосомой.
Помимо наследственных заболеваний потеря дистрофина играет роль в формировании патологии миоцитов при других КМП, включая идиопатическую спорадическую КМП, вирусный миокардит, а также КМП на фоне поражения коронарных артерий. При мышечной дистрофии Duchenne дистрофии практически отсутствует, тогда как при мышечной дистрофии Becker дистрофии есть, однако его количество снижено. Это обусловливает характерное, быстро прогрессирующее поражение скелетных мышц при дистрофии Duchenne и более доброкачественное течение дистрофии Becker. Сердечная мышца поражается при обоих заболеваниях. Специфические мутации гена дистрофина ассоциируются с большей частотой КМП.
б) Клиника. Мышечная дистрофия Duchenne является самой частой наследственной формой нейромышечных заболеваний (30 случаев на 100 000 новорожденных мальчиков). Клинические симптомы обычно манифестируют в первые 5 лет жизни, проявляются прогрессирующей мышечной слабостью, которая приводит к тому, что мальчик оказывается прикованным к инвалидному креслу до достижения им 13 лет. Больные редко доживают до 25 лет и умирают от дыхательной недостаточности или, реже, СН. Применение искусственной вентиляции легких немного увеличивает выживаемость.
Мышечная дистрофия Becker встречается реже (3 случая на 100 000 новорожденных мальчиков); проявления мышечной слабости варьируют; заболевание имеет более благоприятный прогноз, большинство больных доживают до 40-50 лет.
При мышечных дистрофиях Duchenne и Becker наблюдается повышенный уровень креатинкиназы в сыворотке (выше нормы в 10 и 5 раз соответственно).
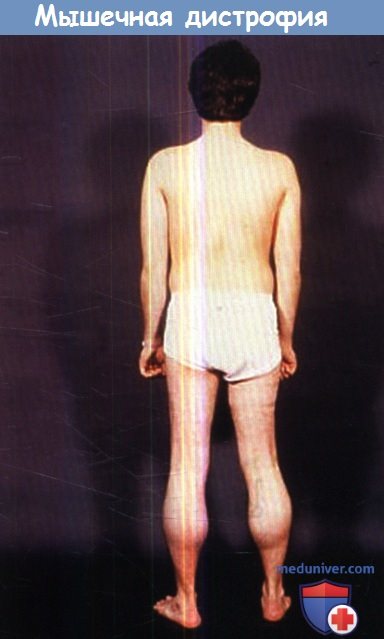
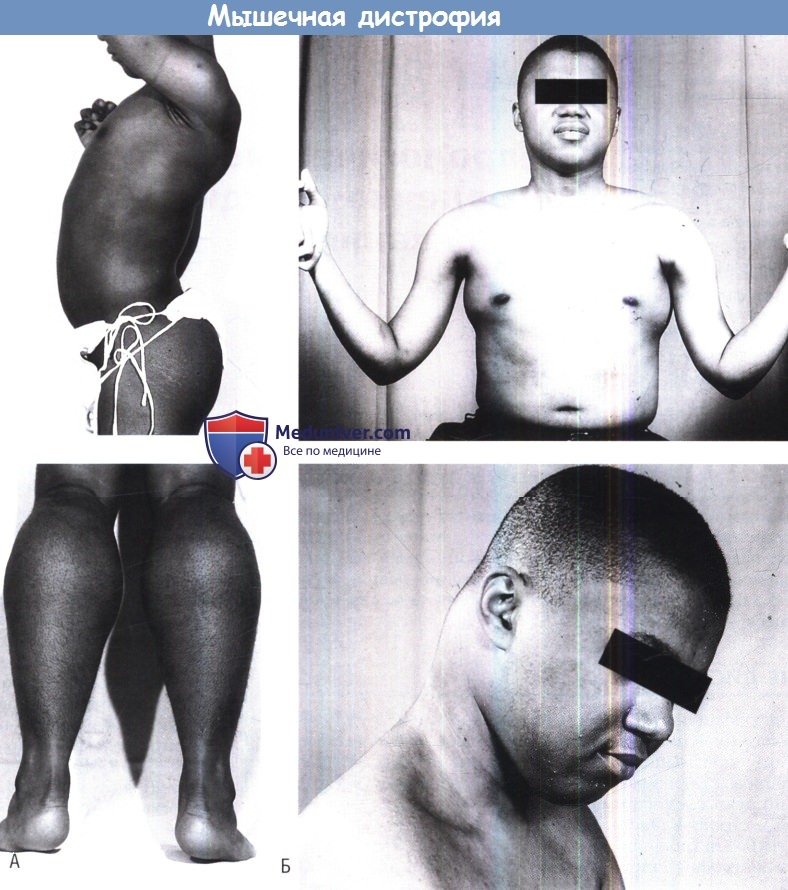
(Б) Мышечная дистрофия Duchenne у 17-летнего мужчины. Гипертрофия/псевдогипертрофия дельтовидной мышцы и большой грудной мышцы (вверху), трапециевидной мышцы (внизу) и обеих голеней (фото нет).
в) Проявления со стороны сердечно-сосудистой системы. У большинства больных с мышечной дистрофией Duchenne развивается КМП, однако клиническая картина может быть замаскирована выраженной мышечной слабостью. Поражение сердца в доклинической стадии выявляют у 25% больных в возрасте 6 лет, клинически выраженная КМП часто появляется после достижения 10-летнего возраста. Отмечается преимущественное поражение заднебазальных и заднелатеральных отделов левого желудочка. При мышечной дистрофии Becker вовлечение миокарла более вариабельно (как и поражение скелетных мышц), чем при дистрофии Duchenne.
Оно может проявляться как полным отсутствием симптомов или субклиническими признаками, так и тяжелой КМП, при которой необходима трансплантация. Степень вовлечения сердечной мышцы при мышечной дистрофии Becker не зависит от тяжести поражения скелетных мышц, при этом некоторые исследователи отмечают увеличение вероятности поражения сердца у пожилых пациентов. Более чем у 50% больных с субклиническим или доброкачественным характером поражения скелетных мышц при тщательном обследовании выявляется вовлечение сердца в патологический процесс. Поражение миокарла обычно имеет прогрессирующее течение. КМП может сначала поражать только ПЖ.
Деформации грудной клетки и высокое стояние диафрагмы могут затруднять оценку состояния сердечно-сосудистой системы при мышечной дистрофии Duchenne. Вследствие уменьшения переднезаднего размера грудной клетки отмечаются смещение сердечного толчка к левому краю грудины, появление короткого среднесистолического шума 1-3/6 степени во втором межреберье слева и громкого пульмонального компонента II тона. При мышечных дистрофиях Duchenne и Becker часто выявляют митральную регургитацию.
У женщин, являющихся носителями генов мышечных дистрофий Duchenne и Becker, отмечается повышенный риск развития ДКМП.
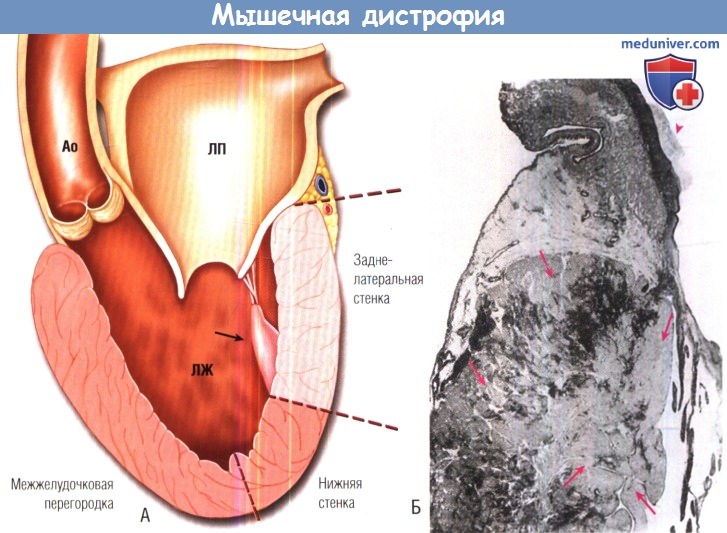
(Б) Гистологический препарат мальчика с классической мышечной дистрофией Duchenne. Видно поражение заднебазальных отделов левого желудочка (стрелки).
В процесс вовлечена заднелатеральная папиллярная мышца, что привело к митральной регургитации и повреждению, вызванному струей регургитации (острие стрелки).
Ао — аорта; ПЖ — левый желудочек; ЛП — левое предсердие.
1. Электрокардиография. У большинства пациентов с мышечной дистрофией Duchenne на ЭКГ выявляются изменения в виде высоких зубцов R характерной формы, увеличение амплитуды зубцов R/S в отведении V, и появление глубоких узких зубцов Q в левых грудных отведениях, что отражает вовлечение в патологический процесс заднелатеральных отделов ЛЖ. У больных мышечной дистрофией Becker изменения на ЭКГ выявляются приблизительно в 75% случаев: высокие зубцы R и увеличение амплитуды зубцов R/S в отведении V1 (аналогичны наблюлаемым при дистрофии Duchenne), также часто выявляется неполная БПНПГ. Последнее, возможно, обусловлено ранним поражением ПЖ. У больных с ХСН часто наблюдается БЛНПГ.
2. Аритмии. Наиболее частая форма аритмии при мышечной дистрофии Duchenne — постоянная или преходящая синусовая тахикардия. Предсердные аритмии, в т.ч. ФП и ТП, возникают главным образом на поздней стадии заболевания. Наблюдаются также нарушения АВ-проводимости, у 10% пациентов выявляется укорочение интервала PR < 120 мсек, еще у 10% — его удлинение. При суточном мониторировании у 30% больных выявляют желудочковые аритмии, в основном желудочковую экстрасистолию.
Описаны также сложные желудочковые аритмии, преимущественно у больных с тяжелым поражением скелетных мышц. При мышечной дистрофии Duchenne может наступить ВС, как правило у пациентов с терминальным поражением мышц. Неизвестно, связана ли ВС этих больных с нарушениями ритма. В нескольких наблюдательных исследованиях была обнаружена связь между ВС и сложными желудочковыми аритмиями. Однако наличие желудочковой аритмии не являлось предиктором смерти от любых причин.
Нарушения сердечного ритма при мышечной дистрофии Becker обычно связаны с тяжестью ассоциированной КМП. Наблюдаются также дистальные нарушения проводимости с развитием полной поперечной блокады и реципрокных ЖТ с блокадой ножки.
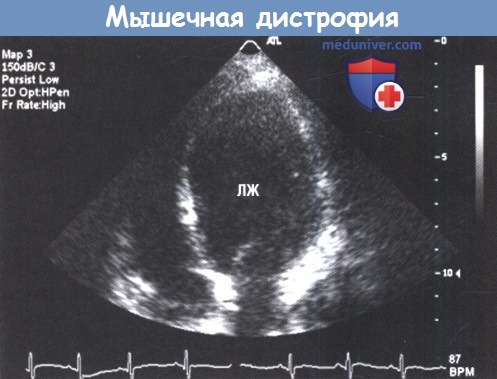
Двухмерная ЭхоКГ (парастернальная позиция, четырехкамерный вид), демонстрирующая расширенный левый желудочек (ЛЖ) с тонкими стенками.
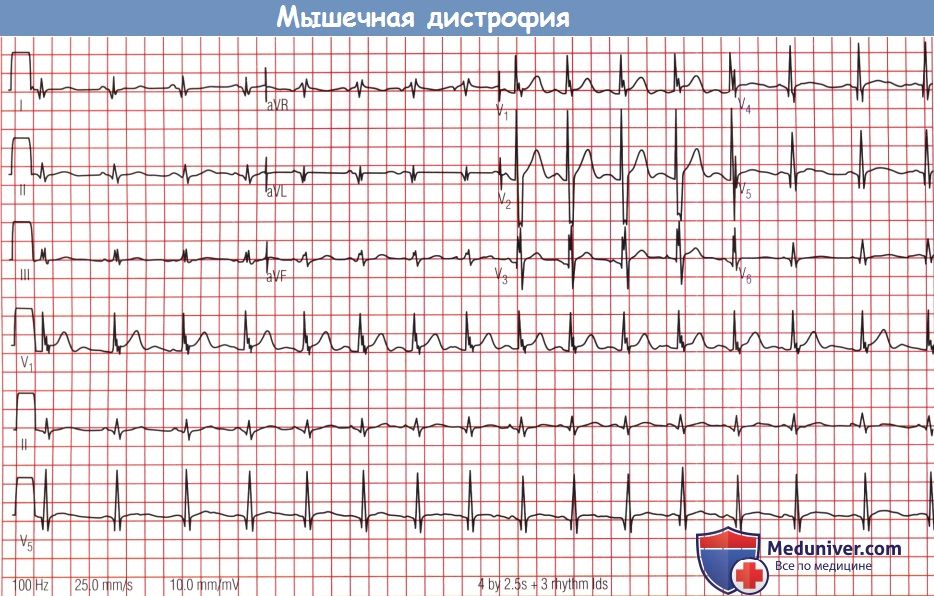
ЭКГ с типичной для дистрофии Duchenne формой комплекса QRS с высокими зубцами R в отведении V1 и глубокими узкими зубцами Q в отведениях I и aVL.
г) Лечение и прогноз. Мышечная дистрофия Duchenne является прогрессирующим заболеванием, приводящим к смерти от дыхательной недостаточности или СН.
Для замедления прогрессирования поражения мышц используют стероиды и их производные. В будущем эффективной может оказаться генная терапия. Сердечная патология служит причиной смерти 25% больных, однако значение поражения сердечно-сосудистой системы значительно больше, поскольку с дыхательными нарушениями научились бороться значительно лучше после появления искусственной вентиляции легких. ВС и смерть от СН встречаются с одинаковой частотой. Начиная с 10-летнего возраста пациентам с мышечной дистрофией Duchenne следует ежегодно оценивать сократительную функцию сердца.
В случае ранней терапии ИАПФ и β-блокаторы могут улучшить сократительную способность миокарда, но неизвестно, улучшает ли такое лечение отдаленный прогноз.
У больных с мышечной дистрофией Becker также отмечается улучшение систолической функции ЛЖ на фоне терапии ИАПФ и β-блокаторами. Скрининг для оценки сократительной способности миокарда при этом заболевании следует проводить таким же образом, как и при мышечной дистрофии Duchenne.
У женщин, являющихся носителями генов мышечных дистрофий Duchenne и Becker, КМП в детстве не развивается, поэтому скрининг следует начинать в позднем подростковом возрасте. Неясно, наступает ли улучшение у носителей этих генов на фоне терапии, уменьшающей постнагрузку, однако подобное лечение, по-видимому, оправданно, учитывая общность механизмов, лежащих в основе заболеваний. При появлении СН проводят стандартную терапию. Описаны случаи трансплантации сердца.
- Читать "Сердечно-сосудистые болезни при миотонической дистрофии"
Редактор: Искандер Милевски. Дата публикации: 26.3.2019
