Механизмы развития латентной ВИЧ-инфекции
Существуют различные гипотезы, объясняющие механизмы развития клеточного латентного состояния ВИЧ. Каждая из них может иметь отношение к определенным процессам в специфических типах клеток и к отдельным штаммам вируса.
Возникновение латентного состояния, возможно, зависит от мест интеграции вируса, в которых может существовать необходимость метилирования определенных участков интегрированной вирусной LTR для индукции процесса репликации, или метилирования экстрахромосомных последовательностей провирусной ДНК.
Это может быть связано с действием регуляторных последовательностей в некодирующих областях хромосомной ДНК или воздействием хроматина на промотер ВИЧ-1. Также могут иметь значение инактивация генов tat или rev или мутации в TAR. В одном раннем исследовании вирусные гены, ответственные за торможение в Т-клеточных линиях, обнаруживали преимущественно в области 3' LTR, но tat, rev и vpu тоже могут оказывать влияние на этот процесс.
Возможные механизмы установления латентного состояния ВИЧ:
• Место интеграции вируса
• Метилирование провирусной ДНК
• Регуляторные последовательности в некодирующих областях ДНК
• Взаимодействие хроматина с промотором ВИЧ
• Отсутствие выраженной экспрессии вирусного белка Tat
• Мутации TAR
• Отсутствие экспрессии Rev
• Супрессия экспрессии генов гистонами (действие HDAC-1)
• Недостаточность внутриклеточных факторов, взаимодействующих с фактором транскрипции NF-kB или соответствующими областями вирусной LTR
• Ингибирование факторами транскрипции человеческих клеток (YY1,LSF)
• Экспрессия вирусного белка Nef
• Отсутствие экспрессии вирусных белков Vpu и Vpr
• Блокирование функции Vpu клеткой
• Действие белка теплового шока 70 (hsp70)
• Действие Murr-1
• Блокирование ИФН-стимулирующего элемента (ISRE) в LTR ВИЧ
• Торможение экспрессии вируса анти-ВИЧ фактором CD8+-клеток (CAF)
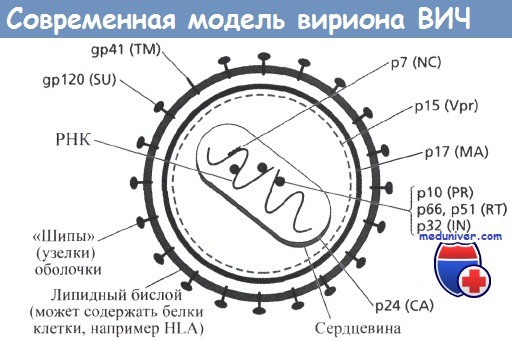
Точная локализация белков Nef и Vif, связанных с сердцевиной, до сих пор не установлена.
Использованы рекомендованные сокращения названий вирусных белков.
Может происходить подавление экспрессии генов гистонами. В этом случае ВИЧ-инфицированные CD4+-Т-клетки способны высвобождать вирус после ингибирования деацетилазы гистонов (HDAC). Латентное состояние ВИЧ в таких клетках, по-видимому, связано с влиянием на структуру хроматина, при этом «молчание» генома ВИЧ зависит от активности HDAC-1.
Таким образом, торможение HDAC и деацетил-трансфераз гистонов, что способствует повышению степени ацетилирование гистонов и других факторов транскрипции, может играть роль в усилении репликации ВИЧ. Другой механизм может быть связан с факторами транскрипции (например, YY1 и LSF) в клетках человека, которые способны ингибировать LTR ВИЧ-1 и, соответственно, продукцию дочерних вирионов.
Ранние исследования на культурах клеток показали, что сам вирус вырабатывает белок, а именно Nef, который взаимодействует с клеточными факторами и вызывает переход инфекции в скрытое состояние. Однако этот эффект, по-видимому, связан с определенными аллелями гена nef и реализуется только в определенных видах клеток.
Как отмечали выше, подавление функций белков Vpu или Vpr может приводить к развитию состояния клеточной латентности, но этот вопрос требует дальнейшего изучения.
В этом отношении показано, что Vpu способствует сборке вирусных частиц, и недавние исследования свидетельствуют, что Vpu доминирует над клеточными факторами, противодействующими высвобождению вирионов из клеток человека. Механизм его действия до конца не изучен. Кроме того, было показано, что белок теплового шока-70 (hsp70) тормозит транслокацию Vpr ВИЧ в макрофагах и может связываться с этим белком вируса.
За счет своего возможного протививирусного действия hsp70 способен уменьшать репликацию в макрофагах или даже вызывать переход инфекции в латентное состояние с помощью такого ингибиторного влияния. В случае Vpr-отрицательных вирусов hsp70 стимулирует импорт преинтеграционного комплекса ВИЧ в ядро и дальнейшую репликацию вируса.
Таким образом, эти два белка могут выполнять сходные функции, но при одновременном присутствии в клетке конкурируют между собой. В качестве дополнительного примера к описанному выше, можно привести еще продукт клеточного гена Murr-1, который тормозит репликацию ВИЧ в покоящихся CD4+-клетках. Белковый продукт этого гена блокирует активность фактора транскрипции NF-kB, чем обеспечивает переход ВИЧ в латентное состояние.
Кроме того, в некоторых случаях торможение репликации ВИЧ интерфероном-а преодолевается благодаря существованию в вирусных длинных концевых повторах (LTR) последовательностей нуклеотидов, сходных с интерферон-стимулиру-емыми элементами (ISRE). Факторы, регулирующие продукцию интерферона, способны связываться с этой областью и усиливать транскрипцию ВИЧ. Также может оказывать влияние блокировка ISRE. Наконец состояние клеточной латентности бывает связано с действием CD8-клеток, подавляющим активность ВИЧ.
Механизмы, вызывающие переход ВИЧ в латентное состояние, к настоящему времени до конца не выяснены. Причины более легкого перехода в латентное состояние некоторых штаммов вируса не известны. Кроме того, остается неясным, насколько данные о латентном состоянии вируса, полученные in vitro, соотносятся с ситуацией, наблюдаемой in vivo. Тем не менее регуляторные белки ВИЧ, Tat, Rev и Nef и определенные внутриклеточные факторы могут оказывать на этот биологический процесс положительное или отрицательное влияние.

Заместитель декана (Корнуолл) и профессор Пиринейского медицинского университета, Университет Плимута, Великобритания.
Др. Пинчинг был одним из первых врачей, разработавших программу клинического наблюдения ВИЧ-инфицированных пациентов в Европе.
- Читать "Клинически латентное состояние ВИЧ"
Оглавление темы "Инфицирование ВИЧ":- Инфицирование ВИЧ покоящихся CD4-лимфоцитов
- Инфицирование ВИЧ покоящихся CD4-эпителиальных клеток
- Клеточная латентность ВИЧ-инфекции и ее активация
- Механизмы развития латентной ВИЧ-инфекции
- Клинически латентное состояние ВИЧ
- Основные моменты теории репликации ВИЧ в клетках
- Цитопатогенные свойства ВИЧ
- Слияние клеток под действием ВИЧ - образование синцития
- Механизм слияния клеток в синцитий при ВИЧ
- Накопление вирусной ДНК ВИЧ как причина смерти клетки
