Наследственная метгемоглобинемия. Диагностика
Железо в гемоглобине обычно присутствует в двухвалентной форме (Fe2+), что имеет первостепенное значение для переноса кислорода. В физиологических условиях происходит медленная постоянная потеря электронов с высвобождаемым кислородом; трехвалентное железо (Fe3+) соединяется с водой образуя метгемоглобин (MHg). Основным внутриклеточным механизмом снижения уровня MHg является цитохром b5. По эффективности этот механизм более чем в 100 раз превышает образование MHg. и, как правило, только 1 % гемоглобина находится в трехвалентном состоянии.
Количество MHg в эритроцитах может увеличиваться под действием токсических веществ или при отсутствии восстановительных путей (дефицит НАДФ-цитохром-b5-редуктазы). Токсическая метгемоглобинемия является гораздо более частым заболеванием, чем наследственная. Дети особенно уязвимы к окислению гемоглобина, потому что уровень цитохром-b5-редуктазы у них составляет 50 % от уровня взрослого человека, HbF более чувствителен к окислению, чем НbА, а более щелочная среда ЖКТ ребенка способствует росту нитритпродуцирующих грамотрицательных бактерий.
Когда уровень MHg превышает 1,5 г/сут, появляется заметный цианоз (15 %); уровень MHg 70 % является смертельным. Уровень MHg обычно указывается в процентах от нормального гемоглобина, токсический уровень ниже при более низком уровне гемоглобина. Случаи метгемоглобинемии также описаны у младенцев, которым дают воду и пищу с высоким содержанием нитратов и анилиновые зубные гели или другие химикаты, и у некоторых младенцев с тяжелым гастроэнтеритом и ацидозом. МHg может окрашивать кровь в коричневый цвет.
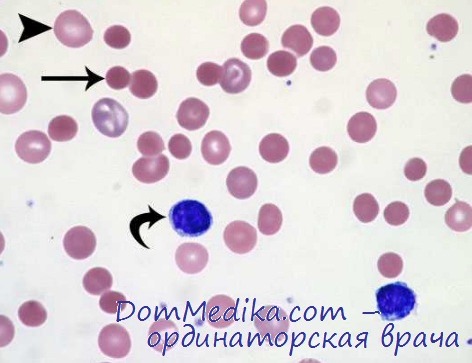
Наследственная метгемоглобинемия с дефицитом НАДФ-цитохром-b5-редуктазы. Эти редкие заболевания классифицируются по четырем типам. При 1-м типе (наиболее распространенном) дефицит активности НАДФ-цитохром-b5-редуктазы отмечается только в эритроцитах. 2-й тип характеризуется дефицитом этого фермента во всех тканях и проявляется в младенческом возрасте энцефалопатией, замедлением умственного развития, спастичностью, микроцефалией и задержкой роста. При 3-м типе данного заболевания дефицит имеет место в лейкоцитах, тромбоцитах и эритроцитах, а при 4-м типе в эритроцитах отмечается только дефицит цитохрома b5.
Интенсивность клинических проявлений цианоза меняется в зависимости от времени года и питания. Время появления цианоза также подвержено вариациям; у некоторых пациентов он проявляется с момента рождения, у других — только в подростковом возрасте. Несмотря на то что 50 % общего Циркулирующего гемоглобина может существовать в виде нефункционального MHg, у таких пациентов очень редко наблюдается кардиореспираторная недостаточность, за исключением случаев физического напряжения.
Ежедневный прием внутрь аскорбиновой кислоты (200-500 мг/сут, в несколько приемов) постепенно снижает уровень MHg до 10 % и цианоз на всем протяжении лечения. Постоянный прием аскорбиновой кислоты в высоких дозах может вызвать гипероксалурию и образование камней в почках. Аскорбиновая кислота не показана при токсической метгемоглобинемии. В данном случае используется внутривенное введение метиленового синего (начальная доза 1-2 мг/кг). В качестве поддерживающей терапии назначается прием этого средства внутрь в дозе 3-5 мг/кг/сут. Метиленовый синий не рекомендуется пациентам с дефицитом глюкозо-6-дегидрогеназы; это неэффективно и может вызвать тяжелый окислительный гемолиз.
- Читать "Синдромы персистирования фетального гемоглобина. Талассемия"
Оглавление темы "Гемоглобинопатии у детей":- Аномальные гемоглобины у детей. Диагностика
- Наследственная метгемоглобинемия. Диагностика
- Синдромы персистирования фетального гемоглобина. Талассемия
- Гомозиготная b-талассемия - анемия Кули. Диагностика
- Лечение b-талассемии - анемии Кули
- B-талассемические синдромы. Промежуточная талассемия
- Альфа-талассемия у детей. Диагностика и лечение
- Гемохромотозы у детей. Избыточное накопление железа
- Дефицит пируваткиназы у детей. Диагностика и лечение
- Анемии при ферментопатиях у детей. Недостаточность ферментов гексозомонофосфатного пути
