Строение и функции эндотелиальных клеток артерий
В эндотелиальных клетках (ЭК) артерий протекают крайне важные, тонко регулируемые процессы, обеспечивающие сосудистый гомеостаз, который часто нарушается в ходе развития заболеваний артерий. Например, ЭК интимы образуют одну из уникальных поверхностей (среди натуральных и синтетических), при длительном контакте с которой кровь остается в жидком состоянии. Это свойство крови отчасти обусловлено экспрессией на поверхности ЭК молекул протеогликана гепарансульфата.
Это соединение, подобно гепарину, служит кофактором антитромбина III и вызывает в его молекуле конформационные изменения, позволяющие этому ингибитору связываться и инактивировать тромбин. На поверхности ЭК присутствует тромбомодулин, который связывает молекулы тромбина и, активируя протеины S и С, оказывает антитромботическое действие. Если начинается образование тромба, в нормально функционирующих ЭК запускаются мощные фибринолитические механизмы.
Эндотелиальные клетки (ЭК) способны продуцировать активаторы плазминогена как тканевого, так и урокиназного типа. Эти ферменты катализируют активацию процесса образования из плазминогена фибринолитического фермента плазмина.
Все эндотелиальные клетки (ЭК) имеют общее происхождение, а в процессе развития организма приобретают характеристики, специфичные для того или иного кровеносного бассейна. ЭК, которые образуют внутреннюю поверхность всех кровеносных сосудов, в ходе эмбриогенеза развиваются из участков, локализованных на периферии эмбриона и называемых кровяными островками. В этих островках содержатся ангиобласты, т.е. предшественники ЭК, а также предшественники кроветворных клеток.
Несмотря на общее происхождение, популяцию клеток отличает значительная гетерогенность даже во время эмбрионального и раннего постнатального периода. Хотя ЭК предположительно происходят от общего предшественника, сигналы, которые они получают в процессе развития сосудов, различаются. По мере формирования рудиментарных кровеносных сосудов предшественники ЭК вступают во взаимодействие с клеточным окружением. Это взаимодействие обеспечивает постепенное (градиентное, ступенчатое) в пространстве и во времени поступление различных стимулов и их рецепторов на ЭК, результатом является гетерогенность популяции этих клеток в организме взрослого человека.
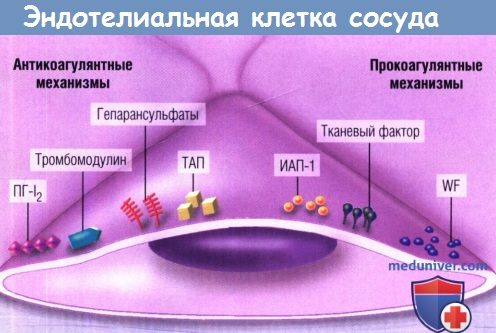
На диаграмме отражены антикоагулянтные и профибринолитические функции эндотелиальной клетки (слева) и некоторые прокоагулянтные и антифибринолитические функции (справа).
WF — фактор Willebrand; ИАП-1 — ингибитор активатора плазминогена 1;
ПГ-I2 — простациклин; ТАП — тканевый активатор плазминогена.
Гетерогенность эндотелиальных клеток (ЭК) зависит и от внешних стимулов, и от эпигенетических особенностей, приобретаемых в процессе развития.
Согласно недавно полученным данным, клетки, выстилающие различные участки артериальной стенки, в постнатальном периоде могут образовываться как из костного мозга, так и из традиционных эмбриональных источников (пуповинной крови). В частности, в периферической крови циркулируют предшественники ЭК, которые способны репарировать эндотелий в зоне десквамации. Более того, в интиме или медии поврежденных или трансплантированных артерий можно обнаружить гладкомышечные клетки (ГМК), происходящих из костного мозга.
Эндотелиальные прогениторные клетки экспрессируют специфические маркеры, в т.ч. CD133, CD34 и рецептор к сосудистому фактору роста типа 2. Количество циркулирующих эндотелиальных прогениторных клеток, согласно данным исследований in vitro, у индивидуумов варьирует. У лиц с большим числом факторов риска (ФР) атеросклероза, количество эндотелиальных прогениторных клеток меньше. У больных атеросклерозом количество эндотелиальных прогениторных клеток коррелирует с прогнозом заболевания. Чем старше человек, тем меньше у него эндотелиальных прогениторных клеток и, следовательно, способность восстановить нарушения целостности интимы ниже.
Дифференциальная экспрессия генов в эндотелиальные клетки (ЭК) различных типов кровеносных сосудов зависит от регуляции процесса транскрипции локальным окружением. Например, промоторный участок гена, кодирующего фактор Willebrand, контролирует его экспрессию в ЭК капилляров мозга и сердца, но не крупных артерий.
Избирательную активацию промотора гена фактора Willebrand наблюдали только при совместном культивировании ЭК с кардиомиоцитами (КМЦ), но не с другими клетками. Аналогично регуляция активности гена эндотелиальной синтазы оксида азота (eNOS) в сердце зависит от сосудистого ложа. В процессе развития организма в ЭК артерий (по сравнению с венами) обнаруживают гетерогенность экспрессии Eph-рецепторов тирозинкиназы и их лигандов, известных под названием «эфрины».
У взрослых людей эфрин-В2 экспрессируется в эндотелиальные клетки (ЭК) и ГМК артерий, но не вен. Эти данные свидетельствуют в пользу стабильных различий в происхождении клеток, образующих артерии и вены. Подобные примеры иллюстрируют разнообразие локализации клеток в сосудистом русле па молекулярном уровне. Применение фагов и методов протеомики позволило в условиях in vivo получить доказательства значимости гетерогенности популяции клеток сосудистой стенки в атерогенезе.
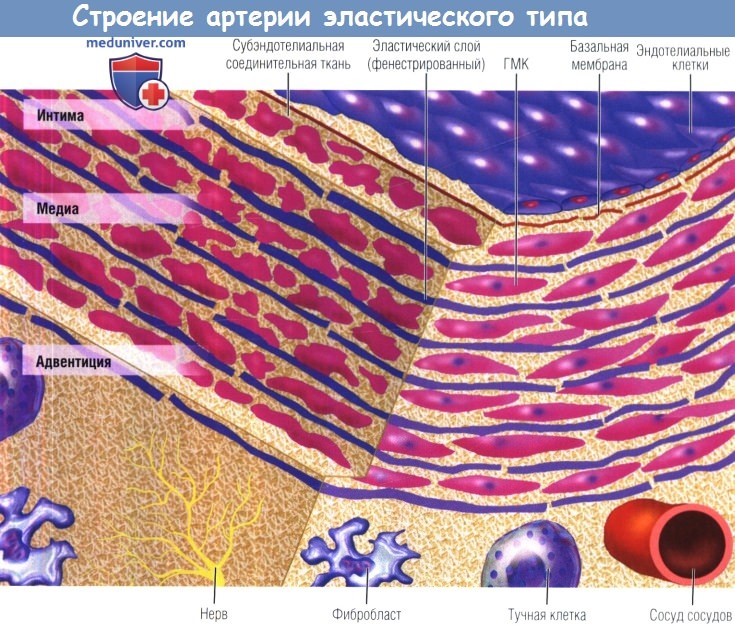
Видны концентрические слои эластической ткани, формирующей сэндвичи из чередующихся слоев гладкомышечных клеток (ГМК).
Для эластических артерий разного калибра характерно определенное количество эластических слоев.
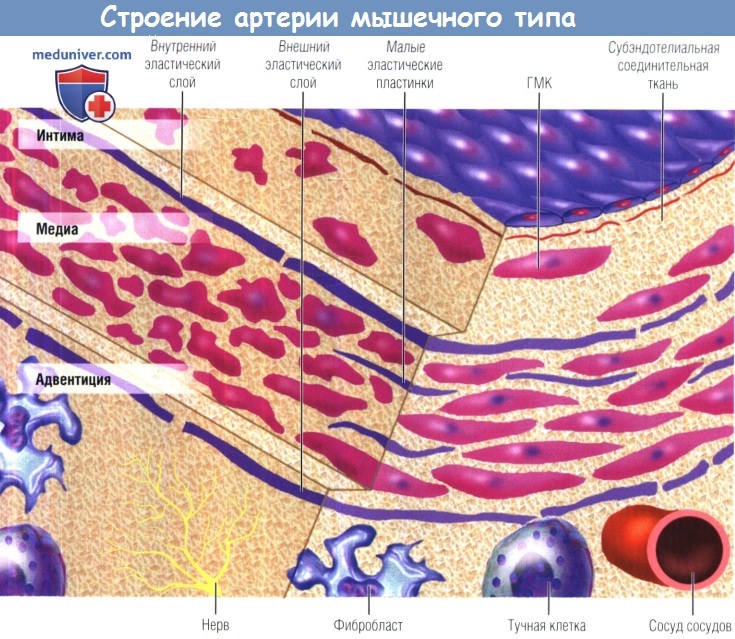
В мышечной артерии ГМК окружены коллагеновым матриксом, но отсутствуют концентрические кольца,
образуемые хорошо организованной эластической тканью, характерной для магистральных артерий.
- Читать "Строение и функции гладкомышечных клеток артерий"
Оглавление темы "Атеросклероз":- Принципы лечения обмороков (синкопе, потери сознания)
- История изучения атеросклероза артерий
- Строение и функции эндотелиальных клеток артерий
- Строение и функции гладкомышечных клеток артерий
- Строение и функции интимы артерии
- Строение, функции медиа и адвентиции артерии
- Механизмы внеклеточного накопления липидов при атеросклерозе
- Механизмы захвата лейкоцитов при атеросклерозе
- Механизмы очагового накопления липидов при атеросклерозе
- Механизмы образования пенистых клеток при атеросклерозе
