Механизмы очагового накопления липидов при атеросклерозе
Попытка объяснить пространственную гетерогенность атеросклероза с механистических позиций сталкивается с определенными противоречиями. Действительно, в кровотоке циркулируют соединения, изменение содержания которых считается ФР атеросклероза, например липопротеины, и которые в одной и той же концентрации контактируют с эндотелием на протяжении всего сосудистого русла.
Трудно себе представить, каким образом повреждение, вызываемое вдыханием сигаретного дыма, способно вызывать какой-то локальный эффект, а не оказывать общее воздействие на артерии. К тому же, как было показано в исследованиях по изучению морфологии накопления липидов и экспрессии молекул адгезии, формирование атеромы обычно носит очаговый характер.
Некоторые исследователи придерживаются мультицентрической гипотезы атерогенеза, утверждая, что атерома возникает в виде доброкачественной лейомиомы артериальной стенки. В пользу этой «моноклональной гипотезы» атерогенеза свидетельствует обнаружение в индивидуальных (отдельных) АБ различных молекулярных маркеров лишь одного типа (монотипия), например изоферментов глюкозо-6-фосфатдегидрогеназы.
В то же время локализация зон, предрасположенных к формированию повреждения, именно в проксимальных участках артерий ниже мест их разветвления и зон бифуркации дает основание предполагать гидродинамическую основу развития ранних поражений. Артерии, не имеющие многочисленных ответвлений (например, внутренние грудные или лучевые), менее подвержены развитию атеросклероза.
Рассмотрев обе концепции, можно попытаться понять, каким образом локальные нарушения потока крови связаны с повышенной склонностью определенных участков сосудистого русла к формированию атеросклеротических поражений. Локальное нарушение кровотока индуцирует изменения, инициирующие ранние этапы атерогенеза.
В противоположность этому при ламинарном потоке, который преобладает в зонах, менее подверженных раннему развитию атеросклеротических поражений, активизируются антиатерогенные механизмы поддержания гомеостаза (атеропротективная функция). В зонах с нормальным кровотоком ЭК подвергаются действию ламинарного напряжения сдвига, а в участках, склонных к атеросклерозу, — действию нарушенного потока (в котором напряжение сдвига обычно снижено).
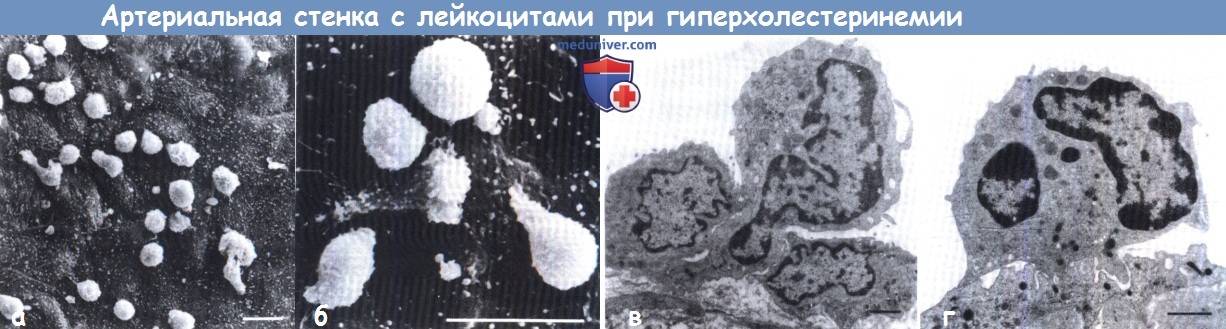
(А) и (Б) Микрофотографии, полученные с помощью сканирующей электронной микроскопии,
на которых видна адгезия мононуклеарных фагоцитов на интактном эндотелии через 12 сут от начала скармливания животным гиперхолестеринемической диеты.
(В) и (Г) Микрофотографии, полученные с помощью трансмиссионной электронной микроскопии.
(В) Видны множественные участки тесного примыкания моноцитов к эндотелию.
(Г) Моноцит, похоже, путем диапедеза просачивается между двумя эндотелиальными клетками, чтобы попасть в интиму.
Согласно данным исследований in vitro, напряжение сдвига ламинарного потока крови усиливает экспрессию генов, способных противостоять развитию атеросклероза, в т.ч. кодирующих различные формы таких ферментов, как супероксиддисмутаза или синтаза оксида азота. Супероксиддисмутаза, катаболизируя активный губительный супероксид, снижает степень окислительного стресса. eNOS продуцирует хорошо известный эндогенный вазодилататор — оксид азота (NO).
Помимо вазодилатирующего действия NO способен противостоять провоспалительной активности сосудистого эндотелия, например снижать экспрессию VCAM-1. Полагают, что NO осуществляет свое антивоспалительное действие на уровне экспрессии генов, взаимодействуя с регулятором транскрипции нуклеарным фактором каппа В (NFkB). На самом деле NO усиливает продукцию IкВα, который служит внутриклеточным ингибитором этого важнейшего фактора транскрипции. NFkB регулирует активность многих генов, вовлеченных в воспалительную реакцию как в целом, так и при атерогенезе в частности.
Согласно проведенным недавно исследованиям, еще один фактор транскрипции KLF2 (Krupple-like factor 2) (назван так из-за гомологии с регуляторным белком дрозофилы Krupple) рассматривают как важный регулятор антивоспалительных свойств эндотелия. KLF2 способен индуцировать экспрессию eNOS, а также угнетать функцию NFkB за счет секвестрирования (изоляции, связывания) кофакторов, необходимых для усиления транскрипционной активности NFkB; в результате ингибируется экспрессия кассетных NFKB-зависимых генов, вовлеченных в регуляцию воспалительных процессов, протекающих в ходе атерогенеза.
Напряжение сдвига при ламинарном потоке ограничивает экспрессию еще одного регулятора функциональной активности эндотелия, а именно тиоредоксин-взаимодействующего протеина (Txnip). Txnip ингибирует действие тиоредоксина (низкомолекулярного многофункционального тиолсодержащего белкового фактора).
Повышенный уровень тиоредоксина в зонах, где действует напряжение сдвига ламинарного потока, обусловленный сниженным уровнем Txnip, усиливает, в свою очередь, активность апоптоз-сигналрегулируемой киназы 1, которая служит активатором митоген-активированных киназ — Jun-N-терминальной киназы (JNK) и р38. Этот метаболический каскад ослабляет активацию JNK и р38 провосгталительными цитокинами, включая фактор некроза опухоли (ФНО). Иными словами, в нормальных артериях в условиях обычного для ламинарного потока напряжения сдвига функционирует целый ряд атеропротективных механизмов, которые и обеспечивают зависимое от тонуса локальное проявление эндотелием антивоспалительных свойств.
Приведенные примеры демонстрируют, как достижения фундаментальной сосудистой биологии позволяют пролить свет на ранее неизвестные, но крайне важные аспекты атерогенеза. Дальнейшие исследования в области изучения молекулярной регуляции функционирования клеток сосудистой стенки посредством механических стимулов должны прояснить механизмы формирования атеросклеротического поражения в определенных бассейнах сосудистого русла.
Аналогично исследования в области биологии развития позволят понять, чем обусловлена различная склонность разных артерий к развитию атеросклероза с разной скоростью и различными путями. Как было отмечено ранее, ГМК в различных регионах кровяного русла варьируют по своему происхождению в эмбриогенезе. Например, в ходе развития артерий верхних отделов тела ГМК захватываются из нейроэктодермы, тогда как ГМК сосудов нижних отделов тела происходят только из мезодермы.
Гладкомышечные клетки коронарных артерий (ГМК КА) происходят из зачатка, называемого проэпикардиальным органом. После повреждения или процедуры трансплантации в артерии могут попасть ГМК, происходящие из костного мозга. Ответы на вопросы о том, каким образом подобная гетерогенность в происхождении ГМК способна повлиять на развитие атеросклероза у человека и как с ее помощью можно объяснить некоторые, не до конца понятные факты, касающиеся неравномерности появления АБ во времени и пространстве, остаются во многом гипотетическими.
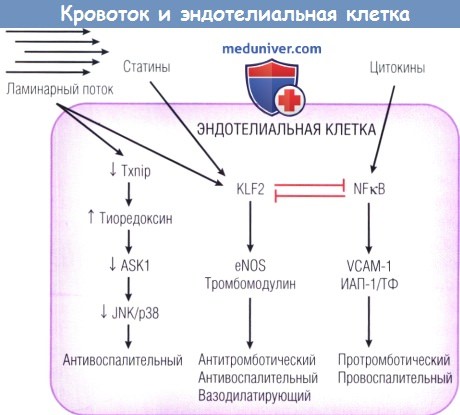
Под действием напряжения сдвига, обусловленного ламинарным потоком крови, активируется фактор транскрипции KLF2 (Krupple-like factor 2),
который, в свою очередь, активирует эндотелиальную синтазу оксида азота (eNOS); этот фермент продуцирует оксид азота, а также тромбомодулин, обеспечивающие последующие антивоспалительный и антитромботический эффекты.
Конкурируя за коактиваторы нуклеарного фактора каппа В (NFkB), активированный KLF2 угнетает провоспалительный,
протромботический и антифибринолитический эффекты последнего, которые опосредуются молекулами адгезии, включая молекулу адгезии сосудистых клеток 1 (VCAM-1),
ингибитором активатора плазминогена 1 (ИАП-1) и прокоагулянтным тканевым фактором (ТФ). При ламинарном потоке активируется и тиоредоксин-взаимодействующий протеин (Txnip),
который, в свою очередь, усиливает функцию тиоредоксина, угнетая активность апоптоз-сигналрегулируемой киназы 1 (ASK1) и, следовательно,
подавляя активность Jun-N-терминальной киназы (JNK) и киназы р38, приводя в результате к уменьшению воспаления.
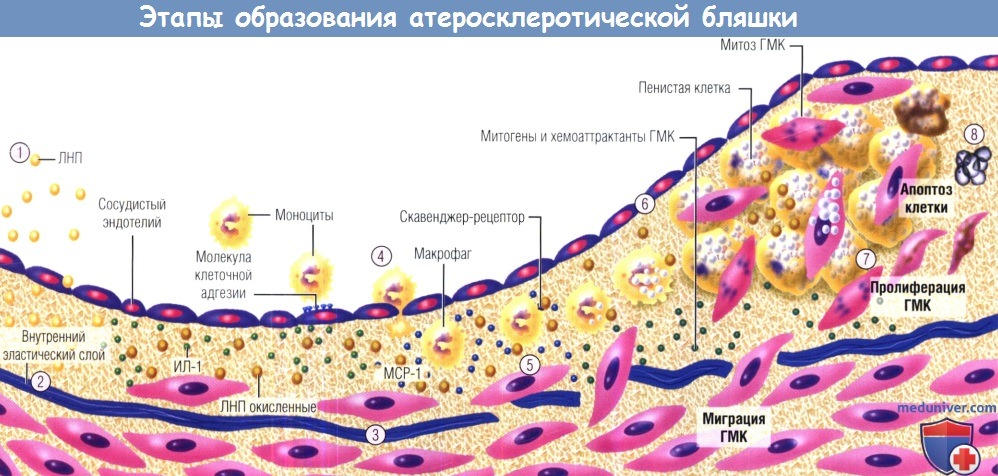
Этап 1: накопление части липопротеинов в интиме; модифицированные липопротеины показаны более темным цветом, модификация — окисление и гликозилирование.
Этап 2: соединения, вызывающие окислительный стресс, включая модифицированные липопротеины, индуцируют локальную продукцию цитокинов.
Этап 3: цитокины, в свою очередь, индуцируют повышенную экспрессию молекул адгезии лейкоцитов, посредством которых последние прикрепляются к эндотелию, и хемоаттрактантов, которые обеспечивают их миграцию в интиму.
Этап 4: моноциты крови, попадающие в артериальную стенку за счет взаимодействия с цитокинами-хемоаттрактантами (например, МСР-1),
получают стимулы (например, от макрофагального колониестимулирующего фактора), усиливающие экспрессию ими скавенджер-рецепторов.
Этап 5: скавенджер-рецепторы опосредуют захват модифицированных липопротеинов и ускоряют образование пенистых клеток.
Образовавшиеся из макрофагов пенистые клетки служат источником медиаторов, включая другие цитокины и эффекторные молекулы, такие как гипохлорная кислота, супероксид (O2-) и матриксные металлопротеиназы.
Этап 6: ГМК интимы делятся, другие ГМК мигрируют из медии в интиму.
Этап 7: ГМК делятся и продуцируют внеклеточный матрикс, способствуя тем самым его накоплению в растущей атеросклеротической бляшке. В такой ситуации липидная полоса превращается в фиброзно-жировое отложение.
Этап 8: на последних этапах происходит кальцификация (не показана) и продолжается фиброз, сопровождаемый иногда гибелью ГМК (в т.ч. путем апоптоза).
В результате формируется почти бесклеточная фиброзная покрышка, окружающая богатое липидами ядро, в котором также могут содержаться гибнущие или мертвые клетки и их детрит (продукт их распада).
МСР-1 — моноритарный хемоаттрактантный белок 1; ГМК — гладкомышечные клетки; ИЛ-1 — интерлейкин 1; ЛНП — липопротеины низкой плотности.
Видео механизм развития атеросклероза (патогенез)
- Читать "Механизмы образования пенистых клеток при атеросклерозе"
Оглавление темы "Атеросклероз":- Принципы лечения обмороков (синкопе, потери сознания)
- История изучения атеросклероза артерий
- Строение и функции эндотелиальных клеток артерий
- Строение и функции гладкомышечных клеток артерий
- Строение и функции интимы артерии
- Строение, функции медиа и адвентиции артерии
- Механизмы внеклеточного накопления липидов при атеросклерозе
- Механизмы захвата лейкоцитов при атеросклерозе
- Механизмы очагового накопления липидов при атеросклерозе
- Механизмы образования пенистых клеток при атеросклерозе
