Неврологические проявления заболеваний надпочечников
а) Анатомия и физиология. Надпочечники — это две небольшие структуры, расположенные на верхнем полюсе обеих почек. Функционально их можно разделить на две области: кору и мозговое вещество.
Кора надпочечников имеет мезодермальное происхождение и состоит из трех областей, которые синтезируют три различных типа гормонов: клубочковая зона, вырабатывающая минералокортикоиды; пучковая зона, вырабатывающая ГКС; сетчатая зона, вырабатывающая андрогены. Секреция гормонов клубочковой зоны контролируется ренин-ангиотензиновой системой, тогда как две другие области регулируются гипоталамо-гипофизарной системой.
Мозговое вещество надпочечников имеет нейроэктодермальное происхождение. Его основная функция — высвобождение катехоламинов (адреналина, норадреналина и дофамина), которые контролируются вегетативной нервной системой.
б) Типы поражения. Неврологические синдромы, связанные с нарушениями функции надпочечников, в первую очередь вызваны гормональной гипо- или гиперфункцией (Bertorini и Perez, 2014). Нарушения со стороны надпочечников, наиболее часто ассоциированные с неврологическими симптомами, включают опухоли (например, феохромоцитому), избыток гормонов (например, при синдроме Кушинга), деструктивные поражения надпочечников (например, болезнь Аддисона) и определенные генетические состояния (например, адренолейкодистрофия).
в) Неврологические проявления заболеваний надпочечников:
1. Синдром Кушинга. Синдром Кушинга развивается при длительном воздействии высоких уровней эндогенных или экзогенных ГКС на организм. Наиболее частыми причинами являются лечение ГКС или АКТГ, а также аномальная секреция ГКС аденомами гипофиза или надпочечников. Наиболее частыми неврологическими проявлениями синдрома Кушинга являются психиатрические симптомы и миопатия.
Пациенты нередко проявляют беспокойство и раздражительность, страдают бессонницей и даже психозом. Миопатия характеризуется незаметно прогрессирующей слабостью проксимальных мышц (особенно в ногах), иногда сопровождающейся атрофией (Katzberg и Kassardjian, 2016; Orrell, 2007). Уровни мышечных ферментов обычно находятся в пределах нормального диапазона.
По данным ЭМГ — норма или незначительные миопатические изменения. У прикованных к постели пациентов, которые подвергаются воздействию высоких уровней ГКС и страдают недоеданием, миопатия может протекать более агрессивно. Это заболевание известно как миопатия критических состояний. Было высказано предположение, что оно с большей вероятностью развивается у пациентов, которые получали седативные препараты и/или нервно-мышечные блокаторы в течение длительного времени.
Миопатия, сопровождающаяся отложением жира (лунообразное лицо, центральное ожирение) и кожными проявлениями (стрии, хрупкость кожи), должна вызывать клиническое подозрение на синдром Кушинга.
Диагностика проводится на основании определения уровня свободного кортизола в моче (Loriaux, 2017). Диагностика не основывается только на определении уровня кортизола в плазме крови, поскольку при синдроме Кушинга исчезает циркадный ритм секреции этого гормона, и его уровень в плазме может быть нормальным. Также важно знать уровень АКТГ, чтобы определить, является ли синдром Кушинга АКТГ-зависимым. АКТГ-секретирующую аденому гипофиза можно диагностировать с помощью МРТ головного мозга с гадолинием. Для визуализации надпочечников необходимо проведение КТ или МРТ.
2. Феохромоцитома. Феохромоцитома — это нейроэндокринная опухоль надпочечников, которая секретирует большое количество катехоламинов. Самый частый неврологический симптом — головная боль. Согласно Международной классификации головных болей (2013), головная боль при феохромоцитоме возникает приступообразно на фоне резкого повышения артериального давления. Боль часто бывает сильной, локализуется в лобной или затылочной области и обычно описывается как пульсирующая или постоянная.
Важной особенностью головной боли является ее малая продолжительность, обычно менее 1 ч. Головная боль обычно сопровождается потоотделением, сердцебиением, бледностью и беспокойством. Другие ассоциированные признаки включают чувство страха и/или тревоги, часто с ощущением приближающейся смерти, тремор, нарушения зрения, боль в животе или груди, тошноту, рвоту и иногда парестезию. В Международной классификации головных болей указано, что головная боль может сопровождаться бледностью или покраснением лица во время приступа.
Диагноз феохромоцитомы устанавливается на основании однократного определения повышенной экскреции катехоламинов или метанефринов в суточной моче. Важно отметить, что феохромоцитомы могут быть ассоциированы с несколькими различными заболеваниями, особенно с нейрокутанными расстройствами. К ним относятся болезнь фон Гиппеля-Линдау, нейрофиброматоз 1-го типа, атаксия-телеангиэктазия, туберозный склероз и синдром Стерджа—Вебера.
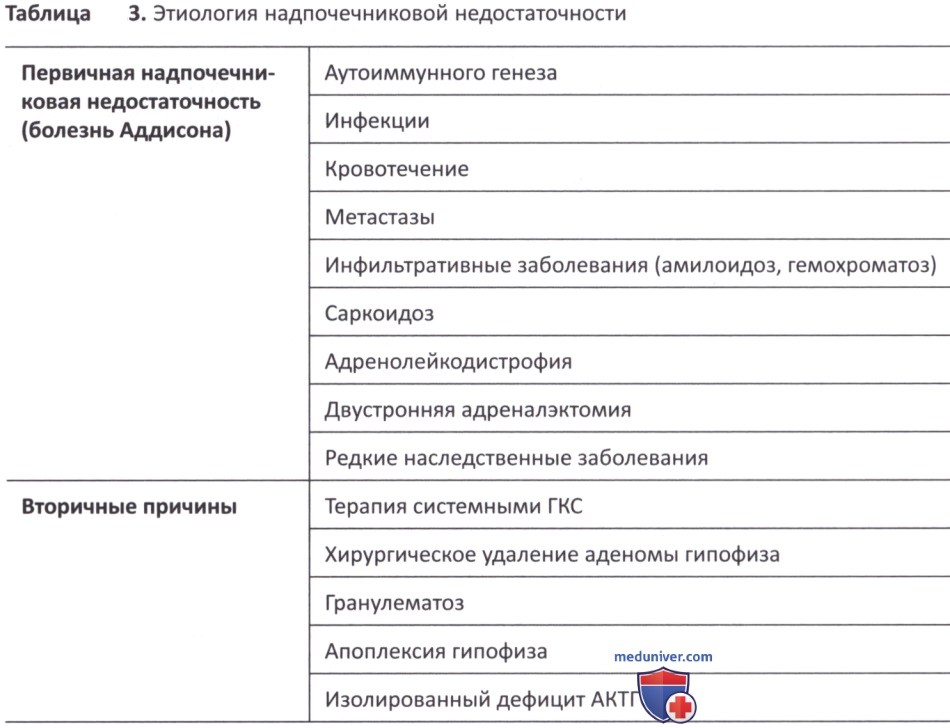
3. Надпочечниковая недостаточность. Надпочечниковая недостаточность возникает в случае недостаточной выработки ГКС (кортизол), минералокортикоидов (альдостерон) или андрогенов. В клинической практике различают два различных типа надпочечниковой недостаточности: первичную и вторичную (табл. 3). Первичная надпочечниковая недостаточность, или болезнь Аддисона, возникает, когда надпочечники не могут производить достаточное количество гормонов, несмотря на нормальный уровень АКТГ. Вторичная надпочечниковая недостаточность возникает вследствие недостаточной секреции АКТГ гипофизом.
В обоих случаях пациенты испытывают симптомы дефицита кортикостероидов, такие как общая мышечная слабость и утомляемость. Другие проявления надпочечниковой недостаточности включают спутанность сознания, психиатрические симптомы (депрессию и психоз), тошноту и боль в животе. Наличие гиперпигментации кожи, особенно на лице, шее и тыльной стороне рук, может возникать при болезни Аддисона, но отсутствует при вторичной надпочечниковой недостаточности (Bertorini и Perez, 2014). Адреналовый криз — потенциально смертельное состояние, связанное с острым дефицитом кортизола.
Симптомы включают боль в животе, рвоту, спутанность сознания при низком артериальном давлении и кому. Криз может развиваться при наличии инфекции, после тяжелой травмы головы или позвоночника или после резкой отмены стероидов у пациентов, длительно принимающих глюкокортикоидные препараты.
Первичная надпочечниковая недостаточность может также включать нарушение выработки альдостерона. Гипокалиемия, развивающаяся при гипоальдостеронизме, может вызывать утомляемость и общую мышечную слабость.
4. Адренолейкодистрофия (комплекс адренолейкодистрофия-адреномиелонейропатия). Адренолейкодистрофия — это Х-сцепленное пероксисомное заболевание, характеризующееся недостаточностью окисления жирных кислот с очень длинной цепью. Нарушение вызвано мутацией гена ALD, кодирующего белок ABCD1, который переносит жирные кислоты с очень длинной цепью в пероксисомы, где они подвергаются β-окислению (Bertorini и Perez, 2014). Симптомы адренолейкодистрофии вторичны по отношению к накоплению этих жирных кислот в нервной системе и надпочечниках.
Типичные неврологические симптомы включают когнитивные и зрительные нарушения, нарушения походки (из-за поражения мозжечка) и пирамидные симптомы (мышечная слабость, спастичность). При адреномиелонейропатии поражается спинной мозг, что приводит к развитию прогрессирующего спастического парапареза. Другие подозрительные клинические симптомы включают гиперпигментацию кожи или слизистых оболочек и ломкость волос.
Характерные поражения, наблюдаемые при этом состоянии, влияют на белое вещество головного мозга (особенно в теменно-затылочной области) и приводят к дегенерации аксонов длинных трактов спинного мозга.
Диагноз может быть поставлен на основе анализов крови на жирные кислоты с очень длинной цепью и подтвержден данными генетического тестирования. Исследование спинномозговой жидкости показывает повышение уровня белка и присутствие олигоклональных полос. МРТ головного мозга выявляет демиелинизирующие поражения белого вещества, преимущественно в теменно-затылочных областях и валике мозолистого тела. Аномалии также могут быть обнаружены с помощью зрительных и/или соматосенсорных вызванных потенциалов и исследования нервной проводимости, в зависимости от конкретного случая.
Лечение включает коррекцию надпочечниковой недостаточности при ее наличии. Диетотерапия (например, масло Лоренцо) не показала свою эффективность в снижении уровня жирных кислот с очень длинной цепью, за исключением очень ранних стадий заболевания, до появления симптомов. Масло Лоренцо обычно рекомендуется детям младше 8 лет с бессимптомным течением и отсутствием изменений на МРТ головного мозга (Bertorini и Perez, 2014). В некоторых случаях также возможна пересадка костного мозга.
Видео физиология гормонов надпочечника - профессор, д.м.н. П.Е. Умрюхин
- Читать "Неврологические проявления заболеваний околощитовидных желез"
Редактор: Искандер Милевски. Дата публикации: 7.2.2023
- Неврологические проявления заболеваний гипофиза
- Неврологические проявления заболеваний щитовидной железы
- Неврологические проявления заболеваний надпочечников
- Неврологические проявления заболеваний околощитовидных желез
- Неврологические проявления заболеваний половых желез
- Неврологические проявления ожирения
- Неврологические проявления сахарного диабета
- Психиатрические проявления эндокринных заболеваний
- Психиатрические проявления заболеваний гипофиза
- Психиатрические проявления заболеваний половых желез
