Каскад коагуляции (факторы и схема системы коагуляции)
Факторы коагуляции в плазме крови в норме циркулируют в виде биологически неактивных форм (проферментов). В случае механического повреждения или воздействия любого системного фактора (например, воспалительной природы), приводящего к нарушению антитромботических свойств сосудов, происходит активация свертывающей системы. Если при этом идет подавление антикоагулянтных механизмов, результатом будет образование тромбов, состоящих из тромбоцитов и фибрина.
Если активация свертывающей системы вызвана местным повреждением сосуда, тромб локализуется в месте поражения.
Последовательность реакций с участием факторов коагуляции в плазме, приводящих к образованию фибрина, традиционно описывают как каскад коагуляции. Каскад коагуляции представляет собой последовательность четко скоординированных и регулируемых ферментативных реакций с последовательной активацией проферментов в плазме и образованием сериновых протеаз. Каждая протеаза катализирует последующий процесс превращения профермента в протеазу, расщепляя пептидные связи. В результате этих реакций незначительный исходный стимул приводит к образованию большого количества конечного продукта — фибрина.
Каскад коагуляции на самом деле включает ряд связанных белковых комплексов, каждый из которых состоит из сериновых протеаз, одного или нескольких кофакторных белков, двухвалентных катионов и клеточной поверхности (например, мембраны тромбоцитов), которая объединяет все эти компоненты.
Существуют два пути активации свертывающей системы: (1) внешний, или тканевый; (2) внутренний, или контактный. Эти два пути активации каскада коагуляции сходятся в одной точке и в итоге приводят к образованию главного фермента свертывающей системы — тромбина. Тромбин не только катализирует превращение фибриногена в фибрин, но и поддерживает весь процесс, активируя факторы коагуляции по механизму обратной связи на различных этапах.
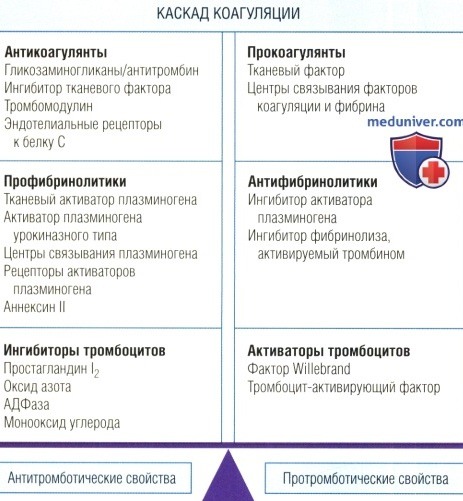
Как правило, в нормальных физиологических условиях преобладают антитромботические свойства.
Если клетки эндотелия повреждены или активированы, преобладают протромботические свойства.
АДФаза — аденозиндифосфатаза.
а) Внешний путь каскада коагуляции. Внешний (тканевый) путь, по-види-мому, запускает каскад коагуляции in vivo. В ответ на повреждение экспрессируется мембранный гликопротеин тканевого фактора на поверхности активированных клеток эндотелия и клеток крови (в частности, лейкоцитов), которые в норме его не экспрессируют. Точно так же при повреждении сосуда клетки крови начинают контактировать с тканевым фактором, экспрессированным на поверхности эндотелиальных, гладкомышечных клеток или макрофагов.
Сериновая протеаза, или фактор VIIa (активная форма фактора VII), в небольшом количестве циркулирует в крови, но ее свободная форма обладает очень низкой ферментативной активностью. Контакт крови с тканевым фактором активирует процесс коагуляции за счет связывания свободной формы фактора VIIa. Комплекс тканевый фактор-фактор VIIa ускоряет процесс превращения фактора VII в активную форму, что, в свою очередь, ведет к увеличению числа комплексов тканевый фактор-фактор VIIa, еще больше ускоряя начальный этап коагуляции.
Активацию фактора VII также вызывают фактор Ха и тромбин, причем эти два фермента являются более мощными активаторами фактора VII, чем комплекс тканевый фактор-фактор VIIa.
Конечной реакцией внешнего пути является активация фактора X с образованием его активной формы — фактора Ха. Этот этап может напрямую катализироваться бимолекулярным комплексом тканевый фактор-фактор VIIa. Кроме того, этот комплекс может вызывать активацию фактора X опосредованно, конвертируя фактор IX в фактор ШХа (обеспечивая взаимодействие между внешним и внутренним путями активации свертывающей системы), который затем активирует фактор X. С точки зрения кинетики непрямой путь активации фактора X, по-видимому, является предпочтительным.
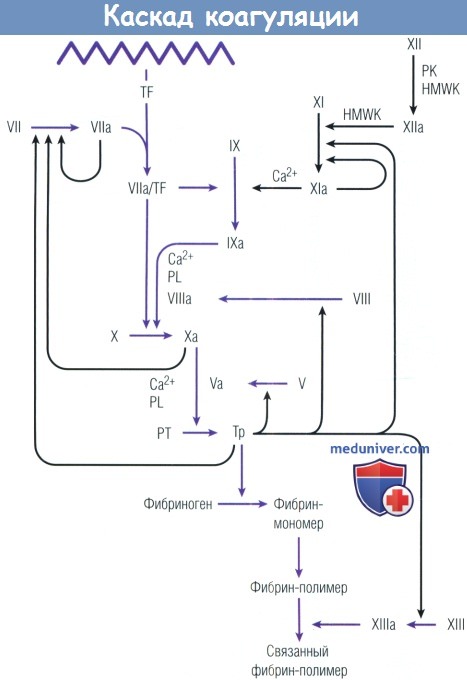
Данная схема подчеркивает значение тканевого пути свертывания in vivo, взаимодействие между путями, а также ключевую роль тромбина в развитии каскада коагуляции за счет активации факторов коагуляции по механизму обратной связи.
HMWK — высокомолекулярный кининоген; РК — прекалликреин; PL — фосфолипид; РТ — протромбин; TF — тканевый фактор; Тр — тромбин.
б) Внутренний путь каскада коагуляции. Внутренний (контактный) путь запускается аутоактивацией фактора XII до его активной формы (фактора ХIIа) на отрицательно заряженной поверхности в присутствии двух других белков, обеспечивающих активацию: прекалликреина и высокомолекулярного кининогена. В физиологических условиях внутренний путь в настоящее время не выявлен. Однако этот путь важен для активации коагуляции in vitro и знание его крайне важно для интерпретации лабораторных данных. При внутренней активации фактор ХПа конвертирует фактор XI в активную форму (ХIа), которая, в свою очередь, активирует фактор IX с образованием фактора IХа.
На заключительном этапе внутреннего пути фактор IХа активирует фактор X до активной формы (Ха). Для этой реакции необходимо присутствие активированной формы кофактора VIII (VIIIa), которая образуется путем протеолиза из фактора VIII под действием тромбина.
Наиболее убедительным доказательством того, что каскад коагуляции не запускается по внутреннему пути, является тот факт, что у лиц с врожденным дефицитом факторов активации внутреннего пути (например, фактора XII, прекалликреина и высокомолекулярного кининогена) кровоточивость не наблюдается. По-видимому, эти белки важны для других физиологических процессов, например регуляции сосудистого тонуса, формирования воспалительного ответа; они также обладают антитромботическими и профибринолитическими свойствами.
И наоборот, при дефиците факторов XI, IX или VIII наблюдается склонность к кровотечениям, следовательно, эти белки внутреннего пути играют существенную роль в обеспечении гемостаза. Участие в гемостазе фактора XI, возможно, определяется его активацией не фактором ХIIа, а тромбином. Такая положительная обратная связь позволяет фактору ХIа обеспечивать распространение процесса коагуляции, а не запускать его.
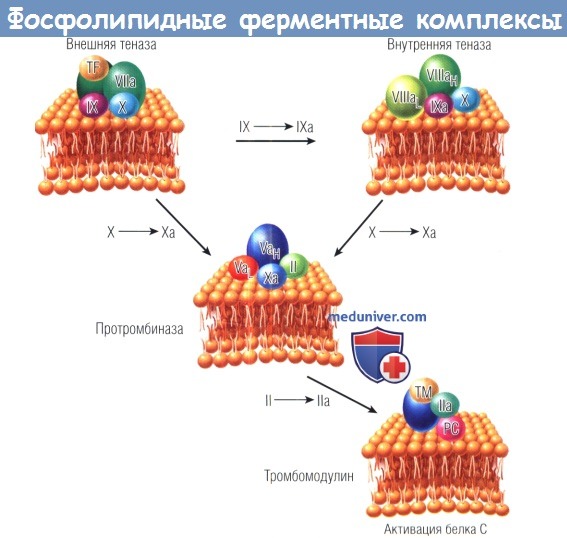
Каждая витамин К-зависимая сериновая протеаза — факторы VIIa, IXa и Ха и α-тромбин (IIа) — связана на поверхности мембраны со своим кофактором — тканевым фактором (TF), факторами VIIIa и Va и тромбомодулином (ТМ) — и субстратами зимогена — факторами IX и X, протромбином (II) и белком С (PC).
Факторы VIIIa и Va характеризуются наличием двух доменов и состоят из тяжелой (Н) и легкой (L) цепей, которые соединены между собой ионами Са2+. Оба домена необходимы для связывания кофактора с мембраной и с протеазой.
в) Общий путь каскада коагуляции. Фактор Ха, который образуется с помощью комплекса тканевый фактор-фактор VIIa или фактора IХа (в присутствии фактора VIIIa), инициирует общий путь коагуляции, конвертируя неактивный протромбин в тромбин, являющийся центральным звеном каскада коагуляции. Кофактором этой реакции является фактор Va, который, как и фактор VIIIa, образуется под влиянием тромбина из фактора V путем протеолиза. Как уже отмечалось, тромбину присуще большое число функций, но его основная роль в процессе свертывания крови сводится к превращению растворимого фибриногена в нерастворимый фибрин.
Полимеризация фибрина представляет собой последовательный процесс межмолекулярных взаимодействий. Тромбин также активирует фактор XIII (фибринстабилизирующий фактор) с образованием фактора ХIIIа — трансглютаминазы, которая ковалентно связывает фибриновый сгусток, стабилизируя его.
Каскад коагуляции, заканчивающийся образованием фибрина, был бы неэффективен, если бы происходил непосредственно в жидкой плазме. Однако взаимодействие всех факторов коагуляции на активированной мембране клеток усиливает скорость реакций и позволяет локализовать процесс формирования сгустка в месте повреждения сосуда. Более того, происходит предотвращение инактивации протеаз, образующих комплексы с факторами коагуляции, что в еще большей степени усиливает эти реакции.
Основными компонентами клеточных мембран, обеспечивающими развитие реакций каскада коагуляции, являются кислые фосфолипиды. Этот тип фосфолипидов в норме не экспрессируется на поверхности клеточных мембран, однако когда механическое повреждение или воспалительный процесс активирует тромбоциты, моноциты или эндотелиальные клетки, прокоагулянтные мембранные фосфолипиды транслоцируются на поверхность этих клеток, обеспечивая их участие в процессах коагуляции.
г) Фосфолипидные ферментные комплексы. Основные мембранные фосфолипидные ферментные комплексы включают теназы и протромбиназные комплексы. Каждый комплекс состоит из сериновой протеазы, ее субстрата (профермента) и кофакторов, связанных друг с другом на поверхности мембраны. Внешняя теназа состоит из комплекса тканевый фактор-фактор VIIa и его субстратов — факторов IX и X. Внутренняя теназа состоит из фермента — фактора 1Ха, субстрата — фактора X и кофактора — фактора VIIIa.
В состав протромбиназного комплекса входят фермент — фактор Ха, субстрат — протромбин (фактор II) и кофактор — фактор Va. Фактор IХа, образующийся под действием внешней теназы, становится ферментом для внутренней теназы. Фактор Ха, образующийся под действием внешней теназы или внутреннего теназного комплекса, становится ферментом для протромбиназного комплекса. Эти последовательные реакции происходят, по-видимому, на одной и той же мембранной поверхности.
Конечный продукт — тромбин — необходим для выполнения целого ряда функций. Как показано на рисунке ниже, во время заключительной реакции свободный тромбин (фактор IIа) связывается с интегральным мембранным белком тромбомодулином, который активирует белок С, являющийся основным антитромботическим белком.
- Читать "Механизмы антикоагуляции (схема антитромботической системы)"
Редактор: Искандер Милевски. Дата публикации: 22.2.2019
