Сердечно-сосудистые проявления акромегалии (избытка гормона роста)
В медицине существует мало областей, в которых базисные научные разработки настолько приближены к клинической практике, как в области сердечно-сосудистой эндокринологии. Знание клеточных и молекулярных эффектов различных гормонов помогает лучше понять клинические проявления состояний с избытком секреции гормонов и их дефицитом. Более 200 лет назад Caleb Hillier Parry, английский терапевт, описал женщину с зобом и сердцебиением, у которой «каждый удар сердца сотрясал грудную клетку». Он был первым, кто высказал предположение о связи между заболеванием сердца и увеличением щитовидной железы.
Аномалии сердечно-сосудистой системы, связанные с патологией желез внутренней секреции, были описаны еще до того, как смогли идентифицировать гормоны, продуцируемые данными органами. Эта и последующие статьи на сайте посвящены заболеваниям сердца, причинами которых являются изменения функционирования органов эндокринной системы. Такой подход позволяет оценить клеточные механизмы повреждения сердечнососудистой системы различными гормонами вследствие их влияния на кардиомиоциты, гладкомышечные клетки сосудов и другие органы и ткани.
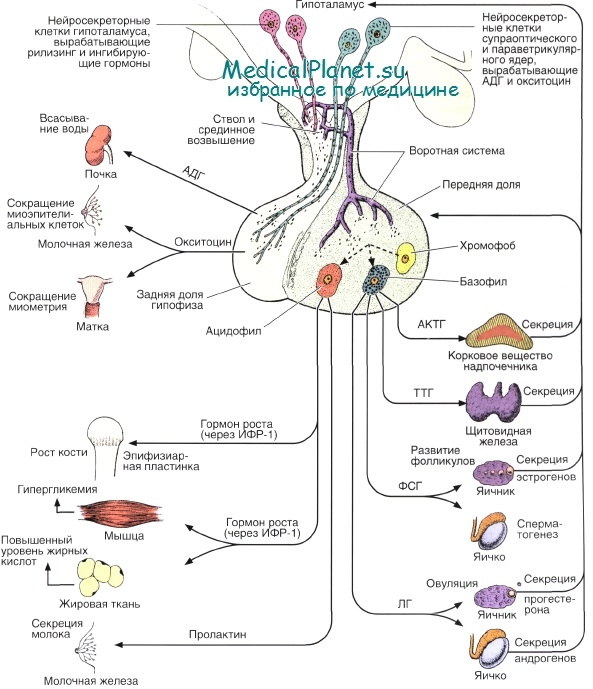
Гипофиз состоит из двух различных анатомических долей. Передняя доля (аденогипофиз) содержит 6 типов клеток, 5 из которых продуцируют пептидные или гликопротеиновые гормоны, 6-й тип — это несекретирующие хромофобные клетки. Развитию сердечно-сосудистых заболеваний (ССЗ) могут способствовать изменения функции как соматотрофных клеток, продуцирующих соматотропный гормон (СТГ), так и кортикогропных клеток, адренокортикотропный гормон (АКТГ). В задней доле гипофиза (нейрогипофизе) находятся окончания аксонов нейросекреторных клеток, выделяющие в кровь вазопрессин (антидиуретический гормон) и окситоцин.
У взрослых повышение секреции СТГ до закрытия зон роста в костях скелета приводит к гигантизму, а после окостенения эпифизов — к акромегалии. Фактор, ускоряющий рост, был выделен из экстрактов гипофиза и идентифицирован Evans и Long в начале 1920-х гг. Через почти 50 лет были установлены белковая последовательность и структура СТГ и его роль как одного из членов семейства факторов, ускоряющих рост (соматических).
Гормон роста действует на клетки двумя различными путями. Один из них — связывание СТГ с гормон-специфичны-ми рецепторами на клетках-мишенях. Такие рецепторы были обнаружены в сердце, скелетных мышцах, жировой ткани, печени, почках и на многих других клетках, существующих в процессе развития плода. Второй путь влияния СТГ на клеточный рост — стимуляция синтеза инсулиноподобного фактора роста 1 (IGF-1). Этот белок первичновырабатывающих продуцируется печенью, но и другие типы клеток могут синтезировать его под влиянием СТГ.
Вскоре после идентификации семейства инсулиноподобных факторов роста было высказано предположение об их способности опосредовать клеточные эффекты СТГ. Выраженность клинических проявлений акромегалии в большей степени коррелирует с IGF-1, чем с СТГ. Способность данных факторов усиливать потребление глюкозы и синтез белка клетками легла в основу термина «инсулиноподобные факторы». IGF-1 связывается со специфичным рецептором (IGF-1-рецептором), расположенным фактически на всех типах клеток. При проведении экспериментов на трансгенных животных было показано, что наличие данного типа рецепторов тесно связано со способностью клеток к делению.
В оригинальных экспериментах при повышении экспрессии IGF-1-рецепторов на кардиомиоцитах увеличилось число клеток, возросла степень митозов и повысилась способность миоцитов к репликации после дифференцировки. Эти изменения могут служить основанием для дальнейших генетических манипуляций и исследований но восстановлению повреждений миокарда.
Инфузия СТГ или IGF-1 остро меняет гемодинамику. Повышение сократимости миокарда и СВ могут быть связаны со снижением системного сосудистого сопротивления и постнагрузки. Кратковременное введение СТГ и IGF-1 не повышает АД, поскольку, как предполагается, увеличение СВ является следствием именно изменений системного сосудистого сопротивления.
а) Сердечно-сосудистые проявления акромегалии. Акромегалия — относительно редкое заболевание в США (900 новых случаев в год). Несмотря на это, акромегалия и гипофизарный гигантизм ассоциированы со значимым ростом заболеваемости и смертности от сердечно-сосудистой патологии. Акромегалия, диагностированная по клинической симптоматике и повышению секреции СТГ, без лечения значительно укорачивает продолжительность жизни (< 20% больных имеют шанс прожить более 60 лет).
Многие исследования также показали, что определенный вклад в повышение уровня смертности в этой группе пациентов вносят опухоли ЖКТ, полипы толстой кишки, рак толстой кишки и легочная патология. Однако сердечно-сосудистые и цереброваскулярные заболевания, включающие гипертензию, кардиомегалию, ХСН и нарушение мозгового кровообращения, продолжают играть главную роль в снижении показателей выживаемости пациентов. Поражение сердечно-сосудистой системы при акромегалии — это хронический и коварный процесс, впервые описанный Pierre Marie в 1886 г.
Сердечно-сосудистые и гемодинамические последствия акромегалии зависят от возраста пациентов, тяжести и длительности заболевани. У больных с длительностью активной фазы болезни < 5 лет значимые изменения САД или ДАД отсутствуют, но индекс массы миокарда ЛЖ по данным ЭхоКГ повышен почти на 35%, сердечный индекс — на 24%. Систолическая функция сердца, включая ударный индекс, значимо выше, системное сосудистое сопротивление повышено на 20%, но диастолическая функция ЛЖ остается в норме. Большая длительность болезни приводит к дисфункции ЛЖ и КМП.
В отсутствие лечения формируется выраженная диастолическая дисфункция в сочетании с гипертрофией миокарда. Аномалии регионарного систолического напряжения миокардиальной стенки, установленные с помощью допплеровского исследования, на фоне лечения обратимы.
Такие известные ФР заболеваний сердца, как гипертензия, инсулинорезистентность, СД и гиперлипидемия, часто присутствуют у пациентов с акромегалией. Первоначально считалось, что нарушение функции сердца при длительно существующей акромегалии связано с потенцированием развития атеросклероза, но данные аутопсии выявили значимые поражения коронарных артерий только у 11% больных, умерших от сердечнососудистых причин. Результаты ангиографии показали, что у большинства больных коронарные артерии в норме или расширены. Радионуклидные исследования при нагрузке дали положительные результаты менее чем у 25% пациентов. Это позволило сделать вывод, что ИБС вряд ли является причиной значимого увеличения бивентрикулярной гипертрофии, СН и сердечно-сосудистой смертности.
Под влиянием длительного воздействия повышенных концентраций СТГ или IGF-1 в сыворотке развиваются скорее специфические функциональные и гистологические изменения миоцитов. До 60% больных акромегалией имеют на ЭКГ признаки ГЛЖ. Масса миокарда ПЖ при акромегалии также выше нормы, что отражает развитие генерализованного процесса вследствие системной гипертензии. Асимметричная гипертрофия перегородки, ранее считавшаяся характерным признаком акромегалии, является нетипичной находкой. Акромегалия также повышает частоту патологии аортального и митрального клапанов, которая персистирует независимо от эффективности лечения основного заболевания. При неконтролируемой акромегалии прогрессируют митральная регургитация и дилатация ЛЖ, могут наблюдаться расширение корня Ао и нарушения в проводящей системе сердца.
Гистологическое исследование у пациентов с акромегалией выявляет гипертрофию кардиомиоцитов (увеличение их размера без увеличения количества клеток). Развиваются также ин терстициальный фиброз и полиморфно-клеточная инфильтрация, в т.ч. мононуклеарная, что свидетельствует о миокардите. Отсутствие клеточных некрозов на фоне воспалительной реакции позволяет высказать предположение, что данные изменения связаны с IGF-1-зависимым апоптозом.
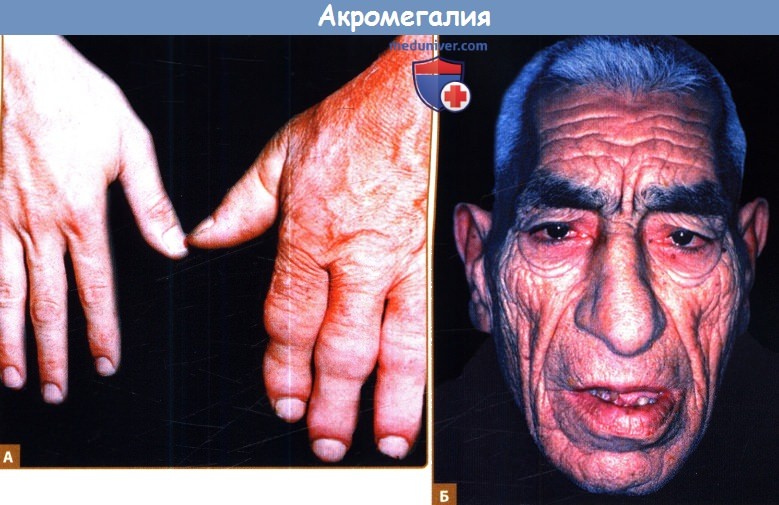
Б. У пациентов развиваются глубокие борозды на лбу и вокруг носогубных складок. При увеличении челюсти могут наблюдаться промежутки между зубами.
Функциональные изменения сердца при акромегалии идут параллельно патогистологическим. Хотя только около 10% вновь выявленных пациентов с акромегалией имеют кардиальные симптомы, этот процент значительно растет с увеличением длительности заболевания. Некоторые исследования показали низкую частоту встречаемости клинически явной левожелудочковой недостаточности, поэтому можно предположить, что для нарушения функции сердца необходимы такие сопутствующие факторы, как гипертензия, СД-2, гиперлипидемия. При акромегалии левожелудочковая недостаточность и ХСН могут развиться без гипертензии в анамнезе, что свидетельствует о роли высоких уровней гормона роста и IGF-1 в развитии патологии кардиомиоцитов без участия каких-либо дополнительных факторов. Следует отметить, что эффективная терапия приводит к регрессу многих, если не всех, изменений миокарда.
Аномалии на ЭКГ, включающие отклонение электрической оси сердца влево, септальные зубцы Q, депрессию интервала ST-T, изменение длительности сегмента QT и нарушения проводящей системы сердца, присутствуют у 50% больных акромегалией. Встречаются различные виды нарушений ритма: предсердная и желудочковая экстрасистолия, синдром слабости синусового узла, наджелудочковые и желудочковые тахикардии. Увеличение в 4 раза частоты сложных желудочковых аритмий и поздних потенциалов на сигнал-усредненной ЭКГ хотя и может быть предиктором электрической нестабильности миокарда желудочков, но более часто отмечается при активной акромегалии, чем у пациентов, получающих лечение. Напротив, нагрузочные тесты не приводят к аритмии или ишемии миокарда, что свидетельствует об отсутствии связи желудочковых аритмий со скрытой ишемией.
У 20-40% больных развивается симптоматическая АГ. Учитывая ее широкое распространение во взрослой популяции и часто постепенное развитие акромегалии, определить, какой характер носит АГ — первичный или вторичный (т.е. сопутствующая патология), — достаточно трудно. Нормализация АД на фоне терапии акромегалии позволяет предположить ее симптоматический характер. Первоначально эпидемиологические исследования выживаемости при акромегалии показали, что гипертензия является независимым ФР летального исхода, но у пациентов, умерших от акромегалии, среднее АД было выше, чем у выживших. Механизмы развития гипертензии при акромегалии недостаточно ясны. У пациентов с небольшой длительностью заболевания показатели САД и ДАД не отличаются от показателей в сходной по возрасту и полу популяционной группе, но сердечный индекс существенно выше.
Создается впечатление, что при большей длительности заболевания увеличивается толщина интимы артерий, которая может уменьшаться в ответ на снижение СТГ.
Назначение гормона роста приводит к задержке натрия и гиперволемии и, по-видимому, оказывает потенциальный антинатрийуретический эффект, независимый от влияния альдостерона. В исследованиях РААС не удалось добиться оптимальной блокады высвобождения ренина при гиперволемии. У пациентов с акромегалией при терапии ингибиторами ангиотензина II АД повышается парадоксальным образом. Обсуждается также роль гиперинсулинизма. Повышение концентрации инсулина может способствовать задержке натрия почками, нарушению эндотелий-зависимой вазодилатации и росту активности СНС.

б) Диагностика акромегалии. В 99% случаев причиной акромегалии является аденома передней доли гипофиза. К моменту постановки диагноза размер опухоли у большинства пациентов составляет > 10 мм (макроаденома), а симптомы заболевания присутствуют свыше 10 лет. Диагноз можно подтвердить уровнями СТГ > 5 нг/дл и IGF-1 > 300 мкМЕ/мл в сыворотке через 1 час после нагрузки глюкозой (100 г). У большинства больных уровень гормона роста натощак составляет > 10 пг/мл. Локализацию опухоли можно определить с помощью МРТ. Реже причиной акромегалии является избыточная секреция соматотропинрилизинг-гормона, что приводит к диффузной гиперплазии гипофиза. Кроме того, возможно развитие эктопической неоплазии эндокринных клеток.
в) Лечение акромегалии и поражения сердца. Методом выбора является транссфеноидальная резекция аденомы. Если уровни СТГ и/или IGF-1 остаются повышенными, для их снижения можно использовать как лучевую терапию (у пожилых пациентов), так и агонисты допаминовых или соматостатиновых рецепторов (у молодых пациентов). Октреотида ацетат, фармакологический аналог соматостатина, эффективен у большинства пациентов для снижения уровня СТГ < 5 нг/мл. Терапию октреотидом назначают для снижения уровня IGF-1 и уменьшения размеров опухоли. При достижении ремиссии заболевания отмечается положительный эффект в отношении АГ, ГЛЖ и дисфункции ЛЖ. Недавно одобренный антагонист рецепторов СТГ пегвисомант при длительном лечении может снижать уровень IGF-1 до нормы и рассматривается как вариант терапии у пациентов, резистентных к соматостатину.
- Читать "Сердечно-сосудистые проявления болезни Кушинга (Cushing)"
Редактор: Искандер Милевски. Дата публикации: 19.2.2019
