Контроль обмена жирных кислот. Запас жирных кислот в клетке
Эти воздействия, очевидно, зависят от соотношений с метаболизмом других соединений (углеводы и белки), от запаса энергии в клетке печени и от перемещения липидов между печенью и другими тканями нашего тела. По отношению к другим тканям печень играет роль, подобную ее роли в поддержании постоянства уровня глюкозы в крови, поскольку печень вносит существенный вклад в обеспечение нормального содержания белков, фосфолипидов, холестерина и некоторых липопротеидов плазмы; печень является важнейшим потребителем жира хиломикронов и фонда свободных жирных кислот плазмы крови.
При регуляции бета-окисления первостепенное значение имеет доступность субстрат. Поступление жирных кислот в клетки печени обеспечивается:
1) захватом неэтерифицированных жирных кислот, доставляемых в печень из жировой ткани (регуляция выхода жирных кислот из жировых клеток осуществляется главным образом гормонами, как это будет изложено в следующем разделе);
2) захватом жирных кислот, освобождаемых при воздействии внеклеточной липазы на хиломикроны (наиболее существенные изменения в поступлении субстрата из этого источника обусловлены содержанием жиров в пище) и
3) освобождением жирных кислот под действием внутриклеточной липазы из триглицеридов печени.
Как и в случае липазы жировой ткани, которую мы будем обсуждать в следующем разделе, действие липазы печени стимулируется теми гормонами, которые способствуют повышению содержания циклического АМФ в результате активации аденилатциклазной системы; в печени, таким образом, действие глюкагона вносит важный вклад в увеличение внутриклеточного образования жирных кислот.
Вторым контролирующим фактором — как и при регуляции всех окислительных реакций, которые сопряжены с функционированием дыхательной цепи,— является уровень запаса энергии в клетке. Цикл бета-окисления в митохондриях зависит от потока электронов через центры сопряжения с окислительным фосфорилированием; таким образом, общая скорость потребления жирных кислот путем их окисления зависит от соотношения концентраций АДФ и АТФ.
Когда содержание АДФ находится на высоком уровне (клеточные резервы энергии малы), могут протекать реакции сопряжения, что способствует синтезу АТФ и поддержанию потока электронов от флавопротеид- и НАД-зависимых дегидрогеназ, участвующих в бета-окислении. С другой стороны, когда повышено содержание АТФ, упомянутые выше реакции тормозятся по механизму дыхательного контроля; накапливающиеся жирные кислоты используются для биосинтеза жиров или фосфолипидов, а суммарный синтез пальмитата и других высших жирных кислот в печени повышается.
К числу последних относятся ацетоуксусная кислота и продукты ее восстановления или декарбоксилирования, бета-оксибутират и ацетон соответственно. Эти вещества могут образоваться в ходе реакции, обратной тиолазной, которая в норме благоприятствует расщеплению образующегося при р-окислении остатка ацетоацетила, но которая может быть направлена в сторону обратного процесса конденсации двух молекул ацетил-КоА, когда их концентрация повышена.
Из ацетоацетил-КоА могут образоваться либо стерины, либо свободная ацетоуксусная кислота, как это будет показано в следующем разделе, посвященном обмену холестерина.
- Вернуться в раздел "медицинская физиология"
Оглавление темы "Обмен жиров в организме":1. Обмен липидов в организме. Жиры пищи
2. Липолиз. Соли желчных кислот и мицеллы
3. Всасывание липидов. Обмен липидов в печени
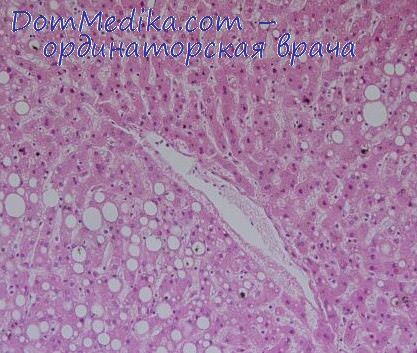
4. Обмен жиров через печеночную артерию. Жировое перерождение печени
5. Окисление жирных кислот. Сжигание жиров в организме
6. Жиры в митохондриях печени. Бета-окисление жиров
7. Эффективный путь окисления жиров. Синтез жирных кислот - липогенез
8. Этапы липогенеза. Стадии синтеза жиров
9. Промежуточные продукты липогенеза. Пальмитил-КоА
10. Контроль обмена жирных кислот. Запас жирных кислот в клетке
