Причины и механизмы развития подагры
Отложение кристаллов солей в полости суставов ассоциируется с широким спектром острых и хронических заболеваний. Среди эндогенных кристаллов выделяют ураты из монофосфата натрия, пирофосфата кальция, гидроксиапатита. К экзогенным кристаллам, способным вызвать заболевания суставов, относят кристаллы сложных эфиров кортикостероидов, талька, полиэтилена, метилметакрилата и биоматериалов.
К сожалению, некоторые производители протезов помимо силикона используют полиэтилен и метилметакрилат. В процессе изнашивания протеза образуются кристаллы, которые могут вызвать локальный артрит и несостоятельность протеза. Эндогенные и экзогенные кристаллы активируют цитокиновый каскад, что лежит в основе патогенеза заболевания. Обсудим два наиболее важных варианта этого вида артропатии: подагру, вызванную накоплением уратов, и псевдоподагру, вызванную отложением пирофосфата кальция.
Человек — единственное млекопитающее, страдающее от спонтанно развивающейся гиперурикемии, которая обусловлена дефицитом фермента уриказы, обеспечивающей деградацию мочевой кислоты у млекопитающих. Дефицит уриказы в сочетании с высокой скоростью реабсорбции мочевой кислоты предрасполагает к развитию гиперурикемии и подагры, являющейся терминальной стадией гиперурикемии.
Подагра характеризуется повторяющимися приступами острого подагрического артрита в результате кристаллизации уратов внутри или около суставов. В конце концов развивается хронический подагрический артрит и формируются тофусы. Тофусы представляют собой крупные агрегаты кристаллов уратов, окруженные воспалительными элементами. У большинства пациентов с хронической подагрой развивается уремическая нефропатия. Гиперурикемия (уровень уратов в плазме более 6,8 мг/дл) является необходимым, но не достаточным условием для развития подагры.
Более 10% населения Западного полушария имеют повышенный уровень уратов в плазме, однако страдают подагрой лишь менее 0,5% из них. Подагра может быть первичной (в большинстве случаев идиопатическая) и вторичной (гиперурикемия является последствием установленного заболевания, а симптомы подагры не доминируют в общей клинической картине). Роль гиперурикемии в развитии гипертонической болезни, хронической почечной недостаточности, сердечно-сосудистых заболеваний, метаболического синдрома и резистентности к инсулину остается в центре внимания исследователей.

а) Патогенез. Мочевая кислота — конечный продукт метаболизма пуринов. Гиперурикемия в 10% наблюдений развивается в результате гиперпродукции уратов из-за повышения метаболизма клетки (например, при злокачественных опухолях, псориазе, распаде опухолей при химиотерапии) и снижения их экскреции.
Уровень мочевой кислоты в плазме регулируется в почках, где происходят процессы клубочковой фильтрации, реабсорбции, секреции и постсекреторной реабсорбции. Примерно 90% мочевой кислоты реабсорбируется, важную роль в этом играет ген URAT1 (транспортера уратов типа 1). Снижение фильтрации и экскреции мочевой кислоты лежит в основе большинства наблюдений первичной подагры. Синтез пуринов происходит посредством двух сигнальных путей:
(1) пути метаболизма de novo, когда пурины синтезируются из непуриновых предшественников;
(2) патологического пути метаболизма нуклеиновых кислот.
В регуляции второго пути участвует фермент гипоксантин-гуанин-фосфорибозилтрансфераза (HGPRT). Дефицит этого фермента приводит к повышению синтеза пуриновых нуклеотидов de novo и, соответственно, увеличению концентрации мочевой кислоты. Полное отсутствие HGPRT ассоциируется со сцепленным с Х-хромосомой синдромом Леш-Найхена и характеризуется гиперурикемией, тяжелым неврологическим дефицитом, нарушением умственного развития и подагрическим артритом. Менее выраженный дефицит HGPRT может вызвать гиперурикемию, подагрический артрит и незначительный неврологический дефицит. Дефицит и полное отсутствие HGPRT достаточно редки.
Как указывалось ранее, гиперурикемия не обязательно приводит к развитию подагры. Переходу бессимптомной гиперурикемии в подагру способствуют многие факторы, среди которых:
- возраст пациента и длительность гиперурикемии. Подагра редко развивается, если гиперурикемия длится менее 20-30 лет;
- генетическая предрасположенность. Помимо полного отсутствия HGPRT подагра ассоциируется со многими наследственными изменениями и передается из поколения в поколение;
- тяжелая алкогольная зависимость, увеличивающая риск приступов подагры;
- ожирение, которое повышает риск развития бессимптомной подагры;
- некоторые лекарственные средства (например, тиазиды), снижающие экскрецию уратов, что повышает вероятность развития подагры;
- отравление свинцом («свинцовая» подагра).
Центральным звеном патогенеза подагры является отложение в полости сустава кристаллов мононатриевых уратов. Растворимость мононатриевых уратов в суставной жидкости зависит от температуры (при более низкой температуре растворимость мононатриевых уратов ниже) и концентрации ионов и мочевой кислоты внутри сосудов. Кристаллизация зависит от наличия ядрообразующих агентов, например растворимых волокон коллагена, хондроитина сульфата, протеогликанов, фрагментов хряща и других веществ. Поскольку суставная жидкость хуже растворяет мочевую кислоту, чем плазма, уровень уратов в суставной жидкости повышается быстрее, чем в плазме, особенно в периферических суставах (лодыжек и пальцев), где температура обычно 20°С.
На фоне длительной гиперурикемии в синовии и суставном хряще формируются кристаллы уратов и микротофусы. В результате неизвестных причин, возможно травмы, кристаллы попадают в синовиальную жидкость и запускается каскад острой воспалительной реакции, обусловливающей клинику подагрического артрита. Макрофаги фагоцитируют кристаллы мононатриевых уратов и посредством неустановленного механизма активируют инфломасому NALP3 — мультипротеиновый комплекс, включающий протеазу каспазы 1. Каспаза 1 активирует ряд цитокинов, наиболее значимые из них — IL-1b и IL-18. IL-1b индуцирует экспрессию молекул адгезии и синтез нейтрофильных хемокинов CXCL8. Нейтрофилы в синовии высвобождают свободные радикалы, лейкотриены (лейкотриен В4) и лизосомные ферменты.
Так идет развитие острого подагрического артрита, симптомы которого исчезают через несколько дней или недель.
Повторяющиеся приступы острого подагрического артрита приводят к хронизации процесса и формированию тофусов в воспаленной синовии и окружающей сустав ткани или где-либо еще. Через некоторое время поражается хрящ и нарушается функция сустава. Неизвестно, почему хронический подагрический артрит некоторое время бессимптомен, хотя в полости сустава выявляются кристаллы мочевой кислоты.
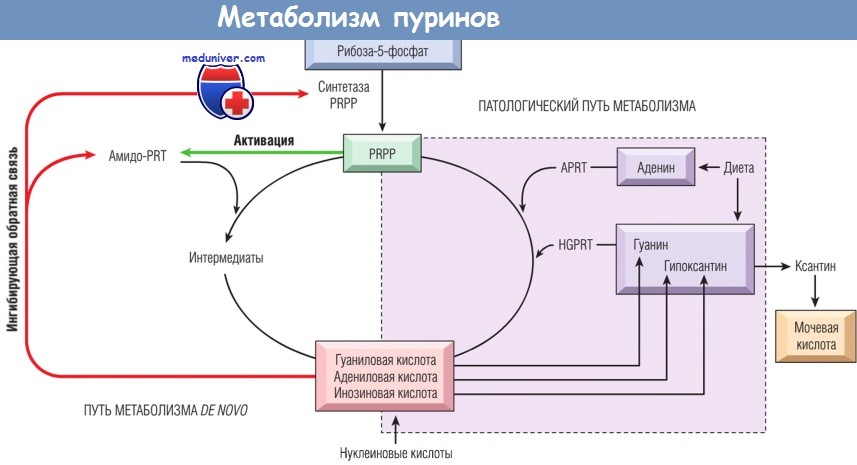
при патологическом пути метаболизма — аденозин-фосфорибозилтрансферазой (APRT) и гипоксантин-гуанин-фос-форибозилтрансферазой (HGPRT).
PRT — фосфорибозилтрансфераза.
б) Морфология. Морфологические изменения при подагре:
(1) острый подагрический артрит;
(2) хронический тофусный артрит;
(3) тофусы других локализаций;
(4) подагрическая нефропатия (иногда).
Острый подагрический артрит характеризуется нейтрофильным инфильтратом в синовии и синовиальной жидкости. В цитоплазме нейтрофилов часто присутствуют кристаллы мононатриевых уратов, которые формируют в синовии небольшие кластеры. Кристаллы имеют форму игл и отрицательное двойное лучепреломление. Синовия отечна и содержит агрегаты лимфоцитов, плазматических клеток и макрофагов. Приступ острого подагрического артрита завершается, когда разрушаются все кристаллы.
Хронический тофусный артрит развивается на фоне атак острого подагрического артрита с повторной преципитацией кристаллов уратов. Ураты могут сильно изменить суставную поверхность и сформировать в синовии депозиты. Синовия становится гиперплазированной, фиброзированной и утолщенной из-за воспалительного инфильтрата, может сформироваться паннус, разрушающий хрящ и кость. При тяжелом течении заболевания наблюдаются фиброзный анкилоз кости, частичная или полная утрата функции сустава.
Тофус — патогномоничный признак подагры. Тофусы образуются в местах крупных отложений кристаллов мочевой кислоты, окруженных воспалительным валом из макрофагов, лимфоцитов и гигантских клеток инородных тел, которые могут быть полностью или частично заполнены кристаллами мочевой кислоты. Тофусы могут формироваться в суставных хрящах и в прилегающих связках, сухожилиях, мягких тканях, включая сумку коленного сустава, суставной отросток локтевой кости и ахиллово сухожилие, а также в мочках ушей. Реже тофусы формируются в почках, хрящах носа, коже пальцев, ладоней и стоп. Поверхностные тофусы могут изъязвляться.
Подагрическая нефропатия ассоциируется с отложением кристаллов мононатриевых уратов в интерстиции мозгового вещества почки. Кристаллы мочевой кислоты могут быть свободно расположенными в мочевыводящих путях, что приводит к формированию уратных камней. Могут развиться вторичные осложнения, например пиелонефрит, особенно при обструкции мочевыводящих путей.
в) Клинические признаки. В клинической картине подагры выделяют несколько стадий:
(1) бессимптомная гиперурикемия;
(2) острый подагрический артрит;
(3) подострая подагра;
(4) хроническая тофусная подагра.
Бессимптомная гиперурикемия развивается у мужчин во время полового созревания, а у женщин после менопаузы. Многие годы острый подагрический артрит протекает в виде приступов, ассоциированных с локальной гиперемией, повышением температуры и нарушением функции суставов. Типичные симптомы артрита появляются редко, кроме небольшого повышения температуры. Большинство приступов являются моноартикулярными. В 50% случаев поражается плюснефаланговый сустав. У 90% пациентов происходят подагрические приступы в следующих суставах (в порядке убывания частоты): плюсневых, голеностопных, коленных, запястных, фаланговых, локтевых.
При отсутствии лечения приступ подагры длится от нескольких часов до двух недель, затем происходит разрешение приступа и заболевание переходит в стадию бессимптомной ремиссии. У некоторых пациентов повторные приступы не наблюдаются вовсе, у других повторяются в течение нескольких месяцев или лет. В отсутствие поддерживающей терапии интервал между приступами уменьшается, часто они становятся полиартритическими. В конце концов спустя годы подагра переходит в хроническую стадию. От первого приступа острого подагрического артрита до хронической тофусной подагры проходит в среднем 12 лет. На последней стадии заболевания на рентгенограммах выявляются характерные околосуставные эрозии костей, вызванные резорбцией костной ткани остеокластами. Прогрессирование приводит к тяжелой инвалидизации.
У пациентов с подагрой распространены сердечнососудистые заболевания, включая атеросклероз и артериальную гипертензию. В некоторых случаях наблюдаются нарушения со стороны почек в виде колик, обусловленных выведением песка и камней, что может вызвать острую подагрическую нефропатию. У 20% пациентов с хронической подагрой развивается хроническая почечная недостаточность. Диагноз «подагра» должен быть поставлен быстро, т.к. многие лекарственные препараты могут снять симптоматику острого артрита и приостановить формирование тофусов. Лекарственная терапия важна, т.к. многие проявления заболевания зависят от уровня и выраженности гиперурикемии. Подагра не влияет на продолжительность жизни, но может значительно снизить ее качество.
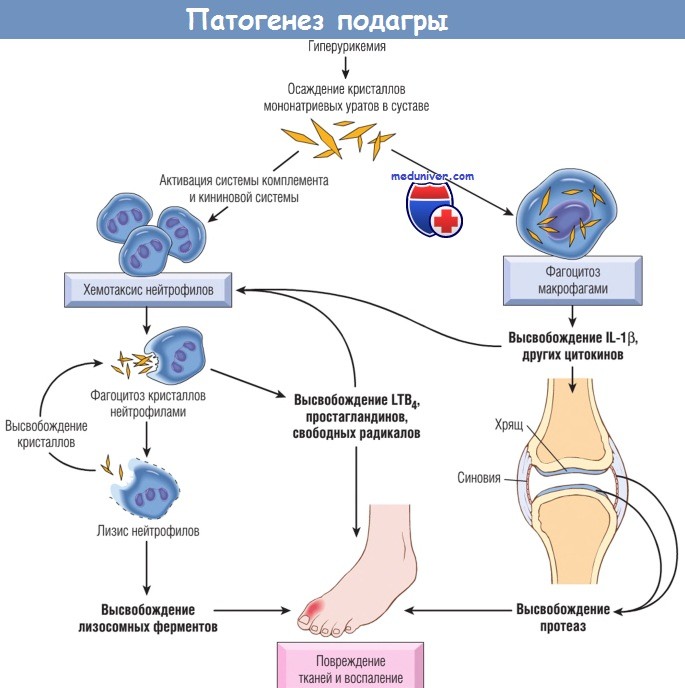
IL — интерлейкин; LTB4 — лейкотриен В4.
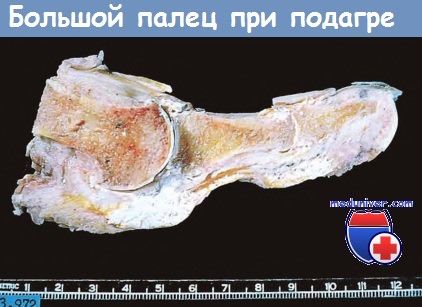
Тофус белого цвета с поражением сустава и мягких тканей.
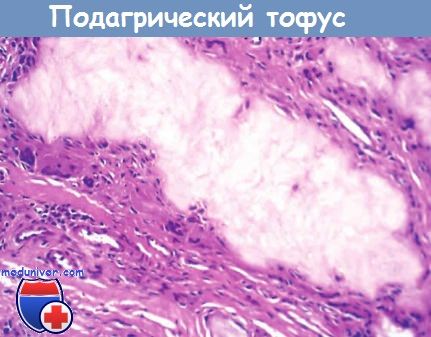
Скопление кристаллов уратов, окруженное реактивными фибробластами,
мононуклеарными воспалительными клетками и гигантскими клетками.
- Читать "Причины и механизмы развития псевдоподагры - хондрокальциноза"
Оглавление темы "Патогенез болезней суставов":- Причины и механизмы развития подагры
- Причины и механизмы развития псевдоподагры - хондрокальциноза
- Причины, механизмы развития гигромы и синовильной кисты
- Причины и механизмы развития теносиновиальной гигантоклеточной опухоли
- Причины и механизмы развития опухолей мягких тканей
- Причины и механизмы развития липомы
- Причины и механизмы развития липосаркомы
- Причины и механизмы развития нодулярного фасциита
- Причины и механизмы развития оссифицирующего миозита
- Причины и механизмы развития фиброматоза
