Причины и механизмы развития сахарного диабета 2 типа
СД типа II является классическим примером мультифакториальной комплексной болезни. В его развитии играют существенную роль такие факторы, как малоподвижный образ жизни и особенности диеты, поскольку установлена взаимосвязь заболевания с ожирением. Также в патогенезе участвуют и генетические факторы, поскольку уровень конкордантности данного заболевания среди монозиготных близнецов варьирует от 35 до 60% (среди дизиготных близнецов он меньше в 2 раза).
Такая конкордантность даже выше, чем при СД типа I, что указывает на большую роль генетического компонента в патогенезе СД типа II. Кроме того, риск развития СД типа II у потомков повышается более чем в 2 раза, если оба родителя страдают этим заболеванием.
Дополнительными доказательствами генетической предрасположенности являются обнаруженные в ходе широкомасштабных исследований генных ассоциаций по крайней мере 12 специфичных локусов. Детальное описание результатов этих исследований не входит в задачи этой главы (будут приведены только несколько типичных примеров таких ассоциаций).
Полимофизмы генов, связанных с функцией b-клеток и секрецией инсулина, определяют повышенный риск развития СД типа II. Самая характерная и воспроизводимая связь затрагивает фактор транскрипции 7, подобный фактору 2 (TCF7L2), на хромосоме 10q, кодирующий синтез фактора транскрипции сигнального пути WNT. Однако в отличие от СД типа I СД типа II не связан с генами, участвующими в обеспечении иммунной толерантности и регуляции (HLA, CTLA4 и т.д.), и не имеет аутоиммунной основы.
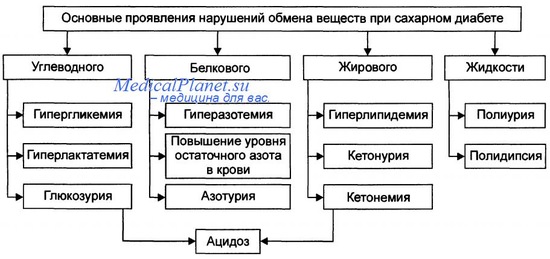
Характерными для СД типа II метаболическими нарушениями являются:
(1) снижение чувствительности периферических тканей к инсулину (инсулинорезистентность);
(2) дисфункция b-клеток, которая проявляется неадекватной секрецией инсулина на фоне инсулинорезистентности и гипергликемии.
Инсулинорезистентность предшествует развитию гипергликемии и обычно на ранних стадиях СД сопровождается компенсаторной гиперфункцией b-клеток и гиперинсулинемией.
а) Инсулинорезистентность. Инсулинорезистентность — это нарушение реакции тканей-мишеней на инсулин, которое приводит к снижению поглощения глюкозы мышцами, уменьшению гликолиза и окисления жирных кислот в печени, а также нарушению подавления глюконеогенеза в печени. Результаты исследований на мышах, лишенных тканеспецифических инсулиновых рецепторов, позволяют предположить, что наибольший вклад в патогенез инсулинорезистентности in vivo вносит утрата чувствительности гепатоцитов к инсулину. При инсулинорезистентности описаны различные функциональные дефекты сигнального пути инсулина (например, снижение фосфорилирования тирозина и увеличение фосфорилирования серина инсулинового рецептора и белков IRS), ослабляющие передачу сигнала.
Самой важной причиной инсулинорезистентности является ожирение.
Эпидемиологическая взаимосвязь ожирения с СД типа II была установлена много лет назад, при этом особое значение имеет висцеральный тип ожирения (80%). Ожирение оказывает сильное влияние на чувствительность тканей к инсулину и, как следствие, на системный гомеостаз глюкозы. Инсулинорезистентность отмечается даже тогда, когда ожирение не сопровождается гипергликемией, что свидетельствует о фундаментальных нарушениях передачи сигнала инсулина при избытке липидов (см. далее). Риск развития СД повышается по мере увеличения индекса массы тела.
При инсулинорезистентности важно не только абсолютное количество жира в организме, но также характер его распределения: абдоминальное (центральное) ожирение в большей степени ассоциируется с развитием инсулинорезистентности, чем висцеральное (периферическое, т.е. в ягодичной области и подкожное).
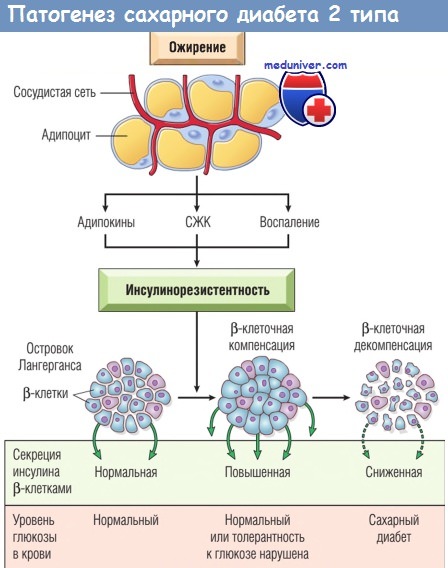
Инсулинорезистентность, связанная с ожирением, индуцирована адипокинами,
свободными жирными кислотами (СЖК) и хроническим воспалением жировой ткани.
b-клетки поджелудочной железы компенсируют инсулинорезистентность гиперсекрецией инсулина,
однако через некоторое время возникает декомпенсация b-клеток и развивается сахарный диабет.
Ожирение может снижать резистентность к инсулину различным образом:
- перекрестный анализ показал наличие отрицательной корреляции между уровнем ненасыщенных жирных кислот в плазме крови натощак и чувствительностью к инсулину. При ожирении в мышечной ткани и ткани печени часто значительно повышен уровень внутриклеточных триглицеридов, предположительно из-за большого количества циркулирующих ненасыщенных жирных кислот и отложения их в этих тканях. Висцеральная жировая ткань более «липолитическая», чем подкожная, что объясняет больший вред такого типа распределения жира. Избыточное количество внутриклеточных ненасыщенных жирных кислот перегружает пути их окисления, что приводит к накоплению в цитоплазме промежуточных продуктов обмена — диацилглицерола и церамида.
Эти промежуточные продукты способны активировать сериновую и/или треониновую киназы, что приводит к аномальному фосфорилированию серина в молекулах инсулинового рецептора и белков IRS. В отличие от модифицирования тирозина фосфорилирование аминокислотных остатков серина ослабляет передачу сигнала инсулина. В норме инсулин подавляет глюконеогенез в печени путем блокады активности фосфоенолпируваткар-боксикиназы (первого фермента в этой цепи). Ослабление передачи сигнала инсулина позволяет этому ферменту усиливать глюконеогенез. При своем избытке свободные жирные кислоты конкурируют с глюкозой в качестве субстрата окисления, что подавляет гликолитические ферменты по механизму обратной связи и усугубляет имеющийся дисбаланс глюкозы;
- установлено, что жировая ткань является не только пассивным депо липидов, но и эндокринным органом, продуцирующим гормоны в ответ на изменения метаболического состояния. Идентифицированы различные белки, секретируемые жировой тканью в кровь, обозначаемые термином «адипокины» (жировые цитокины). Есть прогипергликемические адипокины, например резистин, ретинолсвязывающий белок 4 (RBP4), и антигипергликемические адипокины — лептин и адипонектин. Лептин и адипонектин усиливают чувствительность к инсулину путем непосредственного повышения активности АМФ-активируемой протеинкиназы — фермента, способствующего окислению жирных кислот в печени и скелетных мышцах.
При ожирении уровень адипонектина снижается, что способствует развитию инсулинорезистентности. Необходимо отметить, что АМФ-активируемая протеинкиназа также является мишенью для метформина, который обычно используют в качестве перорального сахароснижающего препарата;
- жировая ткань также секретирует различные провоспалительные цитокины типа TNF, IL-6 и моноцитарный хемоаттрактантный белок 1 (привлекает макрофаги к местам отложения жира). Эксперименты показали, что снижение уровня провоспалительных цитокинов повышает чувствительность к инсулину. Эти цитокины индуцируют инсулинорезистентность, усиливая клеточный стресс, что в конечном итоге приводит к активации многочисленных сигнальных каскадов, препятствующих действию инсулина в периферических тканях;
- рецептор у, активирующий пролиферацию пероксисом (PPARy), является ядерным рецептором и фактором транскрипции, который экспрессируется в жировой ткани и играет важную роль в дифференцировке адипоцитов. Тиазолидины (класс антидиабетических препаратов) действуют как агонисты лигандов для PPARy, улучшая чувствительность к инсулину. Активация PPARy стимулирует секрецию антигипергликемических адипокинов (типа адипонектина) и перемещает процесс отложения ненасыщенных жирных кислот из печени и скелетных мышц в жировую ткань. Как будет сказано далее, редкие мутации гена PPARG, сопровождающиеся серьезным нарушением его функции, могут привести к развитию моногенной формы СД.
б) Дисфункция бета-клеток. При СД типа II b-клетки, по-видимому, со временем исчерпывают свои возможности адаптироваться к длительной инсулинорезистентности периферических тканей. На ранних стадиях инсулинорезистентности, как и при ожирении, секреция инсулина в ответ на любой уровень глюкозы усиливается гораздо больше, чем в норме. Такая гиперинсулинемия является компенсаторным ответом организма на инсулинорезистентность периферических тканей и часто годами поддерживает нормальный уровень глюкозы в плазме крови. После истощения компенсаторных возможностей b-клеток развивается прогрессирующая гипергликемия. Факт, что не у всех лиц с ожирением и инсулинорезистентностью развивается явный СД, позволяет предположить наличие наследственных факторов, предрасполагающих к (3-клеточной недостаточности.
Например, результаты современных исследований показывают, что аллельные варианты гена TCF7L2, связанные с высоким риском развития СД типа II, сопровождаются снижением секреции инсулина клетками островков Лангерганса и указывают на предрасположенность к (3-клеточной недостаточности. Молекулярные механизмы, лежащие в основе дисфункции b-клеток при СД типа II, являются многофакторными и часто перекрываются механизмами инсулинорезистентности. Так, избыток ненасыщенных жирных кислот и ослабление сигнала инсулина способствуют развитию как инсулинорезистентности, так и b-клеточной недостаточности.
Препараты типа метформина, усиливающие окисление жирных кислот путем активации AMФ-активируемой протеинкиназы, также улучшают функцию Р-клеток, тем самым подчеркивая наличие общих патогенетических механизмов у инсулинорезистентности и b-клеточной недостаточности. У лиц с длительно существующим СД типа II характерным признаком заболевания является отложение амилоида в островках Лангерганса (90% случаев). Некоторые исследователи считают, что амилоид в островках Лангерганса оказывает непрямое токсическое действие на их клетки, аналогично действию амилоидных бляшек при болезни Альцгеймера.
- Читать "Причины и механизмы развития моногенных форм сахарного диабета"
Оглавление темы "Патогенез эндокринных болезней":- Причины и механизмы развития вторичного гиперпаратиреоза
- Причины и механизмы развития гипопаратиреоза
- Причины и механизмы развития псевдогипопаратиреоза
- Строение и функции островков Лангерганса поджелудочной железы
- Признаки сахарного диабета
- Классификация сахарного диабета
- Обмен и контроль уровня глюкозы в крови
- Причины и механизмы развития сахарного диабета 1 типа
- Причины и механизмы развития сахарного диабета 2 типа
- Причины и механизмы развития моногенных форм сахарного диабета
