Причины и механизмы развития спорадического рака молочной железы
Факторы риска развития спорадического рака молочной железы связаны с гормональным статусом: возрастом менархе и менопаузы, репродуктивным анамнезом, продолжительностью грудного вскармливания, приемом экзогенных эстрогенов.
Большинство спорадических злокачественных опухолей молочной железы развиваются в постменопаузе и являются ER-позитивными.
Гормональное воздействие увеличивает количество потенциальных клеток-мишеней, стимулируя рост молочных желез во время пубертатного периода, менструального цикла и беременности. Гормоны также регулируют циклы пролиферации, во время которых возможно повреждение ДНК.
При наличии предраковых или злокачественных изменений гормональное воздействие может стимулировать рост опухолевых клеток и нормального эпителия или стромы, что способствует развитию опухоли.
Эстрогены могут играть более значимую роль в канцерогенезе. Метаболиты эстрогенов могут вызвать мутацию или повредить ДНК свободными радикалами клеток, что было показано на животной модели.
Также было отмечено, что некоторые измененные гены, участвующие в синтезе и метаболизме эстрогенов, повышают риск развития рака молочной железы, например аналог цитохрома Р450 изменяет метаболизм тамоксифена у некоторых женщин.
Разнообразные гистологические признаки карциномы молочной железы и вариабельность предраковых поражений служат внешними проявлениями сложных генетических и эпигенетических изменений. Считают, что нормальная клетка должна подвергнуться изменениям, чтобы стать злокачественной. Каждое изменение может быть получено путем смены активности одного из многих генов, регулирующих общий клеточный цикл.
Популяции клеток с генетическими и эпигенетическими изменениями, обусловливающие возможность канцерогенеза, лежат в основе морфологически выявляемых заболеваний молочной железы (см. ранее), которые ассоциируются с повышенным риском рака молочной железы. К самым ранним таким изменениям относят пролиферативные, которые могут быть следствием утраты сигналов, ингибирующих рост, аберрантных усилений сигналов роста или снижения апоптоза. Например, в самых ранних изменениях — атипической протоковой гиперплазии и атипической дольковой гиперплазии — выявляют повышение экспрессии рецепторов гормонов и атипичную регуляцию пролиферации.
Пролиферативные изменения, как правило, редко сопровождаются утратой гетерозиготности, что часто встречается при атипической гиперплазии и является характерным признаком карциномы in situ. Выраженная нестабильность ДНК в виде анеуплоидии (увеличение ядра, нерегулярность контура и гиперхромазия) отмечается только при низкодифференцированной DCIS и некоторых инвазивных карциномах. В определенный момент опухолевой прогрессии клон злокачественных клеток становится бессмертным и приобретает возможность управлять неоангиогенезом.
Морфологические и биологические особенности обычно проявляются уже на стадии карциномы in situ и в большинстве случаев идентичны свойствам сопутствующей инвазивной карциномы.
Происхождение клеток рака молочной железы представляет особый интерес, т.к. имеет большое значение для установления этиологии и назначения терапии. Гипотеза о стволовых опухолевых клетках предполагает, что в популяции стволовых клеток могут появляться злокачественные клетки, которые имеют уникальные характеристики, отличающие их от более дифференцированных клеток.
Хотя большинство опухолевых клеток относятся к нестволовым, только наличие стволовых опухолевых клеток способствует прогрессированию опухоли или ее рецидивированию. Для эффективного лечения необходимо воздействовать только на эту популяцию клеток, которую в настоящее время идентифицировать трудно.
Наиболее вероятный источник большинства карцином молочной железы — люминальные клетки, экспрессирующие ER, т.к. большинство злокачественных опухолей являются ER-позитивными, а клетки на стадии предракового поражения (при атипической гиперплазии) наиболее схожи с люминальными клетками. ER-негативные карциномы могут развиваться из ER-негативных миоэпителиальных клеток, что объясняет, почему в недифференцированной злокачественной опухоли или базальноподобной карциноме обнаруживаются белки миоэпителиальных клеток.
Другим источником происхождения могут быть ER-позитивные клетки-предшественники, утратившие способность экспрессировать ER. Поражения, предшествующие ER-негативным карциномам, неизвестны.
Финальный этап канцерогенеза — трансформация карциномы in situ в инвазивную карциному. Это наиболее важное, но, к сожалению, наименее изученное событие. Генетические маркеры, специфические для инвазивной карциномы, выявить сложно.
Важно помнить, что структура и функционирование нормальной молочной железы зависят от комплексного взаимодействия между люминальными, миоэпителиальными и стромальными клетками. Молекулярные изменения, которые в норме происходят при формировании новых протоков и долек во время полового созревания и беременности (деструкция базальной мембраны, повышение пролиферации, отсутствие подавления роста, ангиогенез и инвазия стромы), могут происходить и при канцерогенезе. Ремоделированием молочных желез, включающим воспалительную и репаративную тканевую реакцию, можно объяснить кратковременное повышение частоты рака молочной железы во время и непосредственно после беременности, т.к. изменения при ремоделировании могут способствовать трансформации карциномы in situ в инвазивную карциному.
Итак, существует множество путей патогенеза рака молочной железы. Рак молочной железы — это не одна болезнь, а несколько, каждая из которых обладает уникальными характеристиками. Определение этой особенности привело к внедрению молекулярной классификации карцином молочной железы.
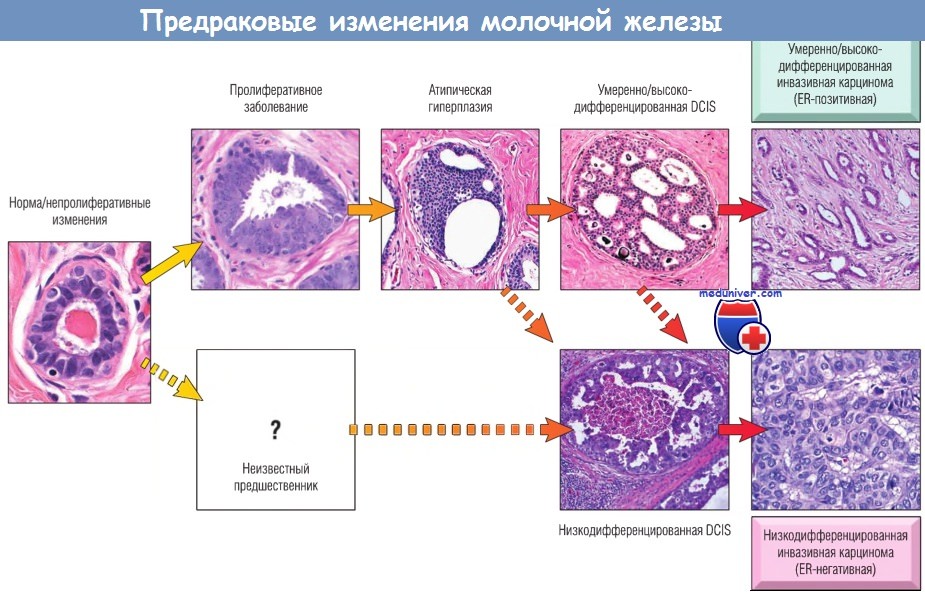
Морфологические характеристики приведены в соответствии с развитием инвазивной карциномы.
DCIS — протоковая карцинома in situ; ER — рецептор эстрогена.
- Вернуться в раздел "медицинская физиология"
Оглавление темы "Патология молочной железы":- Причины и механизмы развития жирового некроза молочной железы
- Причины и механизмы развития лимфоцитарной мастопатии
- Причины и механизмы развития гранулематозного мастита
- Причины и механизмы развития фиброзно-кистозных изменений молочной железы
- Причины и механизмы развития пролиферативных болезней молочной железы без атипии
- Причины и механизмы развития пролиферативных болезней молочной железы с атипией
- Прогноз пролиферативных изменений молочной железы
- Факторы риска рака молочной железы
- Причины и механизмы развития наследственного рака молочной железы
- Причины и механизмы развития спорадического рака молочной железы
