Методы определения адренокортикотропного гормона. Регуляция синтеза АКТГ
АКТГ определяется несколькими методами. Наиболее широко используются методы, основанные на его способности вызывать снижение содержания аскорбиновой кислоты в надпочечниках гипофизэктомированных крыс или увеличивать секрецию 17-оксикортикостероидов, стимулируя кору надпочечников. Поэтому последнему методу раствор стандартного АКТГ или исследуемую пробу вводят в яремную вену или v. saphena крысы, гипофизэктомированиой точно за 2 часа до опыта; в течение 5—20 минут собирают кровь из надпочечниковой вены и определяют в ней содержание 17-оксикортикостероидоп флюорометрическим методом Silber. Таким путем можно определить АКТГ с точностью до 0,03—0,04 миллиединицы.
Использование этого биологического метода позволило установить, что очищенный АКТГ, выделенный из гипофиза овцы, быка или свиньи или приготовленный синтетически, обладает активностью 80—150 международных единиц (Фармакопея США) в 1 мг. Активность человеческого АКТГ равна 26—50 единицам в 1 мг.
Вышеописанный метод позволяет определять содержание АКТГ в плазме крови, если оно превышает 0,1 единицы на 100 мл, поэтому плазму следует концентрировать. В норме в плазме содержится 0—0,5 единицы АКТГ на 100 мл. Уровень АКТГ в плазме повышается при стрессорных состояниях, сопровождающихся стимуляцией коры надпочечников, и колеблется при некоторых расстройствах гипофиза и над почечников. Установлено, что уровень АКТГ в плазме наиболее высок в ранние утренние часы и снижается в течение дня.
Регуляция секреции АКТГ. Гипофизэктомия вызывает быстрое снижение секреции кортикостероидов. Введение АКТГ нормализует секрецию надпочечниковых гормонов, что подтверждает зависимость нормальной секреторной активности надпочечников от гипофизарного АКТГ. У гипофизэктомированных собак имеется линейная зависимость между уровнем секреции кортикоидов и логарифмом дозы АКТГ. Полупериод существования АКТГ у человека составляет около 4—18 минут, а у лабораторных животных еще меньше.
Гормон инактивируется в тканях, в основном в почках. Запасов АКТГ в гипофизе хватает только на то, чтобы поддержать нормальную функцию надпочечников не более часа. Следовательно, синтез и секреция АКТГ должны происходить непрерывно. Регуляция этих процессов является предметом многочисленных исследований и умозрительных построений.
Введение кортикостероидов вызывает уменьшение размеров обоих, надпочечников и угнетает эндогенную секрецию надпочечниковых гормонов. Удаление одного надпочечника сопровождается гипертрофией: оставшегося и повышением секреции им 17-оксикортикостсроидов. У адреналэктомированных животных повышается также уровень АКТГ в крови и гипофизе. Отсюда ясно, что снижение содержания кортикоидов в периферической крови вызывает ускорение продукции АКТГ. Очевидно, что у интактных животных кортикостероиды угнетают синтез и секрецию АКТГ. Это проявляется снижением содержания АКТГ в гипофизе и крови, а также уменьшением веса надпочечников, наступающими, после введения глюкокортикоидов.
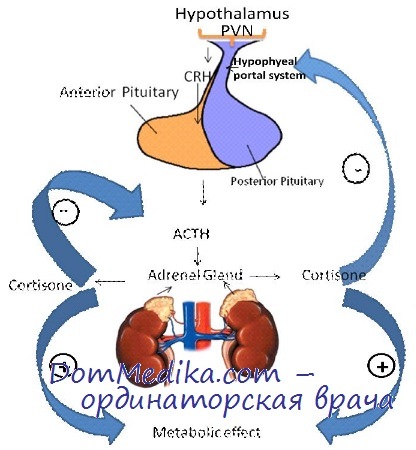
Очевидно, что продукты секреции надпочечников и АКТГ взаимодействуют, коррелируя выброс надпочечниковых гормонов с потребностями организма, опосредуемыми через центральную нервную систему.
Большое внимание уделяется механизму, контролирующему секрецию АКТГ. В этом процессе непосредственно участвует гипоталамус. Однако при удалении гипоталамуса секреция АКТГ не только сохраняется, но может даже превышать ту, которая наблюдается при максимальной гипоталамической стимуляции. В связи с этим вполне возможно, что в норме другие отделы центральной нервной системы оказывают угнетающее влияние на секрецию АКТГ через гипоталамус. Изучением действия экстрактов гипоталамуса доказано, что этот отдел мозга секретирует кортикотропиносвобождающий фактор (CRF), который в свою очередь стимулирует выброс АКТГ из гипофиза.
Brodish и Long доказали наличие этого агента как в крови, оттекающей от срединного возвышения, так и в периферической крови. По-видимому, этот агент образуется каудалыю от перекреста зрительных нервов, так как после двусторонних срединных базальных повреждений в этой области ни адрепалэктомия, ни другие воздействия больше не вызывают выброса АКТГ.
Наряду с другими возможными нейросекреторными факторами роль регулятора секреции АКТГ приписывалась вазопрессину, гормону нейрогипофиза. Имеются также данные о тормозящем влиянии кортикостероидов на структуры среднего мозга, которые имеют свои проекции в гипоталамусе. Так, крысы с перерезкой среднего мозга не выделяли АКЛТ после односторонней адреналэктомип.
Причина этого не в самом надпочечнике, так как он по-прежнему реагирует на экзогенный АКТГ; не понижается при этом сколько-нибудь заметно и чувствительность гипофиза. Образование кортикостероидов в культурах надпочечников крыс in vitro тормозится при добавлении к среде кортизола, что свидетельствует о возможности угнетения системы АКТГ — надпочечники, по крайней мере до некоторой степени, также и на уровне самой коры надпочечников. Таким образом, очевидно, что взаимоотношения АКТГ и надпочечников основаны не на простом принципе обратной связи,. Согласно Yates и Urquhardt, эту связь можно рассматривать как замкнутую петлю (отрицательная обратная связь), своего рода контролирующую систему, включающую элемент обратной связи и изменяющийся уровень, на котором замыкается эта обратная связь; оба компонента локализуются в центральной нервной системе. Говоря языком, более близким биологам, регуляция системы АКТГ — кора надпочечников представляет собой сложное взаимодействуй между рядом нейросекреторных элементов, гипофизом, надпочечниками и, возможно, другими органами.
Реципрокные отношения между секрецией кортикостероидов и АКТГ, служат основой для применения метирапона с целью дифференциальной диагностики между гипофизарным и адреналовым происхождениеч недостаточности коры надпочечников. Введение метирапона (метапирона), блокируя 11-b-гидроксилирование— важный этап синтеза кортикостероидов, снимает существующее в норме сдерживающее влияние: кортизола па выработку АКТГ. Поэтому при нормальной функции гипофиза введение метирапона заметно повышает (у человека от менее чем 0,5 до 1—3 миллиедиииц) содержание АКТГ в плазме.
Однако ограниченность резервов гипофиза, проявляющаяся в том, что реакция на метирапон отсутствует при сохраненной реакции надпочечников на экзогенный АКТГ, может свидетельствовать о нарушении функции либо гипофиза, либо центральной нервной системы, от целостности которой зависит секреция АКТГ. Эффективность АКТГ зависит от способа его. введения. Внутривенное вливание человеку АКТГ в дозе 0,2 единицы в час поддерживает концентрацию АКТГ в плазме, равную 0,5—1 миллиединице в 100 мл, т. е. тот уровень, который наблюдается при стрессе и болезни Cushing. При подкожном введении 5 миллиедиииц АКТГ наступает максимальная секреция надпочечников.
При нормальном содержании кортизола в крови секретируется такое количество АКТГ, которое достаточно для поддержания нормальной активности коры надпочечников, при повышении уровня кортизола продукция АКТГ подавляется частично.
Оглавление темы "Гормоны гипофиза и их функции":- Тиреотропный гормон (ТТГ). Взаимодействие гипофиза и щитовидной железы
- Регуляция синтеза ТТГ. Влияние гипофиза на надпочечники
- Строение адренокортикотропного гормона. Химия АКТГ
- Эффекты адренокортикотропного гормона. Влияние АКТГ на органы
- Методы определения адренокортикотропного гормона. Регуляция синтеза АКТГ
- Влияние гипофиза на половые железы. Эффекты гонадотропных экстрактов и имплантов гипофиза
- Гонадотропные гормоны гипофиза. Фолликулостимулирующий гормон (ФСГ)
- Гормон стимулирующий интерстициальные клетки (ГСИК) - лютеинизирующий гормон (ЛГ). Лактогенный гормон (ЛТГ)
- Гормоны промежуточной доли гипофиза. Химия меланоцитостимулирующих гормонов (МСГ)
- Гормоны нейрогипофиза. Химия вазопрессина и окситоцина
