Профилактика инфекций кровотока в отделениях реанимации новорожденных детей
Бактериальный сепсис развивается у 1 — 10 на 1000 новорожденных детей, несмотря на использование новых и эффективных антибиотиков, уровень смертности новорожденных от бактериального сепсиса остается высоким и варьирует в диапазоне 20-75%. До 6,5% новорожденных детей, находящихся на лечении в отделении интенсивной терапии, имеют диагноз «сепсис», подтвержденный исследованиями крови или ликвора. По данным NNIS, частота катетер-ассоциированных инфекций кровотока в группе новорожденных детей с массой тела менее 1000 г составила 8,5 на 1000 катетеро-дней (данные из 104 отделений), с массой тела 1001-1500 г — 4,0, с массой тела 1501-2500 г — 3,2, в группе с массой тела при рождении более 2500 г — 1,9.
Практически любой патогенный или условно-патогенный микроорганизм может иметь значение как этиологический агент, вызывающий инфекцию кровотока у новорожденных детей.
В этиологии сепсиса у новорожденных детей ведущее место занимают стафилококки (до 50% случаев), второе место — грамотрицательная флора, в основном энтеробактерии (36%). В США этиологическая структура сепсиса менялась с годами: в 30-е годы преобладала грамположительная микрофлора, в 50-60-е годы — грамотрицательная. В последние годы ведущая роль принадлежит стрептококкам группы В и эпидермальному стафилококку, особенно в клиниках для недоношенных детей. Так, G. Tulzer и соавт. отмечают в своих исследованиях, что наиболее частым возбудителем при сепсисе среди новорожденных, находящихся в палате интенсивной терапии, являлся Staphylococcus epidermidis (40% при раннем и 56% при позднем сепсисе).
При раннем сепсисе имели значение Listeria monocytogenes (13%), стрептококки (11%), Е. coli (11%) и S. aureus (10%). Для новорожденных с экстремально низкой массой тела при рождении (< 1000 г), находящихся в отделении реанимации, введение липидсодержащих жидкостей является существенным фактором риска развития коагулазонегативной стафилококковой бактериемии и кандидемии.
Преобладание коагулазонегативных стафилококков в этиологии ИКР в отделениях реанимации связано с более частым и длительным использованием внутрисосудистых устройств, улучшением реанимационной помощи, что приводит к выживанию пациентов, которые раньше имели меньшие шансы (например, новорожденных экстремально низкой массой тела), признание данных микроорганизмов как этиологического фактора.
Бактерии, контаминирующие разъемы катетера, способны мигрировать на его внутреннюю поверхность, а микроорганизмы, находящиеся на руках медицинского персонала, могут быть непосредственно внесены в катетерную рану.
Пути проникновения микроорганизмов в кровоток разнообразны. Возможно распространение микроорганизмов по наружной поверхности катетера, которые попадают с кожных покровов пациента. Они могут мигрировать из места постановки катетера во внутренний тракт и колонизировать конец катетера. Также возможна миграция бактерий по внутренней стенке катетера, если центр канюли колонизирован или если замкнутая внутривенная система становится открытой. В месте постановки катетера происходит создание «катетерной раны», которая включает: место введения, подкожный туннель, выпавший фибрин на катетере, микробную контаминацию, микрофлору кожи пациента, контаминацию разъемов катетера, качество инфузатов, возможность гематогенной миграции бактерий, качество обработки рук персонала.
Проникновение бактерий в кровеносное русло, в котором находится внутрисосудистое устройство, может происходить на фоне уже имеющейся бактериемии, в этом случае реализуется гематогенный путь распространения эндогенной инфекции.
Несмотря на то что введение контаминированных растворов в отделениях другого профиля на сегодняшний день считается наиболее редким, в отделениях реанимации этот путь по-прежнему остается актуальным. Растворы для внутривенного введения часто готовят непосредственно в отделении реанимации из-за необходимости внесения в них множества композиций, при нарушении асептики это часто приводит к возникновению вспышек ВБИ. В Малайзии была зарегистрирована вспышка бактериемии, вызванная Enterobacter gergoviae. Возбудитель был выделен от 11 новорожденных в отделении интенсивной терапии, 9 из которых были недоношенными. Те же самые штаммы были выделены из раствора декстрозы, которая использовалась для разведения парентеральных антибиотиков и обработки рук постовых медицинских сестер. В отделении интенсивной терапии в Тунисе описана вспышка К. pneumoniae с расширенным спектром β-лактамаз. За 25 дней инфекция возникла у 14 новорожденных, все они умерли.
К. pneumoniae оказалась чувствительной только к цефокситину, колестину, имипенему, амикацину (из 17 проверенных антибиотиков). Генотипирование выявило циркуляцию 3 клонов. Загрязнение растворов для внутривенного введения при их приготовлении в отделении явилось причиной возникновения этой вспышки. При расследовании 11 случаев сепсиса, возникших в течение 16 ч, вызванного Е. cloacae, было установлено, что 10 из 11 новорожденных детей получали парентеральное питание. Один и тот же штамм Е. cloacae был выделен в крови 10 из них, а также из парентерального питания. От ребенка, не получавшего это парентеральное питание, был выделен другой штамм. Таким образом, контаминированное парентеральное питание явилось причиной возникновения вспышки сепсиса у детей.
Описано возникновение сепсиса в течение 48 ч у 6 недоношенных новорожденных детей, вызванного Acinetobacter junii. У каждого из них были клинические признаки и дважды из крови выделяли данный возбудитель. Короткий период времени, в течение которого возникла эта вспышка, отсутствие колонизации пациентов данным возбудителем до возникновения сепсиса, позволили предположить, что Acinetobacter junii попала к новорожденным детям при внутривенном введении, Единственным фактором, который объединял всех пациентов, являлось внутривенное введение жировой эмульсии (10% интралипид). У других 4 новорожденных, которым вводился 20% интралипид или аминокислоты, сепсис не развился. Вводимый 1% интралипид уже не был доступен для исследования. Фабричные же партии данной серии раствора не дали роста бактерий. Несмотря на это, именно данный раствор мог быть контаминирован микроорганизмами, поскольку он готовился в нестерильных условиях.
Ретроспективное когортное исследование вспышки Е. cloacae, возникшей в отделении интенсивной терапии другого лечебного учреждения и продолжавшейся в течение 2 месяцев, показало, что из 60 поступивших пациентов 8 были инфицированы cloacae (у 2 диагностировали бактериемию, у 1 — пневмонию, у 1 — инфекцию мягких тканей, у 4 — колонизацию дыхательных путей). У новорожденных детей массой тела менее 2000 г, родившихся в сроки менее 33 недель, более часто развивалась инфекция. Анализ показал, что использование мультидозовых флаконов было независимо связано с контаминацией Е. cloacae.
В Бразилии в результате расследования вспышки лихорадки и клинического сепсиса, повлекшей гибель 36 новорожденных детей, было выявлено наличие высоких титров эндотоксина в крови заболевших пациентов и в глюкозе, использующейся для внутривенных инфузий. Все случаи заболевания возникали после введения растворов глюкозы.
Факторы лечебно-диагностического процесса нередко способствуют возникновению ИКР. Так, например, сосудистые катетеры являются неотъемлемой частью временного лечебного процесса. Катетеризация сосудистого русла сопряжена с риском развития инфекционных осложнений, как местного, так и системного характера септический тромбофлебит, эндокардит, метастатические очаги инфекции в различных органах — остеомиелит, эндофтальмит, артрит и ИКР).
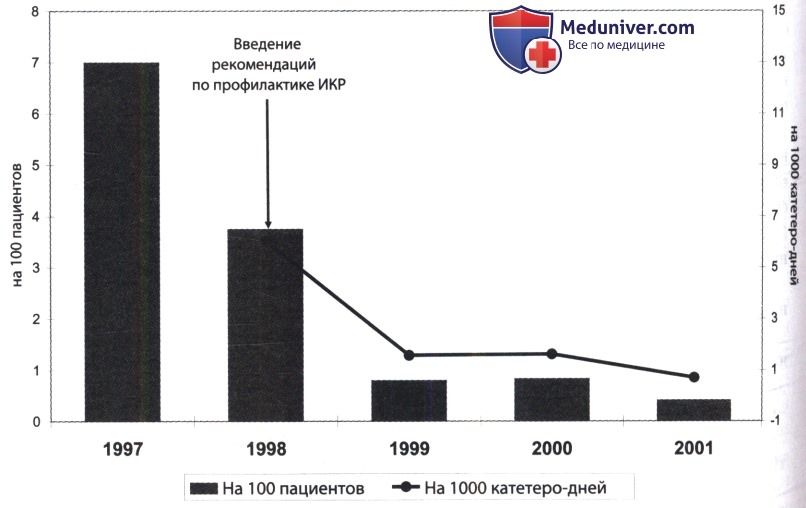
Практические рекомендации по профилактике развития ИКР основываются на знании современных эпидемиологических тенденций развития этих заболеваний.
Для снижения риска развития ИКР необходимо внедрять следующие мероприятия:
• отказ от венесекций;
• катетеризацию центральных вен методом пункции;
• введение в штат процедурных медицинских сестер, ответственных за постановку и уход за катетерами;
• постановку катетера в стерильной одежде, стерильных перчатках;
• внедрение гигиенической антисептики рук и использования стерильных перчаток при любых манипуляциях, связанных с катетерами.
Также необходимо внедрять алгоритмы приготовления внутривенных растворов в специально оборудованном для этого помещении, оснащенном шкафом с ламинарным потоком воздуха. Все растворы для парентерального введения должна готовить специально обученная медицинская сестра. Внедрение этих рекомендаций позволяет значительно снизить частоту ИКР.
Таким образом, внедрение таких недорогостоящих мероприятий, как гигиена рук медицинского персонала, изоляционно-ограничительные мероприятия являются основой мер профилактики инфекций нижних дыхательных путей и инфекций кровотока. Они позволяют снизить частоту ВБИ в отделениях реанимации новорожденных детей. Внедрение современных, действенных методов контроля за течением инфекций вносит вклад в улучшение качества оказания медицинской помощи новорожденным детям и снижает затраты на их лечение.
- Вернуться в оглавление раздела "Медицинская микробиология"
Редактор: Искандер Милевски. Дата публикации: 12.10.2020
- Этиология внутрибольничной инфекции (ВБИ) у новорожденных детей
- Факторы риска возникновения внутрибольничной инфекции (ВБИ) у новорожденных детей
- Причины высокой заболеваемости в отделениях реанимации новорожденных детей
- Факторы передачи инфекции в отделениях реанимации новорожденных детей
- Инфекционный контроль в отделениях реанимации новорожденных детей
- Эпидемиологическое наблюдение в отделениях реанимации новорожденных детей
- Гигиена рук в отделениях реанимации новорожденных детей
- Использование перчаток и одежды в отделениях реанимации новорожденных детей
- Профилактика инфекций нижних дыхательных путей в отделениях реанимации новорожденных детей
- Профилактика инфекций кровотока в отделениях реанимации новорожденных детей
