Избирательная эффективность лекарств для лечения аритмии
Метаболиты антиаритмических препаратов (ААП) могут усиливать или изменять действия ЛС в целом, оказывая тот же эффект, конкурируя с первоначальным препаратом или являясь токсичным медиатором. У хинидина известны но крайней мере 4 активных метаболита; ни один из них не превосходит по силе действия сам препарат в целом, ни один из них не вызывает развитие тахикардии torsades de pointes.
Около 50% прокаинамида метаболизируется до N-ацетилпрокаинамида (NAPA), который пролонгирует реполяризацию и является менее эффективным ААП, но способен конкурировать с прокаинамидом за ренотубулярные секреторные участки и увеличивать период полувыведепия первоначального препарата. Метаболит лидокаина может конкурировать с лидокаином за натриевые каналы и частично устраняет блокаду, вызванную лидокаином.
Фармакогенетика антиаритмических препаратов (ААП)
Генетически детерминированные метаболические пути отвечают за большинство различий в реакциях пациентов на некоторые ААП. Генетически детерминированная активность печеночной N-ацетилтранеферазы регулирует образование антинуклеарных антител и развитие волчаночного синдрома в ответ на прокаинамид.
У фенотипов с более медленным ацетилированием волчанка разовьется скорее, чем при быстром ацетилировании. У 7% пациентов отсутствует дебризоквин-4-гидроксилаза. Для метаболизма дебризоквина (антигипертензивный препарат) и пропафенона нужен фермент цитохром Р450 (CYP450), который гидроксилирует несколько β-АБ и биотрансформирует флекаинид.
Недостаток этого фермента: он снижает метаболизм основного вещества, что ведет к повышению его концентрации в плазме и снижению концентрации его метаболитов. Пропафенон метаболизируется с помощью CYP450 до метаболитов с несколько меньшим антиаритмическим и β-адренергическим блокирующим эффектами, а также с несколькими побочными эффектами (ПЭ) со стороны центральной нервной системы. Таким образом, недостаток метаболитов может привести к большему снижению ЧСС и нейротоксичности, чем их избыток.
Учитывая стереоизбирательность (когда два вещества с идентичным атомным составом, но различной пространственной структурой могут иметь различные фармакологические свойства) и фармакогенетику, можно получить основное представление о различиях в эффективности и токсичности ААП у разных пациентов.
Такие антиаритмические препараты (ААП), как рифампин, фенобарбитал и фенитоин, провоцируют синтез большего количества CYP450, что ведет к снижению концентрации первоначального препарата, который хорошо метаболизируется, в то время как эритромицин, кларитромицин, флуоксетин и грейпфрутовый сок ингибируют активность фермента, что ведет к аккумуляции первоначального ЛС.
Это объясняет, почему антиаритмические препараты (ААП) цизаприд, применяемый для увеличения секреции в желудочке, может влиять на удлинение интервала QT, а в отдельных случаях быть причиной развития тахикардии torsades de pointes. Цизаприд блокирует задержанное выпрямление тока IKR, но у большинства пациентов не удлиняет значительно интервал QT, в основном из-за усиленного метаболизма. У пациентов, которые принимают ингибитор CYP450 (например, эритромицин) вместе с цизапридом, последний может накапливаться, что ведет к удлинению интервала QT и развитию тахикардии torsades de pointes.
- Читать "Дозы, частота приема лекарств для лечения аритмии"
Оглавление темы "Аритмии":- Электрофизиологическое исследование (ЭФИ) при потере сознания
- Электрофизиологическое исследование (ЭФИ) при сердцебиении
- Осложнения электрофизиологического исследования (ЭФИ)
- Прямое картирование сердца при аритмии и электроанатомическая карта
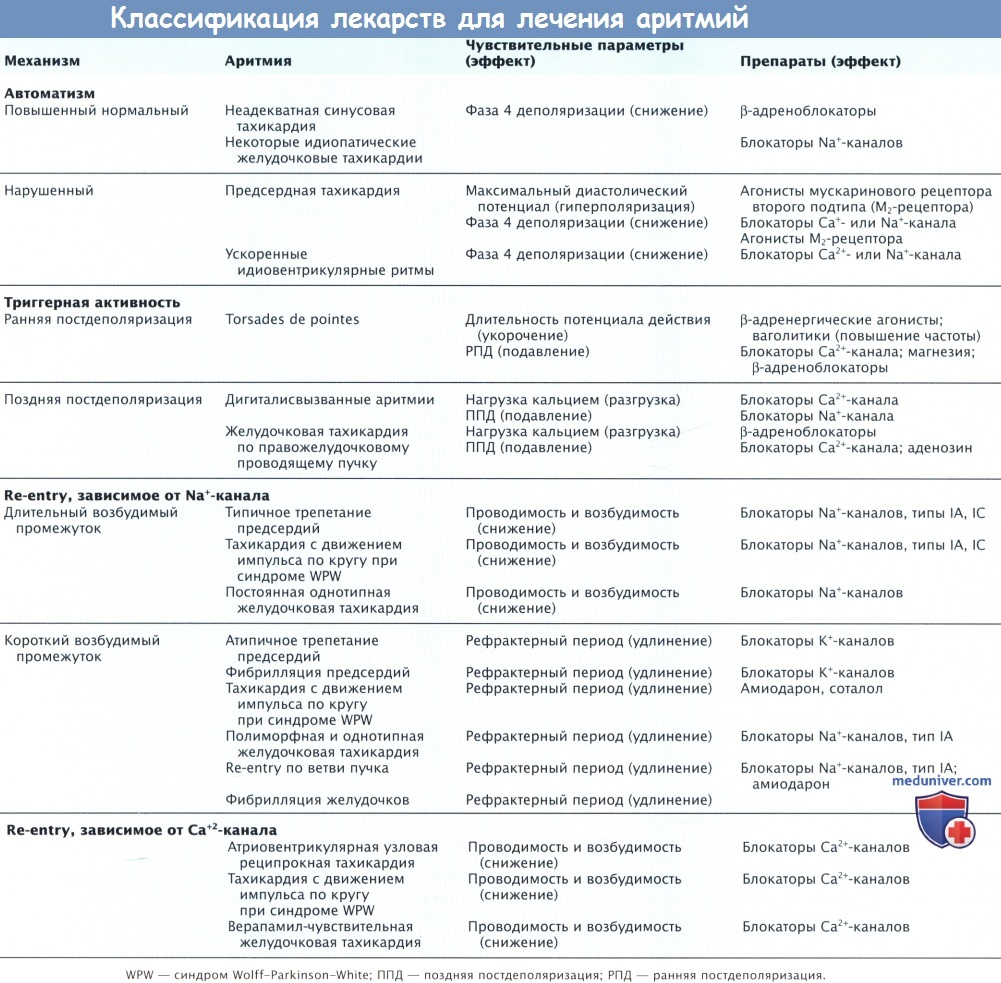
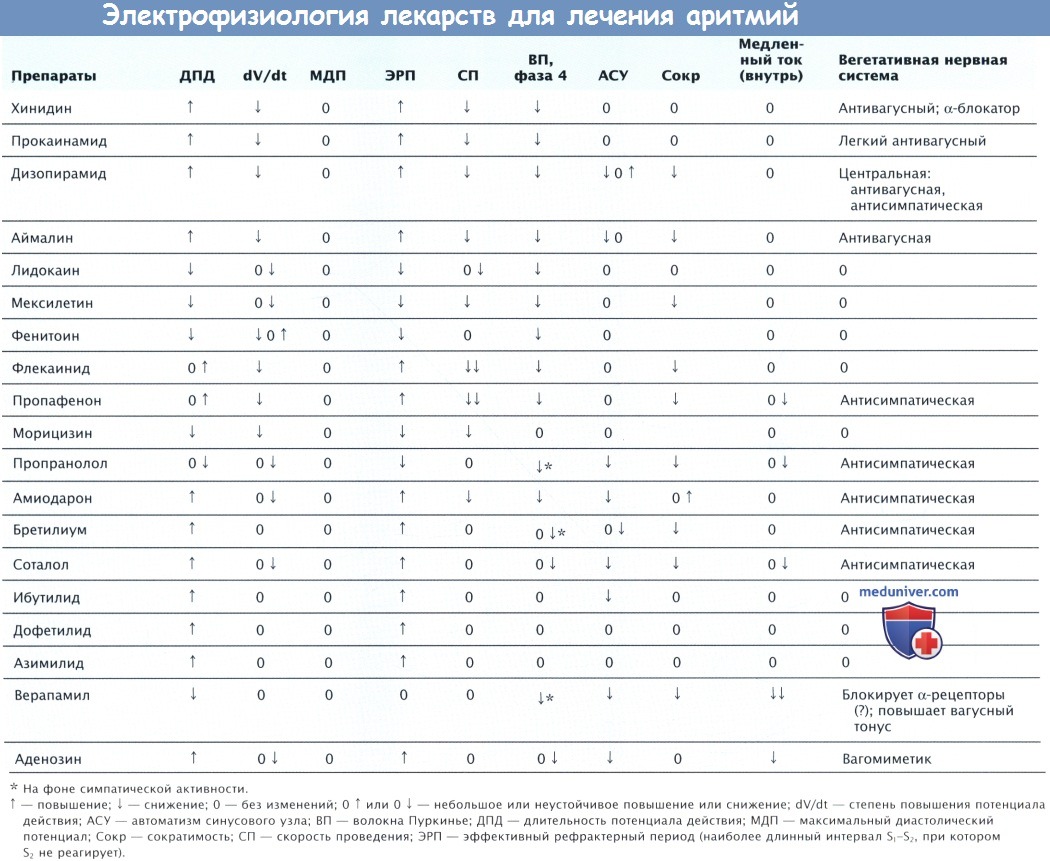
- Классификация антиаритмических лекарственных препаратов
- Частотная зависимость антиаритмических препаратов
- Механизмы подавления аритмии антиаритмическими лекарственными препаратами
- Избирательная эффективность лекарств для лечения аритмии (фармакогенетика)
- Дозы, частота приема лекарств для лечения аритмии
- Побочные эффекты лекарств для лечения аритмии
