Функции и иннервация синусового узла
Весьма вероятно, что ни одна одиночная клетка синусового узла (СУ) не может выполнять функцию водителя сердечного ритма. Скорее всего, клетки СУ функционируют как электрически сопряженные осцилляторы, которые разряжаются синхронно вследствие взаимного поглощения. Таким образом, те клетки, которые разряжаются быстрее, тормозятся клетками, разряжающимися медленнее.
Они сами «подгоняют» себя таким образом, что возникает самостоятельно спровоцированный частотный разряд. Их взаимодействие зависит от степени сопряжения и электрофизиологических характеристик индивидуальных синоатриальных клеток. При этом скорость, с которой разряжается СУ, не является средней арифметической скорости разряда каждой клетки. Любая клетка, обладающая свойствами водителя ритма, взаимодействует в среднем с пятью другими клетками, каждая из которых потенциально обладает разными электрофизиологическими свойствами, вот поэтому результирующую скорость потери заряда нельзя спрогнозировать заранее.
У человека синусовый ритм запускается импульсом, происходящим из достаточно удаленных друг от друга очагов СУ, в которых формируются два или три волновых фронта, сливающихся в один, широко распространяющийся фронт.
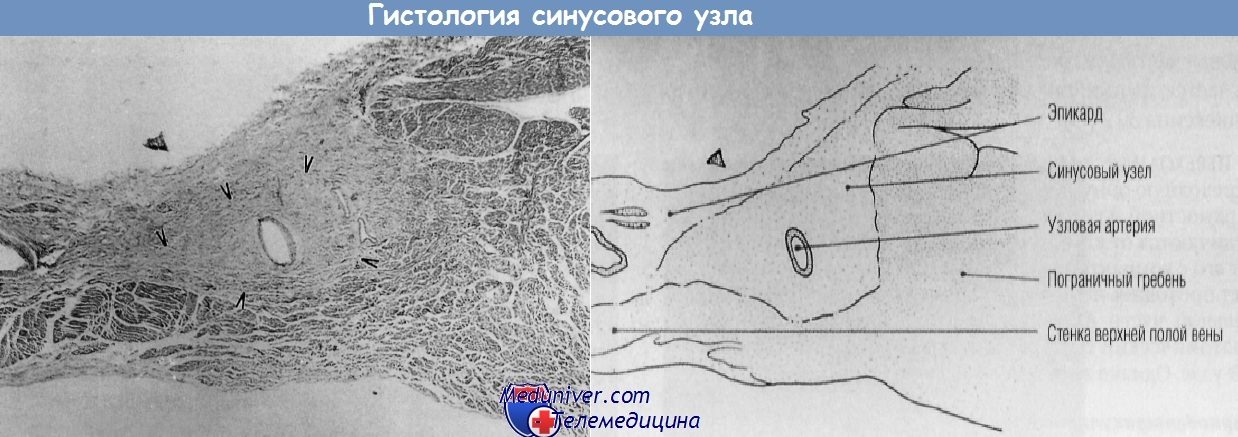
показывает, что по короткой оси узел представляет собой клиновидную структуру, расположенную между стенкой верхней полой вены и пограничным гребнем.
Отмечены прерывистые границы между синусовым узлом и тканью предсердия (острия стрелок). В узел проникает артерия синусового узла.
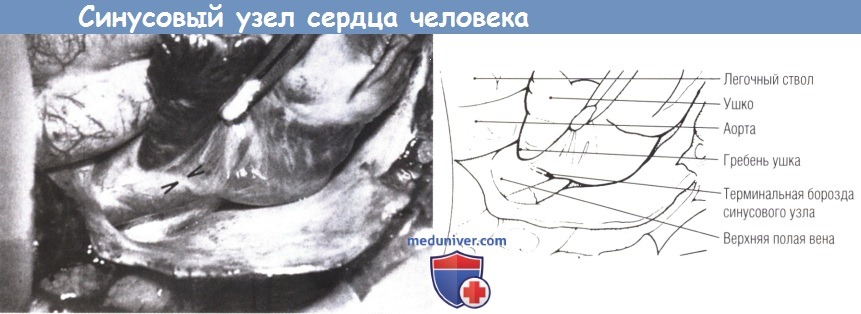
На фотографии, сделанной непосредственно во время операции, представлена локализация синусового узла нормальной сигароподобной формы,
расположенного вдоль латеральной границы терминальной борозды в области соединения верхней полой вены и предсердия (острия стрелок).
Иннервация синусового узла (СУ)
Синусовый узел (СУ) густо иннервирован постганглионарными адренергическими и холинергическими нервными окончаниями. У собак и нечеловекообразных приматов отдельные вагусные центробежные волокна иннервируют области СУ и атриовентрикулярного узла. Большинство центробежных вагусных волокон, направляющихся к предсердию, стремится соединиться сначала в области единственной жировой «подушки», расположенной между медиальной частью ВПВ и корнем Ао спереди от правой ЛA. Затем волокна проходят через два других жировых слоя в области соединения НПВ с ЛП и правой ЛВ с предсердием, постепенно проникая нервными окончаниями в оба предсердия. Вагусные волокна, направляющиеся к СУ и АВ-узлу, также подходят к области ВПВ-корень аорты (Ао) через жировую прослойку, прежде чем достигнут жирового слоя в области правой ЛВ и НПВ.
При этом в синусовый узел (СУ) определяется некоторое количество норадреналина, эквивалентное тому, которое обнаруживается в других областях ПП, а также ацетилхолина, ацетилхолинэстеразы и холинацетилтрансферазы (фермента, необходимого для синтеза ацетилхолина). Все эти вещества в наиболее высокой концентрации были обнаружены в СУ, в более низкой концентрации — в ПП, в минимальной концентрации — в ЛП. Концентрация ацетилхолина в желудочках сердца составляет только 20-50% от его концентрации в предсердиях.
Нейротрансмиттеры модулируют скорость потери потенциала (напряжения) в синусовый узел (СУ) посредством стимуляции адренергических и мускариновых рецепторов. В СУ располагаются адренорецепторы обоих типов: β-1 и β-2. В СУ человека плотность β-адренорецепторов и мускариновых рецепторов в 3 раза выше, чем в смежных тканях предсердия. В чем состоят функциональные различия между двумя типами β-адренорецепторов в СУ, неясно. Связывание агонистов рецепторов, высвобождающихся из симпатических нервных окончаний, вызывает положительный хронотропный эффект, который формируется при участии β-1-рецепторно-активированного пути.
Этот путь участвует в стимуляции гуанозинтрифосфата, регуляторного белка, в активации аденилилциклазы, внутриклеточной аккумуляции циклического аденозинмонофосфата, стимуляции цАМФ-зависимой протеинкиназы А, а также в фосфорилировании белков-мишеней, в т.ч. кальциевых каналов L-типа, каналов, обеспечивающих If, рианодин-чувствительных кальцийвысвобождающих каналов (рианодиновые рецепторы) в мембране саркоплазматического ретикулума. Механизм участия вторичных мессенджеров (посредников), лежащий в основе увеличения частоты сердечных сокращений путем активации β-2-рецепторов и основных белков-мишеней, не совсем изучен; вероятнее всего, он функционирует за счет ГТФ-связывающего ингибиторного G-белка.
Отрицательный хронотропный эффект, формируемый при вагусной стимуляции, обеспечивается связыванием ацетилхолина и, как результат, активацией М2-рецепторов. Мембранный ток, регулируемый активацией мускариновых рецепторов, включает ацетилхолин- и аденозин-чувствительный ток К+ — IK(Ach,Ade), Ics.l и If. Влияние агонистов мускариновых рецепторов на активацию IK(Ach,Ade) обеспечивается прямым взаимодействием субъединицы G-белка с K(AchAde)-каналами и не требует дополнительных посредников . Активация IK(Ach,Ade) вызывает гиперполяризацию клеточных мембран СУ, в результате снижается скорость диастолической деполяризации. Воздействие на ICa.L и If, обусловленное активацией мускариновых рецепторов, в первую очередь обеспечивается уменьшением уровня внутриклеточного цАМФ в противовес положительному хронотропному влиянию стимуляции бета-адренорецепторов.
Помимо отрицательного хронотропного влияния ацетилхолин продлевает время внутриузлового проведения, иногда достигая точки (момента) блокады выхода из СУ. Ацетилхолин повышает рефрактерность центра СУ, в то время как норадреналин снижает этот показатель. Фаза сердечного цикла, во время которой происходит вагусная разрядка, зависит от базового уровня симпатической активности, что существенно влияет на скорость и синусовую проводимость. После прекращения вагусной стимуляции функция СУ может автоматически временно ускориться (возникает так называемая поствагусная тахикардия).
Нейротрансмиттеры — нейропептид Y и вазоактивный интестинальный пептид — присутствуют в симпатических и парасимпатических нервных окончаниях соответственно. Вазоактивный интестинальный пептид обратимо повышает If, тогда как нейропептид Y обратимо его снижает. Роль остальных периферических нейротрансмиттеров (пептид, связанный с геном кальцитонина, субстанция Р) в обеспечении электрофизиологической активности СУ остается неясной.
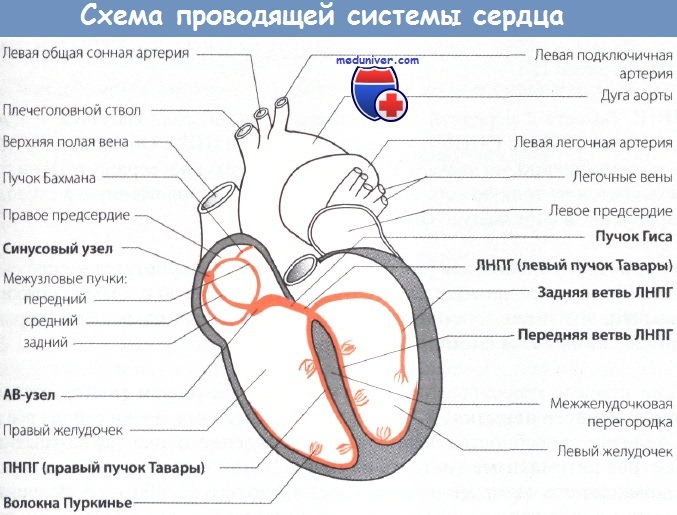
Видео физиология фазы потенциала действия пейсмекерных клеток сердца
- Читать "Механизмы проведения возбуждения от синусового узла по предсердиям"
Оглавление темы "Проводящая система сердца":- Функции и иннервация синусового узла
- Механизмы проведения возбуждения от синусового узла по предсердиям
- Топография, строение атриовентрикулярного узла (АВ-узла) и проведение по нему
- Топография, строение пучка Гиса и проведение по нему
- Топография, строение волокон Пуркинье и проведение по ним
- Клеточный состав АВ-узла и пучка Гиса
- Иннервация АВ-узла, пучка Гиса и желудочков сердца
- Вегетативная нервная система как причина аритмии и внезапной смерти
- Строение ионных каналов сердца и обмен ионов
- Молекулярное строение ионных каналов кардиомиоцитов сердца
