Желудочковая тахикардия по механизму re-entry
Анатомическое или функциональное re-entry в желудочках как причина устойчивой ЖТ была подтверждена во многих экспериментальных и клинических исследованиях. Re-entry в миокарде желудочков с участием специализированной ткани или без нее обусловливает большинство ЖТ у пациентов с ИБС. Область микро-re-entry является очень маленькой, и в редких случаях обнаруживается контур макро-re-entry вокруг постинфарктного рубца.
Живая ткань миокарда, разделенная соединительной тканью, предоставляет извилистые пути активации, пересекающие зоны ИМ, которые могут образовывать пути re-entry. Re-entry ножки пучка Гиса (НПГ) может вызвать устойчивую ЖТ, особенно у пациентов с ДКМП.
Были описаны контуры re-entry как в виде цифры 8, так и в виде одиночного круга, циркулирующие вокруг зоны функционального блока соответственно ведущей гипотезе или с медленным проведением по видимой области блока, созданной анизотропией. Когда интрамуральный миокард жизнеспособен, он может формировать часть контура re-entry.
Структурная неоднородность (нарушение непрерывности), которая разделяет мышечные пучки, например в результате естественной ориентации миокардиальных волокон и анизотропного проведения, а также коллагеновый матрикс, сформированный из фиброзной ткани после ИМ, служат основой для замедленного проведения, фрагментированных электрограмм и продолжительной электрической активности, что может привести к формированию re-entry.
После инфаркта миокарда (ИМ) ткань эпикарда на границе некроза подвержена электрическому ремоделированию, включая уменьшение скорости проведения и увеличение анизотропии, что приводит к появлению контуров re-entry и ЖТ. Замедление проведения происходит из-за нарушения пространственного распределения и электрических свойств ЩС коннексина 43, а также из-за уменьшения токов натрия.
Во время острой ишемии различные факторы, включая подъем уровня [К]o и снижение pH, сочетаются и снижают ПД ишемизированных клеток, что замедляет проведение и может приводить к возникновению re-entry. Действительно, исследования с использованием оптического картирования перфузируемых артериальной кровыо клинообразных препаратов сердца собаки во время выраженной ишемии продемонстрировали запуск механизма re-entry во время первичной ишемии и последующей реперфузии, вызванной однонаправленным блоком проведения в результате пространственно-временного распределения реакций ткани на стимуляцию.
Быстрые изменения в трансмуральном рассеивании в ответ на эндокардиальную стимуляцию и скорость проведения создают динамический субстрат, в котором re-entry может возникнуть и поддерживаться. Результаты этого исследования согласуются с более ранними наблюдениями, при которых фибрилляция во время реперфузии была вызвана интрамуральным механизмом re-entry. Интересно, что трансмуральное re-entry в этих экспериментальных условиях может быть индуцировано эиикардиальной, но не эндокардиальной стимуляцией. Клинически это может способствовать появлению тахикардии, ПЖК, возникающих в эпикарде, но не в эндокарде.
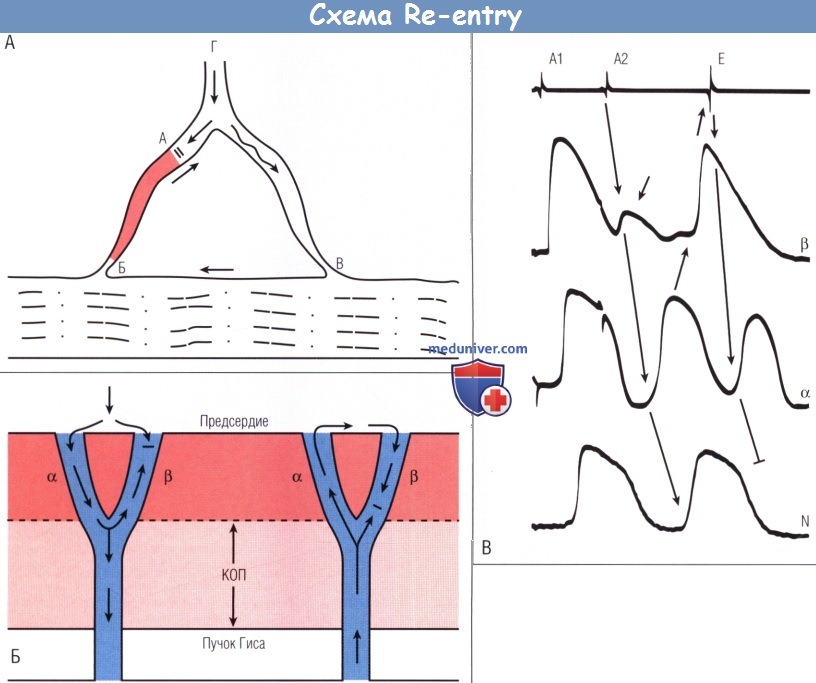
Волокна Пуркинье (Г) разделяются на два пути (Б и В), которые, в свою очередь, соединены с миокардом желудочка.
Предполагают, что импульс продвигается вниз по Г, блокируется в своем антероградном направлении в области А (стрелка, указывающая на двойную линию) и продолжает медленно продвигаться по В (волнистая стрелка),
возбуждая миокард желудочка. Затем импульс повторно входит в волокна Пуркинье на участке Б и ретроградно возбуждает А и Г.
Если импульс продолжает продвигаться по Г до миокарда желудочка и вызывает деполяризацию желудочка,
то образуется желудочковая экстрасистола re-entry. Продолжающееся re-entry такого типа вызовет желудочковую тахикардию.
(Б) Схематическое изображение внутриузловой диссоциации, отвечающей за предсердное эхо (слева).
Преждевременный предсердный ответ не пенетрирует в β-путь, где происходит однонаправленный блок, а распространяется антероградно по a-пути.
Когда конечный общий путь (КОП) занят, импульс может вернуться в предсердие по уже восстановленному β-пути и вызвать предсердное эхо.
На правой схеме — пример распространения во время генерации желудочкового эхо.
Преждевременный ответ в пучке Гиса переходит на КОП, наталкивается на рефрактерный β-путь (однонаправленный блок),
достигает предсердия по a-пути и возвращается по уже восстановленному β-пути, создавая желудочковый эхо-ответ. (В) Запись с предсердия (первая кривая) с клетками, отмеченными в β-области (вторая кривая),
α-область (третья кривая) и часть N АВ-узла (четвертая кривая) в изолированном препарате сердца кролика.
Основной ответ на А1 — активация как а-, так и β-пути и N-клеток (первый уровень ПД).
Преждевременный предсердный ответ на А2, вызванный только локальным ответом в β-клетках (короткая стрелка), с задержкой переходит на а-клетки, в дальнейшем с задержкой распространяется на N-клетки.
Вслед за ответом а-клетки происходит спонтанный ответ β-клетки и распространяется на предсердия (Е). Этот предсердный ответ представляет собой предсердное эхо.
Эхо возвращается для стимуляции а-клеток, но не распространяется на N-клетки. Важно отметить, что, хотя внутриузловое re-entry показано в АВ-узле кролика,
АВ-узловое re-entry у человека, возможно, проходит по внеузловым путям.
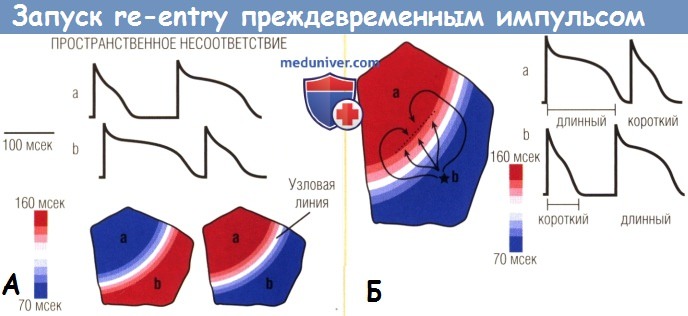
(А) Вверху. При высокой настоте наблюдаются колебания ПД в области а по типу короткий—длинный, а в области b — по типу длинный—короткий.
Создается постепенный градиент распределения длительности ПД с узловой линией без колебаний длительности ПД, отделяющей области а и b вне фазы (внизу).
(Б) Преждевременный импульс (звездочка), возникающий в области b, создает блок (пунктирная линия) при распространении через узловую линию в область с большой длительностью ПД (а).
Преждевременный импульс распространяется латерально вдоль узловой линии в ожидании реполяризации области с большой длительностью ПД и затем повторно входит в зону блока для формирования контура re-entry в виде восьмерки.
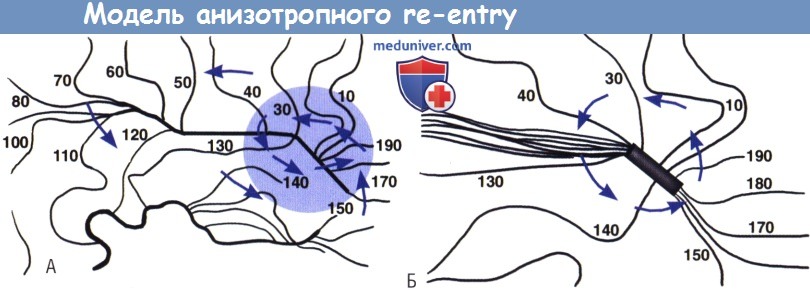
(А) Схема активации одного контура re-entry. Стрелки указывают на общую модель активации; похоже, что активация возникает вдоль длинной линии блока.
Тем не менее параллельные изохроны, прилегающие к линии (изохроны 130 и 140) также указывают,
что активация пересекает линию и приводит к формированию меньшего круга (стрелки в выделенной области).
(Б) Контур re-entry (при увеличении). Быстрая активация происходит параллельно длинной оси направления волокон (изохроны с 10 по 40 и с 130 по 150),
в то время как очень медленная активация (близко к пучку изохронов 50-120) идет поперечно ориентации волокон в контуре.
Темный прямоугольник — область функциональной и анатомической блокады, которая формирует основу контура.
- Читать "Механизм развития синдрома Brugada"
Оглавление темы "Диагностика аритмий":- Желудочковая тахикардия по механизму re-entry
- Механизм развития синдрома Brugada
- Механизм возникновения фибрилляции желудочков (ФЖ)
- Сбор анамнеза при аритмии сердца
- Физикальное обследование при аритмии сердца
- Электрокардиография при аритмии сердца
- Проба с физической нагрузкой при аритмии сердца
- Длительное ЭКГ-мониторирование по Холтеру в диагностике аритмии
- Значение оценки вариабельности сердечного ритма (ВСР)
- Значение турбулентности сердечного ритма (TCP)
