Микробиологическая диагностика возбудителя дифтерии (C. diphtheriae)
Микробиологическая диагностика дифтерийной инфекции основана на классическом бактериологическом исследовании, являющимся золотым стандартом. Учитывая локализацию возбудителя (слизистые оболочки открытых полостей) при выделении и идентификации С. diphtheriae необходимо проводить его дифференциацию с близкими коринебактериями — комменсалами слизистых человека, а также со сходным патогеном домашнего скота С. ulcerans. Последний вызывает маститы коров и через молочные продукты передается человеку.
Однако заражение обычно не возникает, так как С. ulcerans не колонизирует слизистые оболочки человека. Но известны редкие случаи, когда С. ulcerans выделяют из зева здоровых лиц, больных ангинами и даже от людей с дифтериеподобными поражениями зева. В последних случаях заболевание, похожее на дифтерию, вызывают штаммы, выделяющие экзотоксин, сходный с дифтерийным. С. ulcerans обладает нейраминидазой и поражающей ткани фосфолипазой. Некоторые зарубежные авторы предлагают считать С. ulcerans вариантом C.diphtheriae.
Однако экологический признак — неспособность С.ulcerans в норме колонизировать человека не позволяет объединить оба вида. Но о возможности выделения С. ulcerans у человека, больного или бактерионосителя, необходимо помнить.
Морфологически С. ulcerans представляет собой овоидные клетки, беспорядочно расположенные. Колонии на кровяном теллуритовом агаре черные с серым ободком, сухие. Биохимически С.ulcerans активен — разлагает цистин и углеводы, как С. diphtheriae биотипа gravis (глюкозу, мальтозу, крахмал, декстрин) и вдобавок обладает уреазой, но не редуцирует нитраты.
Среди коринебактерий, населяющих слизистые оболочки зева и носа, следует иметь в виду ложнодифтерийную палочку Гофманна (С. pseudodiphtheriticum), С. xerosis, С. striatum. Эти коринебактерии отличаются от С. diphtheriae неспособностью восстанавливать теллур (их колонии на теллуритовых средах серые), отсутствием фермента цистиназы, иногда наличием уреазы, а также иным отношением к углеводам. О роли этих коринебактерий как потенциальных возбудителей оппортунистических гнойно-септических инфекций будет сказано в соответствующей статье на сайте.
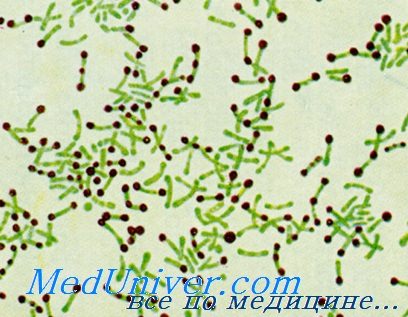
а) Взятие материала для исследования. Материалом для исследования на наличие дифтерийных бактерий служит отделяемое пораженных участков ротоглотки и носа; при редких локализациях — отделяемое конъюнктивы, влагалища, кожных поражений.
При обследовании здоровых лиц на дифтерийное бактерионосительство берется слизь из зева (миндалины, дужки) и носа (нижние носовые ходы). Для взятия проб используют стерильные ватные тампоны, укрепленные на палочках из дерева, нержавеющей стали или алюминия. Фибринозную пленку можно снять пинцетом. Материал берется натощак или не ранее, чем через 2 ч после еды. Отделяемое слизистой ротоглотки (налеты на миндалинах, дужках, язычке), а также носоглотки берется одним тампоном, а нижних носовых ходов — другим. При подозрении на экстрабуккальную дифтерию материал из каждого поражения берется отдельным тампоном; наряду с этим обязательно взятие слизи из зева и носа.
Материал доставляют в лабораторию не позднее, чем через 3 ч после взятия. При необходимости транспортировки проб свыше этого срока тампоны с материалом погружают в транспортную полужидкую теллуритовую среду. После инкубации 18-20 ч в термостате (с целью обогащения) делается высев в чашку Петри с плотной средой.
1. Первый день исследования. Для выделения коринебактерий дифтерии применяют прямой посев ватным тампоном (сухим или смоченным в транспортной среде) на селективную агаровую среду в чашку Петри. Оптимальной является среда с добавлением 10-15% гемолизированной крови (барана, лошади, морской свинки, донора); для подавления сопутствующей флоры в среду вносят 0,04% теллурита калия (кровяной теллуритовый агар, среда Клауберга-2.
Если исследуется материал от больного с подозрением на заболевание дифтерией, то уместен посев на селективную дифференциально-диагностическую среду - цистин-теллурит-сывороточный агар (среда Тинсдейла) в чашку Петри. Преимуществом среды является возможность отбора колоний, обладающих цистиназой, то есть образующих коричневые ореолы вокруг черных колоний (за счет образования сероводорода из цистина и последующего соединения с теллуром). Среда очень демонстративна, но недостаточно чувствительна. Поэтому она не рекомендуется для выделения С. diphtheriae от бактерионосителей, из носа больных дифтерией зева др. источников.
2. Второй день. Через 24 ч инкубации (не раньше!) исследуют появившиеся на агаре колонии, окрашенные в черный цвет благодаря восстановлению металлического теллура из его соли. Дифтерийные колонии суховаты, легко снимаются петлей. При сплошном росте заметны границы между колониями (рост в виде «шагреневой кожи»). Выросшие колонии рассматривают под лупой или в стереоскопическом микроскопе.
Через 48 ч на кровяных теллуритовых средах четко выявляются различия между колониями разных биотипов. Колонии биотипа gravis — аспидно-черные 1,0-1,5 мм в диаметре; через 48 ч благодаря фестончатому краю, радиальной исчерченности и приподнятому центру напоминают цветок маргаритки. Колонии биотипа mitis черные круглые слегка выпуклые, мельче, чем колонии биотипа gravis (0,5-1,5 мм в диаметре), с ровными краями; к концу вторых суток инкубации бывают окружены валиком. Колонии биотипа intermedius — слегка конусообразные круглые 0,5-1,0 мм в диаметре, с серо-черным центром и зернистой поверхностью.
Не дожидаясь формирования различий, на 2-й день исследования (чаще через 24 ч, реже через 48 ч) отбирают несколько подозрительных колоний. Из каждой делают отсев в пробирку со скошенным сывороточным агаром и одновременно — на среды для определения токсигенности и цистиназы.
Отсев нескольких одинаковых колоний обязателен, так как одно и то же лицо может быть инфицировано и токсигенным, и нетоксигенным штаммами одновременно. Отсев на среду для определения токсигенности делают из каждой колонии в виде отдельной «бляшки».
Фермент цистиназу определяют путем посева части колонии уколом в столбик агаровой среды Пизу, содержащей нормальную сыворотку, цистин (субстрат искомого фермента) и уксусно-кислый свинец. Последний играет роль индикатора, который при соединении с H2S, образующимся при расщеплении цистина, переходит в сернистый свинец — соединение темно-коричневого цвета. Посев на среду Пизу делают даже в том случае, если колония была снята со среды Тинсдейла и обладала коричневым ореолом.
3. Третий день. Через сутки у выросшей чистой культуры изучают морфологические и тинкториальные свойства, биохимическую активность — фермент цистиназу, отсутствие уреазы, а также учитывают результаты посева на среду для определения токсигенности. Из выросшей на сывороточном агаре культуры готовят препараты-мазки, окрашенные щелочным метиленовым синим Леффлера, убеждаются в чистоте культуры и изучают ее морфологию. Цистиназу определяют по почернению среды по ходу укола и вокруг него в виде коричневого «облачка».
Дифтерийные бактерии никогда не образуют уреазу, расщепляющую мочевину до СО2 и NH3, в отличие от некоторых других коринебактерий. Для ее выявления взвесь испытуемой культуры вносят в каплю (0,1 мл) реактива Заксе, содержащего спиртовой раствор мочевины и феноловый красный (в нейтральной среде — желтого цвета). Через 30 мин инкубации при 37°С под влиянием образовавшегося гидрата аммония (NH4OH) смесь краснеет, что говорит о наличии уреазы.
Если выросшая культура представляет собой типичные палочки, иногда с метахроматическими зернами, обладает характерным («сухим», иногда кремовым) ростом на сывороточном агаре, расщепляет цистин и не имеет уреазы, то она может быть отнесена к виду С. diphtheriae. В случае выявления у штамма одновременно и цистиназы, и уреазы культура может быть заподозрена как C.ulcerans.
Чтобы окончательно подтвердить (или отвергнуть) эти диагнозы, а также установить биотип культуры, признанной дифтерийной, выделенную коринебактерию засевают на среды для определения сбраживания углеводов — глюкозы, мальтозы, сахарозы, крахмала и декстрина. В этот же день иногда удается определить и токсигенность по появлению линий преципитации на специальной среде с антитоксической сывороткой, куда был сделан посев в предыдущий день.
4. Четвертый день. Учитывают результаты посевов на средах с углеводами и определяют культурально-биохимический тип выделенной культуры (или подтверждают выделение С. ulcerans). Устанавливают наличие токсигенности (если это не было сделано на 3-й день) или, в случае отсутствия линий преципитации, относят изучаемую культуру к нетоксигенным.
Итак, если питательные среды приготовлены правильно, то в большинстве случаев на 3-й день исследования (т.е. через 48 ч с момента его начала) возможна выдача окончательного ответа о выделении токсигенных дифтерийных бактерий (без указания биотипа). В случаях, если рост колоний при первичном посеве задерживается до 2 сут. и/или токсигенность не выявлена через 24 ч после посева на соответствующую среду, то выдача окончательного ответа задерживается еще на 1-2 сут. (т.е. до 72-96 ч с момента начала исследования).
В случае применения транспортной среды обогащения выдача окончательного ответа задерживается на 1 сутки.
При необходимости сохранения выделенной дифтерийной культуры ее отсевают на столбик полужидкого агара с 10% нормальной сыворотки и хранят в холодильнике.
Определение чувствительности выделенной культуры к антибиотикам. Чувствительность к пенициллинам, тетрациклинам, макролидам определяется диско-диффузионным методом.
- Читать далее "Постановка теста на токсигенность дифтерийных культур in vitro иммуно-диффузным методом"
Редактор: Искандер Милевски. Дата публикации: 25.11.2019
- Возбудитель дифтерии (Corynebacterium diphtheriae): морфология и культурально-биохимические свойства
- Антигены возбудителя дифтерии (C. diphtheriae)
- Факторы патогенности возбудителя дифтерии (C. diphtheriae)
- Биологические модели дифтерийной инфекции
- Клинические проявления дифтерийной инфекции
- Иммунитет при дифтерийной инфекции
- Эпидемиология возбудителя дифтерии (C. diphtheriae)
- Микробиологическая диагностика возбудителя дифтерии (C. diphtheriae)
- Постановка теста на токсигенность дифтерийных культур in vitro иммуно-диффузным методом
- Экспресс и серологическая диагностика возбудителя дифтерии (C. diphtheriae)
- Лечение и профилактика дифтерийной инфекции
