Тромбоз артерии как осложнение атеросклероза
В развитии взглядов на патогенез острых коронарных синдромов (ОКС) сделан новый акцент на тромбообразовании как на переломном (решающем) механизме перехода от хронического атеросклероза к его острому течению. Понимание механизмов тромбоза коронарной артерии (КА) существенно прогрессирует.
Сейчас уже ясно, что физическое разрушение атеросклеротической бляшки (АБ) обычно сопровождается острым тромбозом. Появление большинства коронарных тромбов провоцируется разрывами атеросклеротической бляшки (АБ), обусловленными несколькими механизмами.
Первый механизм, объясняющий почти 60% случаев ОИМ, заключается в трещине фиброзной покрышки АБ. Другой механизм — поверхностная эрозия интимы, что объясняет до 25% всех ОИМ среди тщательно отобранных наблюдений, поступивших от экспертов, анализировавших причины внезапной сердечной смерти (ВСС). Поверхностная эрозия в качестве механизма ВСС чаще фигурирует у женщин, чем у мужчин.
а) Разрыв атеросклеротической бляшки и тромбоз. Разрыв фиброзной покрышки АБ отражает, видимо, дисбаланс между силами воздействия на покрышку и силой напряжения самой фиброзной покрышки. Биомеханическая устойчивость к разрыву фиброзной покрышки обеспечивается в основном интерстициальными формами коллагена. Следовательно, процессы метаболизма коллагена участвуют в регуляции предрасположенности атеросклеротической бляшки (АБ) к разрыву. Факторы, угнетающие синтез коллагена в ГМК, снижают способность этих клеток восстанавливать и сохранять фиброзную покрышку атеросклеротической бляшки (АБ).
Например, продуцируемый Т-клетками цитокин IFNγ является мощным ингибитором синтеза коллагена в ГМК. В то же время, как уже отмечалось, некоторые медиаторы, высвобождаемые из тромбоцитарных гранул в процессе их активации, усиливают синтез коллагена в ГМК, укрепляя тем самым фиброзную структуру АБ. К таким медиаторам относятся TGFβ и PDGF.
Помимо снижения в ГМК синтеза коллагена de novo, повышенный катаболизм макромолекул внеклеточного матрикса, которые входят в состав фиброзной покрышки бляшки, также вносит вклад в ослабление этой структуры и повышает риск разрыва, а следовательно, и образования тромба. Те же самые деградирующие ферменты, которые, как полагают, участвуют в миграции ГМК и ремоделировании артерий, могут ослаблять и фиброзную покрышку.
В прогрессирующей атероме человека макрофаги в избытке экспрессируют металлопротеиназы и обладающие эластолитическим действием катепсины, которые способны разрушать коллаген и эластин внеклеточного матрикса артерий. Таким образом, натяжение фиброзной покрышки АБ подвержено динамической регуляции, при которой воспалительная реакция интимы сопряжена с молекулярными детерминантами стабильности АБ и, следовательно, с осложнениями атеромы в виде тромбообразова-ния. Истончение фиброзной покрышки в результате сниженного синтеза коллагена и повышенной его деградации объясняет, почему АБ, которые разорвались и привели к развитию фатального ИМ, имеют согласно патологоанатомическим исследованиям характерную тонкую фиброзную покрышку.
Другой особенностью такой атеросклеротической бляшки (АБ), называемой уязвимой, является относительный дефицит ГМК. Как объяснялось ранее, медиаторы воспаления — как растворимые, так и ассоциированные с поверхностью Т-лимфоцитов — способны вызывать апоптоз ГМК. «Выпадение» ГМК из участков локального воспаления в АБ вносит, вероятно, определенный вклад в относительный дефицит ГМК в тех местах, где происходит разрыв АБ.
Поскольку эти клетки служат источником вновь синтезированного коллагена, необходимого для восстановления и сохранения фиброзной покрышки, при дефиците ГМК она ослабляется, а склонность АБ к разрыву, соответственно, возрастает.
Выраженное скопление макрофагов и большой липидный пул являются третьей микроанатомической особенностью уязвимой АБ. С точки зрения строгой биомеханики большой липидный пул способен концентрировать на себе биомеханические силы, направленные на «плечи» АБ — обычные зоны разрыва фиброзной покрышки. С точки зрения метаболизма активированные макрофаги, характерные для ядра АБ, продуцируют цитокины и деградирующие матрикс ферменты, которые, в свою очередь, как полагают, регулируют метаболизм матрикса и апоптоз ГМК. Находящиеся в состоянии апоптоза макрофаги, как и ГМК, вырабатывают тканевый фактор — потенциальный инициатор капиллярного тромбоза после спонтанного или ятрогенного разрыва АБ. Успехи липидснижающей терапии в уменьшении частоты возникновения ОИМ или НС у пациентов с высоким риском могут быть результатом снижения накопления липидов, уменьшения воспаления и тромбогенности АБ. Результаты недавно выполненных на животных исследований, а также данные мониторинга периферических маркеров воспаления у людей подтверждают эту концепцию.
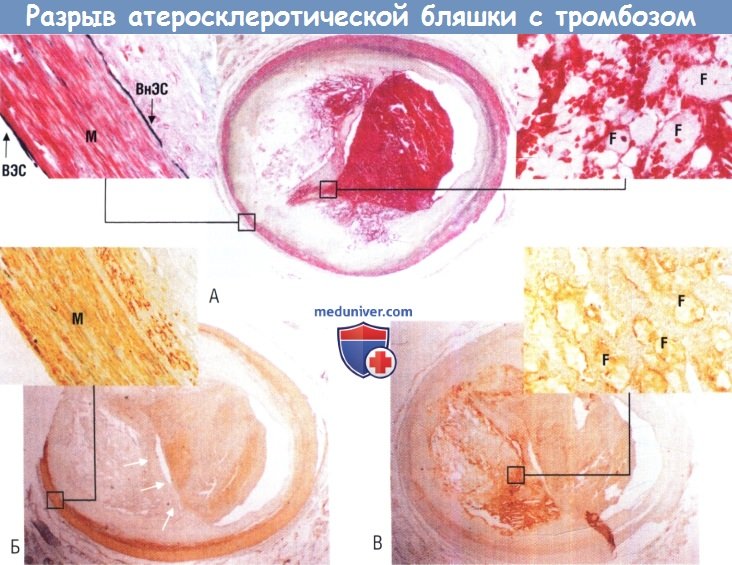
(А) Окрашивание по Movat. (Б) Иммуноокрашивание с помощью HHF-35, при котором визуализируются ГМК.
Видно незначительное количество ГМК в фиброзной покрышке (стрелки) в противоположность их изобилию в среднем слое (вставка).
(В) Окрашивание макрофагов (CD68) позволяет видеть скопление воспалительных клеток вблизи фиброзной покрышки (вставка).
F — пенистая клетка; ВнЭС — внутренний эластический слой; ВЭС — внешний эластический слой; М — медиа.
б) Тромбоз, вызванный поверхностным изъязвлением бляшки. В следующей статье будет обсуждена патофизиология разрыва фиброзной покрышки атеросклеротической бляшки (АБ). Ясности в вопросах поверхностного изъязвления намного меньше. При экспериментальном атеросклерозе, вызванном у обезьян, зоны отсутствия эндотелия и отложения тромбоцитов появляются в более сформированных атеросклеротических бляшек (АБ).
Оказалось, что у человека поверхностные эрозии являются вероятной причиной случаев фатального ОИМ у женщин и лиц с гипертриглицеридемией и СД. Однако молекулярные механизмы, лежащие в основе этого явления, остаются нераскрытыми. Апоптоз ЭК может вносить определенный вклад в десквамацию эндотелия в зонах поверхностного изъязвления. Аналогично этому ММП, включая некоторые желатиназы, специализирующиеся на деградации нефибриллярного коллагена, расположенного в базальной мембране (например, коллаген IV типа), также могут разрушать участки соединения ЭК с подлежащей базальной мембраной и ускорять их десквамацию.
В большинстве случаев разрывы атеросклеротической бляшки (АБ) не приводят к клинически выраженным коронарным событиям. При тщательном патологоанатомическом изучении препаратов сердца, полученных от внезапно умерших по некардиальной причине лиц, в АБ на удивление часто находили очаговые (фокальные) разрывы с ограниченным числом пристеночных тромбов.
Более того, при исследовании извлеченных и сразу же зафиксированных сердец от пациентов, страдавших выраженным атеросклерозом с хроническим стабильным течением и перенесших процедуру трансплантации сердца в связи с ишемической кардиомиопатией (КМП), были получены аналогичные данные, свидетельствующие о бессимптомных разрывах АБ. У обезьян с экспериментальным атеросклерозом было показано, что пристеночные тромбы могут усугубить изъязвление АБ, не вызывая сужение артерии.
Отсюда следует, что повторные циклы, включающие разрыв атеросклеротической бляшки (АБ), тромбообразование in situ и заживление (рубцевание), вносят, вероятно, определенный вклад в прогрессирование атеросклеротического поражения и рост АБ. Подобные эпизоды тромбообразования и рубцевания представляют собой один из типов «кризиса» в процессе развития АБ, который вызывает всплеск пролиферации и миграции ГМК и синтеза в них матрикса. Синтез коллагена в ГМК, как отмечено ранее, стимулируют TGFβ и PDGF, высвобождаемые из тромбоцитарных гранул. В роли мощного стимулятора пролиферации ГМК выступает тромбин, образующийся в зоне пристеночного тромбоза.
Последняя стадия атеросклеротического процесса («перегоревшая» фиброзная и кальцифицированная атерома) представляет собой конечный этап развития исходно перегруженной липидами и уязвимой бляшки, превратившейся в фиброзное и практически бесклеточное образование в ответ на повреждение, опосредуемого продуктами тромбообразования.
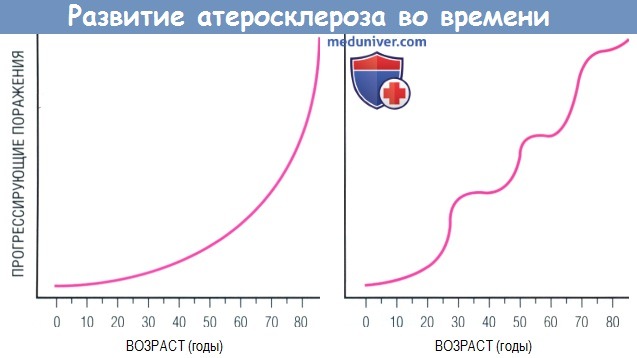
Согласно традиционному взгляду, формирование атеромы с течением лет происходит прогрессивно по нарастающей (слева).
Современный взгляд предлагает альтернативную модель: не монотонная эволюция поражения в зависимости от времени, а скорее ее поэтапное развитие (справа).
Согласно последней модели, в процессе развития атеросклеротического поражения относительно спокойные периоды могут сменяться «кризисами».
Вслед за таким «кризисом» возможен разрыв бляшки с интрамуральным тромбозом, ее рубцевание, сопровождающееся всплеском пролиферации ГМК и отложением матрикса.
Аналогичное развитие событий может быть спровоцировано кровоизлиянием внутри бляшки, вызванным разрывом хрупких микрососудов.
Такие эпизоды обычно клинически не проявляются. Внесосудистые события, например случайная инфекция, сопровождающаяся системной цитокинемией или эндотоксинемией,
способны вызвать «эхо» на уровне артериальной стенки, индуцируя цикл локальной экспрессии генов цитокинов с помощью «профессиональных» воспалительных лейкоцитов, присутствующих в зоне поражения.
Представленная справа модель эпизодического прогрессирования бляшки больше соответствует данным ангиографии у человека, чем кривая слева.
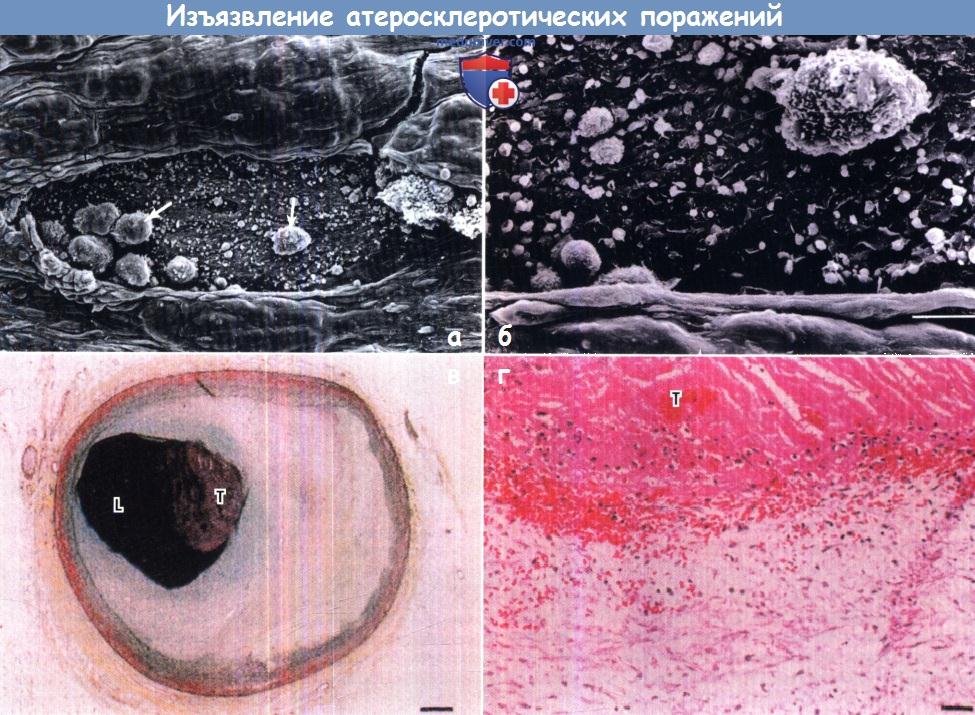
Прогрессирующие атеросклеротические бляшки стимулируют тромбообразование за счет поверхностного изъязвления эндотелиального слоя и контакта крови
и тромбоцитов с содержащей коллаген субэндотелиальной базальной мембраной, а также активацию тромбоцитов и тромбообразование.
(А) При низком разрешении видна трещина в эндотелии. Лейкоциты (стрелки) прилипли к субэндотелию, который начинает покрываться слоем тромбоцитов.
(Б) При высоком разрешении на участке, выбранном из центра (А), видны лейкоциты и тромбоциты, прилипшие к субэндотелию.
(В) Гистологический срез через коронарную артерию с тромбом, образовавшимся в результате поверхностного изъязвления (фото низкого разрешения).
(Г) Гистологический срез через коронарную артерию с тромбом, образовавшимся в результате поверхностного изъязвления (фото высокого разрешения).
L — просвет сосуда; Т — тромб.
- Читать "Воспаление атеросклеротической бляшки при атеросклерозе как причина осложнений"
Оглавление темы "Атеросклероз и его осложнения":- Роль иммунитета в развитии атеросклероза
- Миграция и пролиферация гладкомышечных клеток при атеросклерозе
- Механизм гибели гладкомышечных клеток при атеросклерозе
- Внеклеточный матрикс артерии при атеросклерозе
- Рост сосудов в атеросклеротической бляшке - ангиогенез
- Отложение кальция в атеросклеротической бляшке - минерализация, кальцификация
- Сужение артерии (стеноз) как осложнение атеросклероза
- Тромбоз артерии как осложнение атеросклероза
- Воспаление атеросклеротической бляшки при атеросклерозе как причина осложнений
- Аневризмы артерий как осложнение атеросклероза
