Физиология дыхательной системы у детей
а) Легочные объемы. Ранее предполагалось, что новорожденные имеют меньшую ФОЕ легких на килограмм массы тела по сравнению со взрослыми, пока методы точного микроспирометрического измерения легочных объемов и емкостей новорожденных не показали, что при спонтанном дыхании у новорожденных наблюдается показатель ФОЕ на килограмм массы тела аналогичный таковому для взрослого человека. У взрослого ФОБ — это объем легких, при котором внешняя эластическая тяга грудной клетки равна внутренней эластической тяге легких. Несмотря на то что легкие новорожденных имеют высокую податливость, податливость грудной стенки у них намного выше, чем у взрослого человека.
Внешняя эластическая тяга грудной клетки у новорожденных намного меньше, чем внутренняя эластическая тяга легких, которая стремится уменьшить ФОБ. Новорожденный увеличивает ее с помощью закрытия голосовой щели, а также благодаря стимуляции мышц вдоха во время выдоха. Это приводит к эффекту торможения на выдохе, который в противном случае является пассивным и зависит от эластической тяги легких. Этот эффект был назван активным ФОБ новорожденного.
Тем не менее под общей анестезией (особенно с миорелаксацией) очень податливая хрящевая грудная клетка, слабо развитые мышцы и высокая степень податливости легких новорожденных способствуют спадению легких и формированию ателектазов. Высокая податливость легких у новорожденных частично обусловлена тем, что эластические волокна легких не развиваются до постнатального периода. Точно так же легкие пожилых людей имеют высокую податливость из-за хрупких и нефункционирующих эластических волокон. Таковы основные причины высокого объема закрытия легких у новорожденных и людей пожилого возраста.
Сочетание этих факторов с практически удвоенной скоростью потребления кислорода по отношению к массе тела или площади поверхности (по сравнению со взрослыми) объясняет очень быстрый темп десатурации артериальной крови, возникающей после апноэ у новорожденных (табл. 1).

б) Дыхательные механизмы. При рождении ребенка внутриплевральное давление должно составлять от —30 до —70 см вод.ст., для того чтобы раздуть легкие и начать дыхание. На поздних сроках беременности плод начинает совершать дыхательные движения. Эти движения, как полагают, необходимы для того, чтобы стимулировать развитие мышц и помочь изгнать часть жидкости, производимой легкими. Эта жидкость расширяет дыхательные пути, стимулируя рост и развитие легких, в то же время составляя третью часть от общего объема амниотической жидкости.
Большая часть легочной жидкости выделяется из дыхательных путей с помощью сжимающих сил во время прохождения через родовые пути. В случае кесарева сечения задача аспирации дыхательных путей возложена на неонатолога. Остаточная жидкость покидает легкие через легочные капилляры и лимфатические сосуды в течение первых нескольких дней жизни. Это улучшает податливость легких и снижает затрату сил на дыхание легко утомляющегося новорожденного. Выход из окружения амниотической жидкости во время рождения и последующая потеря воды из всех тканей организма объясняют потерю веса в первые дни после рождения.
в) Контроль дыхания. Ритмичное дыхание при рождении инициируется и поддерживается несколькими факторами, такими как перевязка пуповины и увеличение артериальной концентрации кислорода при дыхании воздухом. Пренатальная гипоксия может вызвать гаспинг-дыхание в утробе матери, приводящее к аспирации мекония, как было указано выше. Это происходит независимо от ритма дыхания. Механизмы, ответственные за контроль дыхания и, особенно, реагирующие на гипоксию, развиваются у новорожденного постепенно и не созревают по крайней мере до 42-44 нед после зачатия. Гипоксия подавляет или нарушает ритмичное дыхание и в утробе матери, и при рождении.
Перевязка пуповины улучшает ритмичность дыхания. Дыхание новорожденного относительно слабо влияет на рaCO2. Новорожденные реагируют на гиперкапнию увеличением активности вентиляции, но в меньшей степени, чем это делают дети старшего возраста. Наклон кривой реакции на CO2 с возрастом увеличивается. У взрослых при гипоксии она смещается влево, а у новорожденных — вправо. Кроме того, нормальный уровень рaCO2 у новорожденных ниже, чем у более старших детей и взрослых.
В течение первых 2—3 нед жизни как доношенные, так и недоношенные дети в теплой среде отвечают на гипоксемию преходящим увеличением активности вентиляции с последующим устойчивым угнетением дыхания. В холодной окружающей среде начальный период преходящего гиперпноэ отсутствует. В три недели гипоксемия у доношенных новорожденных вызывает устойчивое гиперпноэ, как это происходит у взрослых и детей более старшего возраста. У недоношенных детей этот процесс задерживается. В любом возрасте дыхательная активность на фоне гипоксии может быть утрачена при минимальной альвеолярной концентрации ингаляционного анестетика всего лишь 0,1.
Периодическое дыхание, при котором ритмичное дыхание прерывается повторяющимися короткими эпизодами апноэ продолжительностью от 5 до 10 с, обычно возникает у здоровых новорожденных и маленьких грудных детей. Частота встречаемости периодического дыхания у недоношенных новорожденных гораздо выше, чем у доношенных. Тем не менее центральное апноэ новорожденных, длящееся в течение >15 с, сопровождается брадикардией и/или артериальной десатурацией. Центральное апноэ прочно связано со степенью недоношенности и низким весом при рождении (<2 кг). Считается, что причина этого в незрелости механизмов регуляции дыхания. Формирование и созревание центральных и периферических хеморецепторов, а также созревание (и миелинизация) головного мозга новорожденных в целом могут быть причиной недостаточного контроля дыхания.
В связи с риском возникновения жизнеугрожающих эпизодов апноэ в послеоперационном периоде у младенцев и у преждевременно родившихся детей было рекомендовано установить наблюдение после общей анестезии и операции на всю ночь даже для доношенных детей в возрасте до 44—46 нед после зачатия. Эта тема остается спорной среди детских анестезиологов с наиболее консервативным подходом, не позволяющим проводить амбулаторные хирургические операции для детей, рожденных преждевременно (<37 нед), до 60 нед после зачатия (Cote). Была предложена шкала для определения времени оказания хирургической помощи в зависимости от степени недоношенности (табл. 2).
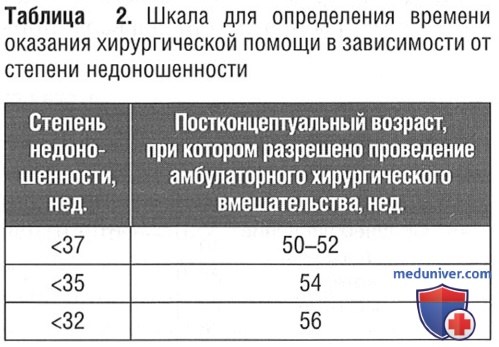
Эти рекомендации дополняются различными критериями, такими как частота эпизодов апноэ и интервал с момента последнего эпизода. Анемия, гипотермия, сопутствующие заболевания и потребность в больших дозах опиоидов в послеоперационном периоде увеличивают риск послеоперационного апноэ. В некоторых случаях допускается выполнение амбулаторного хирургического вмешательства у грудного ребенка, родившегося недоношенным, если родители уже имеют опыт работы с домашним монитором апноэ. Регионарная анестезия (например, спинальная анестезия при паховой грыже) может снизить риск развития послеоперационного апноэ.
в) Сердечно-легочная трансформация. С первым вдохом легкие расправляются воздухом, давление и сопротивление в легочной артерии резко падают, а легочный кровоток заметно увеличивается (рис. 2).
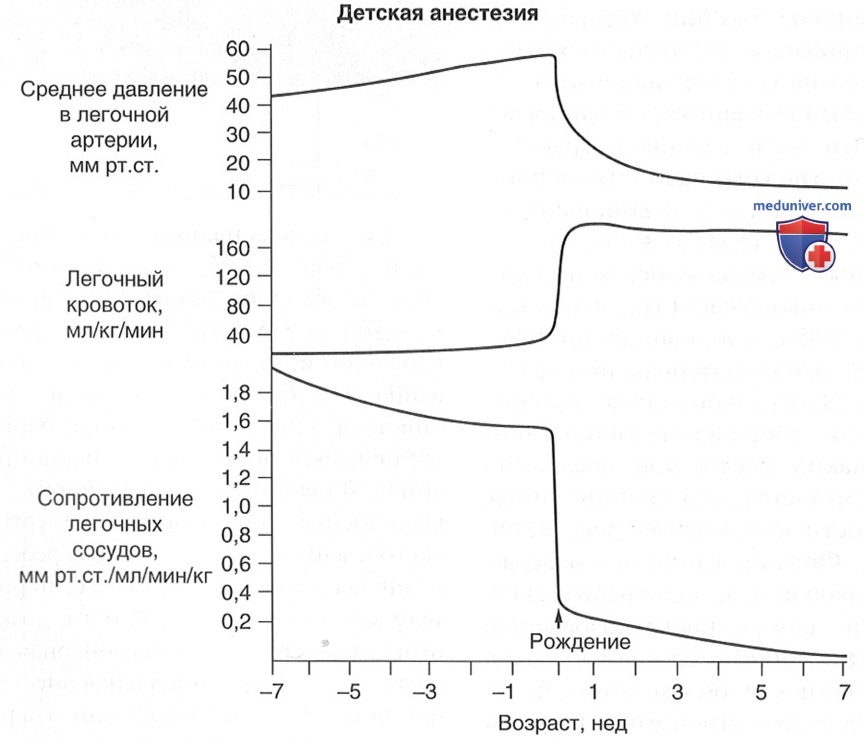
Эти изменения связаны с устранением эффекта гипоксической легочной вазоконстрикции, действующего в спавшихся легких в утробе матери. Первый вдох повышает альвеолярный рO2 и pH, уменьшает рСO2 и количество нерасправленных (ателектазированных) альвеол. Все эти факторы влияют на гипоксическую легочную вазоконстрикцию. Кроме того, эффект связывания при расправлении альвеол приводит к раскручиванию и выпрямлению легочных капилляров так, что стенка каждой альвеолы восстанавливает давление и сопротивление сосудов (около 1000 капилляров для каждой альвеолы). В то же время системное сосудистое сопротивление увеличивается за счет потери низкого сосудистого сопротивления плаценты, которая кровоснабжа-лась параллельно с другими органами тела.
Эти гемодинамические изменения, происходящие в момент рождения (уве личение системного сосудистого сопротивления в сочетании со снижением легочного сосудистого сопротивления и давления), изменяют градиент давления в предсердиях и закрывают овальное отверстие, которое обычно функционирует как односторонний клапан, шунтирующий кровь справа налево.
Анатомическое закрытие овального окна происходит с возрастом, но примерно у 20% 80-летних людей оно может остаться открытым. Такие заболевания легких, как респираторный дистресс-синдром новорожденных, аспирация мекония или врожденная диафрагмальная грыжа (ВДГ), с альвеолярной гипоксией и ателектазами поддерживают высокий уровень гипоксической легочной вазоконстрикции, и овальное окно остается открытым, а кровь шунтируется справа налево.
Резкое увеличение кровотока в сосудах легких при нормальном рождении способствует выделению простагландинов и запуску легочных метаболических механизмов (описываются ниже), которые почти полностью удаляют сосудорасширяющие простагландины Е и F. Уменьшение уровней этих простагландинов, как правило, приводит к закрытию артериального протока, но при необходимости введение новорожденным НПВС (индометацина в США, ибупрофена в Европе) может еще больше снизить уровни простагландинов и привести к закрытию. К сожалению, НПВС повышают риск внутримозгового кровоизлияния. При некоторых «синих» ВПС, таких как атрезия трехстворчатого клапана или легочного ствола, легочный кровоток зависит от функционирования артериального протока, поэтому для поддержания его проходимости необходима инфузия простагландина F2α.
г) Вентиляция. Спонтанная альвеолярная вентиляция у грудных детей (100—150 мл/кг в минуту) примерно в 2 раза больше, чем у взрослых (60 мл/кг в минуту). Значения мертвого пространства (2—2,5 мл/кг) и дыхательного объема (7 мл/кг) на килограмм для младенцев и взрослых сопоставимы. Протективная механическая вентиляция легких (при ИВЛ — дыхательный объем 6—7 мл/кг) оказалась полезной у взрослых пациентов, которым проводится интенсивная терапия. В настоящее время проводится исследование влияния такого режима вентиляции во взрослой хирургии. Этот метод использования низкого дыхательного объема может быть эффективным для педиатрических больных, но может потребоваться проведение искусственных вздохов для уменьшения тенденции к ателектазам.
Дыхательный объем обычно составляет 10—12 мл/кг с соотношением вдох/ выдох 1:2. Создание положительного давления в конце выдоха на 3—5 см вод.ст. также уменьшает вероятность развития ателектазов, но может привести к нежелательному (для хирургов) раздуванию легких во время операций на грудной клетке. Частота вентиляции должна быть установлена на 20—30 вдохов в минуту для грудных детей, 14—20 вдохов в минуту для детей раннего возраста и 14—19 вдохов в минуту для подростков. Грудные дети нуждаются в высокой частоте вентиляции из-за их повышенной потребности в кислороде и нормальной высокой частоте спонтанного дыхания, которая составляет 30-50 вдохов в минуту.
Капнография является стандартным методом мониторинга детей и взрослых во время хирургической операции. рСО2 в конце выдоха обычно меньше артериального рСО2 на 2—3 мм рт.ст., но этот градиент может непредсказуемо увеличиваться в условиях, связанных с повышением альвеолярного мертвого пространства (например, высокое давление в дыхательных путях или низкая перфузия легких). У детей с пороками сердца «синего» типа капнография является ненадежным методом оценки артериального рСО2 (табл. 3).

д) Вентиляция и перфузия. В утробе матери легкие не вентилируются воздухом, и циркуляция обходит легочные сосуды справа налево через шунты овального окна и артериального протока. На момент рождения расправление легких в сочетании с увеличением кровотока приводит к резкому переходу к внематочному газообмену. Вентиляция у новорожденных достаточно хорошо согласована с перфузией, хотя большое количество воды в легких снижает их растяжимость и увеличивает работу дыхания.
Кроме того, быстрое снижение ФОЕ, обусловленное общей анестезией, вызывает вентиляционно-перфузионные нарушения. При шунтировании и артериальной десатурации, возникающей во время ингаляционной индукции у больного ребенка, желательно увеличить FiO2 до 100%. Тем не менее введение 100% кислорода в плохо вентилируемые (но хорошо перфузируемые) альвеолы может быстро привести к исчезновению ателектазов и постоянных шунтов. Растяжение альвеол при вздохе (давление в дыхательных путях — 40—60 см вод.ст.) может уменьшить выраженность шунтирования и улучшить податливость.
е) Транспорт кислорода. У новорожденных сродство крови к кислороду очень высокое (кривая диссоциации оксигемоглобина смещена влево) из-за низкого уровня 2,3-дифосфоглицерата, вследствие чего фетальный гемоглобин плохо взаимодействует с 2,3-дифосфоглицератом. Таким образом, у новорожденного Р50 составляет всего от 18 до 19 мм рт.ст. (у взрослого Р50=27 мм.рт.ст.). В связи с этим рО2 в тканях новорожденных низкое, но это компенсируется физиологически высоким уровнем гемоглобина у новорожденного. Уровни общего и фетального гемоглобина быстро снижаются после рождения, их самые низкие уровни наблюдаются со 2-го по 3-й месяц (так называемая физиологическая анемия грудного возраста).
Этот период анемии, как правило, начинается раньше, более длителен, а наиболее низкий гематокрит у грудных детей наблюдается в случае преждевременного рождения. Уровень Р50 постепенно увеличивается (также растет выработка HbA), достигая своего пика в 10-месячном возрасте (Р50 = 30 мм рт.ст.).
ж) Физиология альвеолоцитов. На уровне альвеолярно-капиллярной мембраны 3 типа клеток играют различные роли в газообмене, защите легких или продукции различных местных и гуморальных веществ. Альвеолоциты I типа — плоские альвеолярные клетки, покрывают около 80% дыхательной поверхности. Их роль в метаболизме довольно ограничена, а при повреждении они замещаются размножающимися альвеолоцитами II типа.
Клетки II типа мультипотентны, вырабатывают разнообразные метаболиты и ферменты в дополнение к выработке сурфактанта. Альвеолярные макрофаги (альвеолоциты III типа) выполняют важную иммунологическую и фагоцитарную защиту легких, реагируют на инфекции и вносят свой вклад в воспалительный ответ.
з) Сурфактант и поверхностное натяжение. Выработка сурфактанта начинается в период между 24—28 нед развития плода, а достижение его адекватных уровней для нормальной функции легких происходит примерно к 35-й неделе. Сурфактант (состоит из 6 липидов и 4 белков, главным образом из дипальмитоилфосфатидилхолина) снижает поверхностное натяжение, работу дыхания и тенденцию к развитию ателектаза. Сурфактант преимущественно уменьшает поверхностное натяжение в маленьких альвеолах (которые в наибольшей степени подвержены спадению) и помогает стабилизировать их. Поверхностное натяжение возникает на границе сред воздух—жидкость и способствует повышению упругости, которая сокращает размер альвеол, что приводит к возникновению ателектазов.
Сурфактант также снижает перемещение жидкости из легочных капилляров в альвеолярные пространства, содержащие воздух. Благодаря этим механизмам сурфактант увеличивает растяжимость легких, уменьшая дыхательную работу для новорожденного. Некоторые белки сурфактанта (SP-A и SP-D) являются опсинами для макрофагов, покрывающими бактерии и вирусы, повышая иммунную функцию.
При большой вероятности преждевременных родов введение матери глюкокортикоидов ускоряет созревание легких плода и увеличивает продукцию эндогенного сурфактанта. Длительный внутриутробный стресс также может ускорить созревание легких плода. Кроме того, синтетический сурфактант или сурфактант животного происхождения можно вводить недоношенным новорожденным через ЭТТ, что может значительно улучшить функции легких и повысить шансы на выживание.
При рождении эффективность вентиляции легких в первую очередь зависит от сокращений диафрагмы, ввиду более позднего развития межреберных мышц. Диафрагма состоит из двух типов мышц: тип 1 — медленно сокращающиеся, устойчивые волокна с низкой утомляемостью, в то время как тип 2 — это быстро сокращающиеся волокна, характеризующиеся быстрым утомлением. Зрелая диафрагма (после 2 лет) на 55% состоит из волокон 1-го типа, в то время как новорожденные имеют только около 25% волокон 1-го типа, а недоношенные дети всего лишь 10%. Таким образом, у новорожденных, особенно у недоношенных, есть риск развития усталости мышц диафрагмы при увеличении работы дыхания.
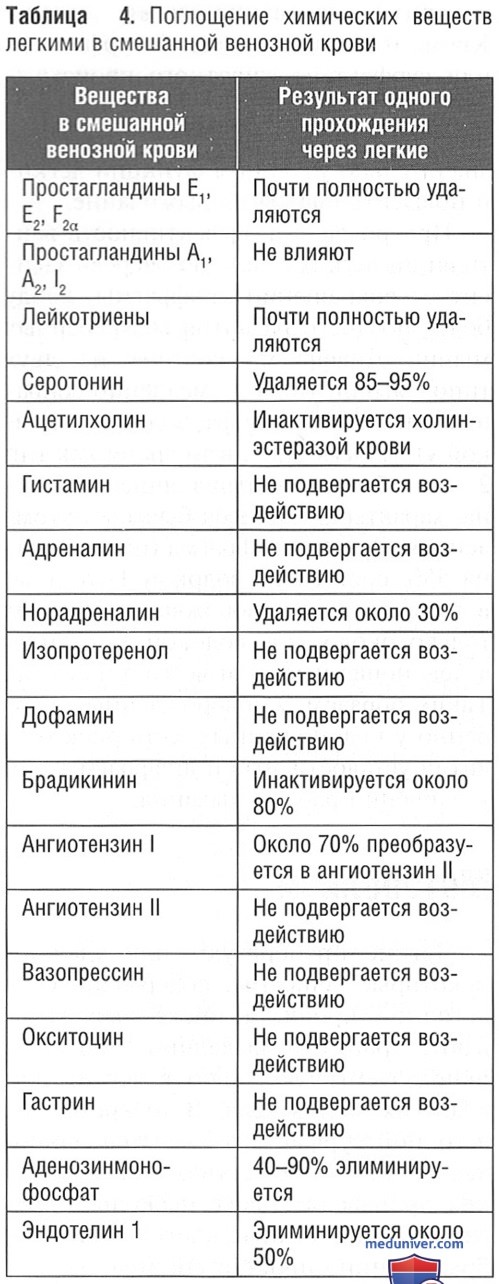
и) Метаболизм. Легкие преобразуют или удаляют некоторые вещества, содержащиеся в легочной крови, а также вырабатывают, хранят и выделяют вещества, используемые локально в легких или в других частях тела. В то время как легочной сурфактант является наиболее значимым веществом, клетки легких производят также несколько других веществ. Тучные клетки выделяют брадикинин, простагландины, лейкотриены, серотонин, лизосомальные ферменты, фактор активации тромбоцитов, хемотаксические факторы нейтрофилов и эозинофилов и гистамин (табл. 4). Вещества, вырабатываемые легкими и выделяемые в дыхательные пути, включают слизь и другие трахеобронхиальные секреты: поверхностные ферменты, белки и иммунологически активные вещества, такие как опсины. Эти вещества вырабатываются клетками подслизистых желез, бокаловидными клетками, клетками Клара и макрофагами.
Эндотелий сосудов легких почти полностью удаляет простагландины Е1, Е2, F2α (это способствует закрытию артериального протока у новорожденных) и лейкотриены при первом прохождении. Эндотелии 1 удаляется почти на 50%, в то время как 80—90% брадикинина инактивируется при первом прохождении через легкие. Удаляется 30% норадреналина, в то время как 70% ангиотензина I при первом прохождении преобразуется в ангиотензин II. Простагландины А1, А2, простациклин, адреналин и дофамин в легких не изменяются. Таким образом, некоторые вещества могут быть удалены из крови, поступающей в легкие, и затем опять попадают в кровь при продукции различными клетками.
В целом метаболизм у детей быстрее, чем у взрослых. Взрослые потребляют 3—3,5 мл О2/кг в минуту, в то время как у новорожденных потребление кислорода примерно в 2 раза больше (7—9,5 мл О2/кг в минуту). Это один из факторов, который приводит к очень быстрому снижению сатурации оксигемоглобина при развитии у ребенка апноэ.
- Читать далее "Обструкция дыхательных путей при анестезии у детей"
Редактор: Искандер Милевски. Дата публикации: 6.11.2022
- Фармакокинетика и фармакодинамика седативных, анксиолитиков у детей
- Фармакокинетика и фармакодинамика противорвотных препаратов (антиэметиков) у детей
- Фармакокинетика и фармакодинамика ингаляционных анестетиков у детей
- Фармакокинетика и фармакодинамика местных анестетиков у детей
- Фармакокинетика и фармакодинамика миорелаксантов у детей
- Фармакокинетика и фармакодинамика препаратов влияющих на симпатическую, парасимпатическую нервную систему у детей
- Фармакокинетика и фармакодинамика препаратов влияющих на коагуляцию у детей
- Пренатальное и постнатальное развитие дыхательной системы
- Физиология дыхательной системы у детей
- Обструкция дыхательных путей при анестезии у детей
