Сочетание стентирования и тромболитической терапии при инфаркте миокарда
а) Спасительное стентирование (чрескожное коронарное вмешательство, ЧКВ). Несмотря на увеличение случаев применения первичного ЧКВ, большинство пациентов получает реперфузионную ТЛТ. Имеется небольшое количество данных относительно значимости спасительного ЧКВ у пациентов, у которых ТЛТ была неэффективна.
Рандомизированное исследование больных с передним ИМ (n = 151) показало снижение 30-суточной комбинированной конечной точки, включающей СН и смерть (6,4% vs 16,6%, р = 0,05). В объединенном анализе нескольких небольших исследований были отмечены снижение числа случаев СН и улучшение выживаемости в течение 1 года больных со средним и большим ИМ.
В более позднем исследовании MERLIN (Middlesbtough Early Revascularization to Limit Infarction) рандомизировали на спасительное ЧКВ и консервативную терапию 307 пациентов со снижением подъема сегмента ST < 50% через 60 мин после введения стрептокиназы. Не было получено достоверной разницы в первичной конечной точке (смерть).
Последующая реваскуляризация была меньше (6,5% vs 20,1%, р < 0,01) в группе спасительного ЧКВ (стенты — 50%; ингибиторы рецепторов гликопротеина IIb/IIIа — 3%), но в группе ЧКВ было больше МИ (4,6% vs 0,6%, р < 0,03). Следует отметить, что применение ингибиторов рецепторов гликопротеина IIb/IIIа и стентирования привело к более значительному количеству спасенного миокарда по сравнению с баллонной ангиопластикой (n = 181; индекс сохраненного миокарда 0,35 vs 0,25, р = 0,005).
Недавно опубликованы результаты исследования REACT, в котором 427 пациентов после неэффективной ТЛТ (снижение подъема сегмента ST < 50% за 90 мин) были рандомизированы на консервативное лечение, повторную ТЛТ и спасительное ЧКВ (88% — стенты).
Хотя различий в показателях смертности не было, 6-месячный период без сердечно-сосудистых событий (СССоб) был больше в группе спасительного ЧКВ (84,6% vs 70,1% для консервативного лечения и 68,7% для повторной ТЛТ, р = 0,004).
Ошибки неинвазивной оценки состояния перфузии инфаркт-связанной коронарной артерии (КА) остаются серьезным ограничением данного подхода. Комплексная оценка клинической картины, определение биомаркеров в начале ИМ и через 60 мин, снижение подъема сегмента ST могут улучшить точность прогноза.
Считается, что лучше иметь клинические подозрения и направить пациента на ангиографию до появления нестабильности гемодинамики. Современные руководства рекомендуют спасительное ЧКВ для пациентов с кардиогенным шоком и СН и с меньшим уровнем доказательности — для пациентов с электрической нестабильностью или стойкой ишемией. Кроме этого, результаты недавних исследований свидетельствуют о необходимости такого подхода и к пациентам с признаками сохраняющейся ишемии.
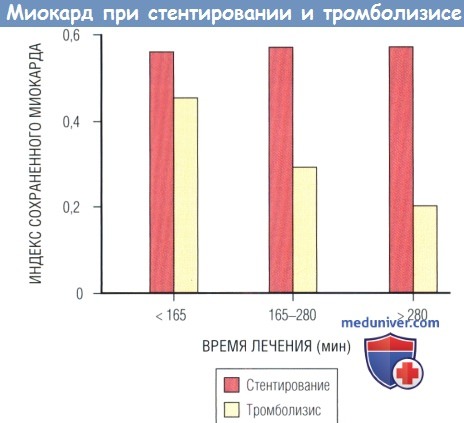
Было отмечено уменьшение индекса сохраненного миокарда в зависимости от времени в группе ТЛТ (р = 0,03), но не в группе стентирования (р = 0,59).
б) Упрощенное стентирование (чрескожное коронарное вмешательство, ЧКВ). Совершенствование ТЛТ и ЧКВ привело к комбинированию этих методов при лечении ОИМ с целью восстановления просвета коронарной артерии (КА) и уменьшения риска ишемии. Однако несколько исследований, выполненных за последние 10 лет, продемонстрировали неблагоприятный результат ангиопластики, проведенной непосредственно после ТЛТ: наблюдалось значительно больше кровотечений, повторных ишемий, КШ и летальных исходов.
Эти события возникали из-за вызванной ТЛТ активации тромбоцитов и/или обширного внутрисосудистого кровоизлияния. Современные методы ангиопластики улучшили безопасность процедуры в этом отношении. В исследованиях T1MI-10B (тенектеплаза vs ТАП) и TIMI-14 (уменьшенная доза ТАП и/или абциксимаб) у пациентов, подвергшихся дополнительному или отсроченному вмешательству (стенты в > 60% случаев), мультивариабельный анализ выявил более низкую 30-суточную смертность и/или более низкий риск реинфаркта по сравнению с пациентами с успешной ТЛТ (кровоток TIMI-3 в течение 90 мин) без вмешательства.
Мощный толчок к продолжению фармакоинвазивной стратегии лечения ИМ дали результаты исследований, показавших улучшение выживаемости пациентов высокого риска со спонтанной реперфузией (кровоток TIMI-3) до первичного ЧКВ. Действительно, достижение эффективного раннего восстановления коронарного кровотока у пациентов в течение 2-3 час от начала ИМ приводит к спасению большей части миокарда и росту благоприятных исходов, особенно у доставленных в больницу пациентов. Это обстоятельство стимулировало дальнейшее развитие понятия «упрощенная ангиопластика», которая сочетает в себе преимущества фармакологической реперфузии относительно скорости эффекта и безопасность механического воздействия для полноценного восстановления просвета КА.
Предварительные исследования с полной или уменьшенной дозой тромболитиков с ингибиторами рецепторов гликопротеина IIb/IIIa или без них подтвердили возможность достижения кровотока TIMI-3 при первичной ангиографии. В крупномасштабном исследовании упрощенного ЧКВ ASSENT-4 рандомизировали 1667 пациентов (< 6 час от начала заболевания) на первичное ЧКВ и первичное ЧКВ с предшествующей полной дозой тенектеплазы. Несмотря на большее количество лиц с кровотоком TIMI-3 до ЧКВ (43% vs 15%, р < 0,001) в группе ТЛТ, исследование было завершено досрочно из-за увеличенной смертности в группе упрощенного ЧКВ (6% vs 3%, р = 0,01).
Кроме того, первичная конечная точка (СН, шок или смерть в течение 90 сут) была выше в группе упрощенного ЧКВ (19% vs 13%, р = 0,0045). В этой же группе также было значительно больше МИ (1,8% vs 0%, р < 0,0001) и ишемических осложнений (реинфаркты 6% vs 4%, р = 0,03). В большом исследовании FINESSE (Facilitated Intervention with Enhanced Reperfusion Speed to Stop Events) сравнивают раннее применение абциксимаба vs уменьшенная доза ретеплазы плюс абциксимаб vs абциксимаб и ЧКВ (отбор пациентов в это исследование продолжается). Исследование BRAVE (n = 253) сравнило применение 1/2 дозы ретеплазы и абциксимаба vs один абциксимаб перед ЧКВ и не выявило различий в размере ИМ и клинических исходах.
Недавний метаанализ 17 исследований упрощенного ЧКВ (включая ASSENT-4) показал, что, хотя упрощенное ЧКВ более чем в 2 раза увеличивает начальный кровоток TIMI-3, после ЧКВ кровоток не отличается (89% vs 88%) по сравнению с первичным ЧКВ [100]. Показатели смертности (5% vs 3%, р = 0,04), РСМ (4% vs 1%, р = 0,01), массивных кровотечений (7% vs 5%, р = 0,01) и МИ (1,1% vs 0,3%, р = 0,0008) были значительно выше в группе упрощенного ЧКВ. Неблагоприятные исходы наблюдались у пациентов, получавших тромболитик, в то время как применение одного ингибитора гликопротеина IIb/IIIa не приводило к неблагоприятным результатам.
Геморрагические осложнения, связанные с применением тромболитика (местное артериальное, миокардиальное и церебральное повреждения) и фактором времени (позднее обращение, длительность тромболитического эффекта), взаимодействуют при таком подходе, по-видимому, неблагоприятно. Имеющиеся данные не подтверждают обоснованность комбинации ТЛТ с упрощенным ЧКВ.
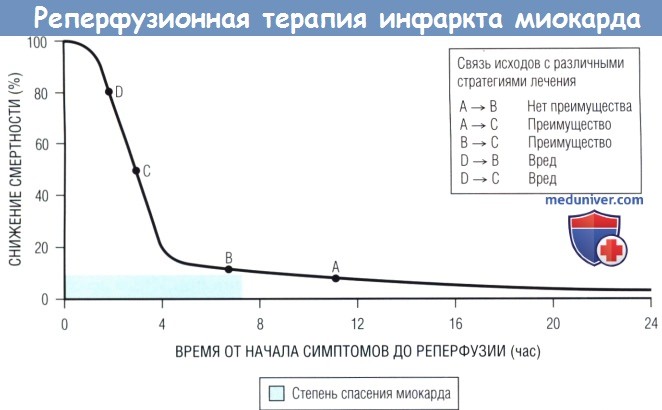
Наиболее вероятный результат вмешательства — спасение миокарда.
На длительность этого раннего критинеского периода могут повлиять такие факторы, как наличие функционирующих коллатералей коронарных артерий,
предшествующая ишемия, потребность миокарда в кислороде и продолжительность ишемии.
По прошествии этого раннего периода преимущество реперфузионной терапии в отношении смертности резко уменьшается (кривая снижения смертности сглаживается),
и фактор времени проведения реперфузии становится менее важным.
Преимущество при смещении от точки А или В к точке С будет значительным, а при смещении от точки А к точке В — небольшим.
Лечебная стратегия, отдаляющая начало терапии в ранний критический период, например транспортировка пациента для проведения ЧКВ, может приносить вред (смещение от точки D к точке С или В).
в) Дополнительное стентирование (чрескожное коронарное вмешательство, ЧКВ) после успешного тромболизиса. Как было отмечено ранее, после успешного тромболизиса в большинстве артерий сохраняется существенный остаточный стеноз. Реинфаркты после тромболизиса характеризуются увеличенной смертностью и являются непредсказуемыми событиями. Ранние исследования, оценивавшие эффективность рутинной баллонной ангиопластики, проведенной через несколько часов или суток после успешной ТЛТ, не выявили преимуществ в отношении реинфарктов, функции ЛЖ или выживаемости.
У пациентов со спонтанной или провоцируемой ишемией после тромболитической терапии (ТЛТ) меньше повторных ИМ или эпизодов ишемии после ЧКВ. В связи с этим в современных руководствах рекомендуется проведение дополнительного ЧКВ пациентам после ТЛТ при повторном ИМ, провоцируемой ишемией, или находящимся в шоке (класс IIа) и предлагают рассматривать это вмешательство для пациентов с СИ, ФВ ЛЖ < 40% или серьезными желудочковыми аритмиями.
Усовершенствование техники ЧКВ позволило пересмотреть рутинный подход к пациентам после успешной ТЛТ. Например, в исследованиях TIMI-4, TIMI-10B и TIMI-17 проведение ЧКВ после тромболизиса снижало риск реинфарктов и двухлетнюю смертность. В исследовании GRACIA-1 (GRupo de Analisis de la Cardiopatia Isque'mica Aguda) 500 пациентов были рандомизированы на ангиографию и дополнительное ЧКВ со стентированием и абциксимабом через 6-24 час после ТЛТ или консервативное лечение.
Стентирование артерий было выполнено в 80% случаев в группе инвазивного лечения и в 20% — в группе консервативного лечения. Через 1 год первичная конечная точка, включавшая реинфаркт, реваскуляризацию и смерть, была меньше (9% vs 21%, р = 0,0008) в группе инвазивной терапии. В группе консервативного лечения количество внеплановых реваскуляризаций за время госпитализации в связи со спонтанной ишемией было в 5 раз выше. Хотя это исследование не выявило преимуществ в выживаемости больных, оно показало, что современное дополнительное ЧКВ как часть посттромболитической инвазивной стратегии может быть безопасным и полезным для пациентов.
- Читать "Плюсы и минусы первичного стентирования при инфаркте миокарда"
Оглавление темы "Инфаркт миокарда и нестабильная стенокардия.":- Клеточные технологии при инфаркте миокарда
- Сочетание стентирования и тромболитической терапии при инфаркте миокарда
- Плюсы и минусы первичного стентирования при инфаркте миокарда
- Показания для первичного стентирования с фибринолизом при инфаркте миокарда
- Показания для стентирования после фибринолиза при инфаркте миокарда
- Показания для позднего стентирования при инфаркте миокарда после госпитализации
- Требования к врачу, отделению для стентирования (чрескожного коронарного вмешательства, ЧКВ)
- Определение и классификация нестабильной стенокардии по Браунвальду
- Патогенез нестабильной стенокардии
- Клиника и ЭКГ при нестабильной стенокардии
