Влияние альдостерона на развитие сердечно-сосудистых заболеваний
Альдостерон — это минералокортикоидный гормон, вырабатываемый надпочечниками. Секреция альдостерона регулируется в первую очередь ренин-ангиотензиновой системой, а также другими факторами, такими как сывороточные уровни натрия, калия и АКТГ. Функция минералокортикоидных гормонов состоит в поддержании нормальной концентрации натрия и калия, а также оптимальной степени гидратации.
Все больше данных показывают, что РААС играет значительную роль в развитии ожирения, дислипидемии, ИР, ХБП и артериальной гипертензии, в патогенезе метаболического синдрома (Sowers и соавт., 2009).
Недавно было продемонстрировано прямое влияние повышенного уровня альдостерона плазмы крови на ИР, эндотелиальную дисфункцию, гиперфильтрацию клубочков и избыточную секрецию альбумина через клубочки и канальцы почек, что приводит к неадекватному функционированию сердечно-сосудистой системы и ремоделированию почек.
Кроме того, у пациентов с резистентной артериальной гипертензией все чаще отмечается тенденция к избыточной массе тела и выявляется повышение уровня альдостерона в плазме крови и моче.
Альдостерон проявляет свои геномные эффекты, связываясь с МКР; с другой стороны, альдостерон оказывает быстрые негеномные эффекты, которые опосредуют дезадаптивное ремоделирование тканей сердечно-сосудистой и центральной нервной системы, что еще больше усугубляет метаболический синдром, ИР и гипертонию.
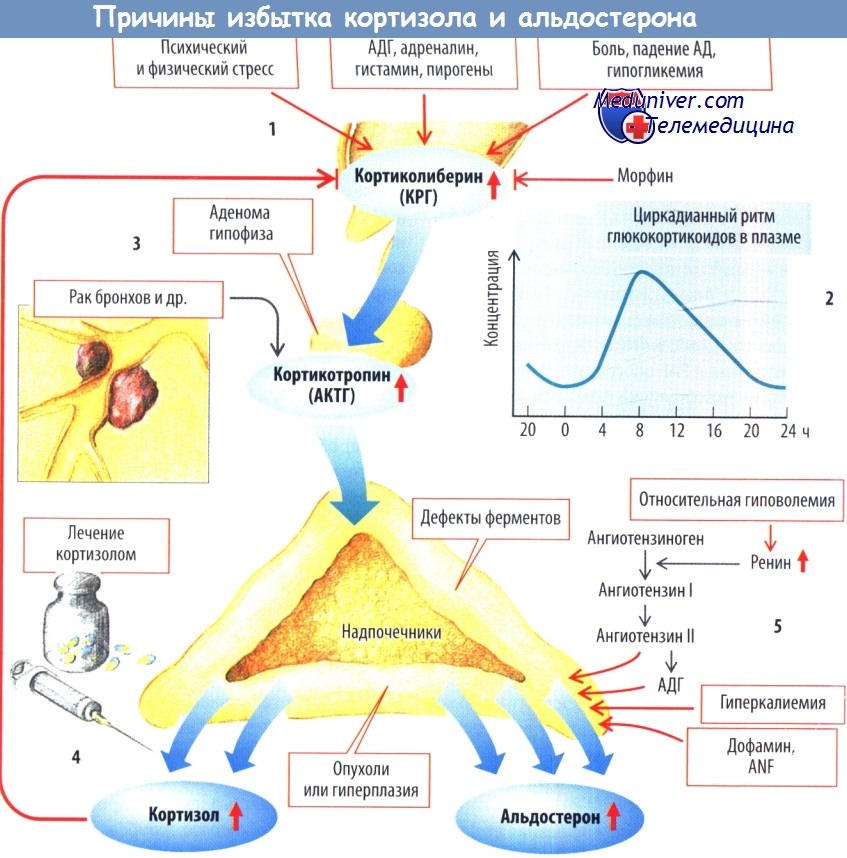
а) Альдостерон и инсулинорезистентность. Считается, что секреция альдостерона надпочечниками регулируется активацией РААС в ответ на снижение внутрисосудистого объема. При некоторых заболеваниях, включая метаболический синдром, сердечную недостаточность и ХБП, нормальное функционирование этой системы нарушается, что сопровождается неадекватной секрецией альдостерона, несмотря на усиленную задержку соли и жидкости, приводя к развитию гиперальдостеронизма (Whaley-Connell и соавт., 2010).
Повышенная стимуляция МКР в ответ на высокий уровень альдостерона играет роль в развитии ИР и других компонентов метаболического синдрома. Фактически МКР имеет высокое сродство как к альдостерону, так и к 11-β-гидроксиглюкокортикоидам, уровни которых часто повышаются при ожирении — типичном признаке метаболического синдрома. Поскольку при метаболическом синдроме уровень циркулирующих ГКС может быть на несколько порядков выше, чем уровень альдостерона, вполне вероятно, что 11-β-гидроксиглюкокортикоиды связываются с МКР вместо альдостерона, влияя таким образом на метаболизм инсулина.
Было показано, что жировая ткань продуцирует жирорастворимый фактор, который стимулирует секрецию альдостерона. Более того, как альдостерон, так и ГКС могут оказывать свое действие, связываясь с МКР, что стимулирует адипогенез и увеличивает инфильтрацию жировой ткани макрофагами. Таким образом, взаимодействие жировой ткани, коры надпочечников и альдостерона/глюкокортикоидов способствует дальнейшему адипогенезу и развитию воспаления в жировой ткани.
Это означает, что в клинических условиях, при которых наблюдается повышение образования жировой ткани, активация МКР ГКС в дополнение к альдостерону усиливает воспаление, окислительный стресс, фиброз и ИР (Fallo и соавт., 2006).
Первичный гиперальдостеронизм — это группа состояний, характеризующихся избыточной продукцией альдостерона, что приводит к подавлению РААС. Основным проявлением первичного гиперальдостеронизма является артериальная гипертензия, а его распространенность среди пациентов с гипертонической болезнью составляет 0,5—4,8%. Также для этого заболевания характерно истощение запасов калия. Наиболее частыми причинами первичного гиперальдостеронизма являются односторонняя автономно функционирующая аденома коры надпочечников и односторонняя или двусторонняя гиперплазия коры надпочечников.
Редкой причиной первичного гиперальдостеронизма является наследственное заболевание, известное как глюкокортикоид-подавляемый гиперальдостеронизм (ГПГА).
б) Альдостерон и функция эндотелия. Эндотелиальная дисфункция обычно сочетается с ИР и другими метаболическими изменениями. У пациентов с ожирением и инсулинорезистентностью наблюдается ряд нарушений обменных процессов в сосудах. Они включают нарушение стимулируемого инсулином захвата глюкозы и снижение содержания биодоступного NO. В этом контексте инсулинозависимая утилизация глюкозы частично зависит от инсулин-опосредованного увеличения кровотока и доставки субстрата к тканям.
При ИР наблюдается снижение стимуляции инсулином биологической активности NO, уменьшение вазодилатации и нарушение доставки необходимых веществ. Все больше данных говорят о том, что повышенный уровень альдостерона в плазме приводит к снижению активности сигнальной инсулиновой системы в тканях сосудов. Пациенты с ИР, ожирением и повышенным уровнем альдостерона в плазме крови более склонны к развитию эндотелиальной дисфункции вследствие увеличения образования активных форм кислорода (АФК), активирующих чувствительные к окислению сериновые киназы, которые способствуют фосфорилированию серина инсулинового рецептора-1, что приводит к снижению его взаимодействия с фосфоинозитол-3-киназой, с последующим уменьшением уровня протеинкиназы В и атипичной активацией фосфорилирования эндотелиальной синтазы азота.
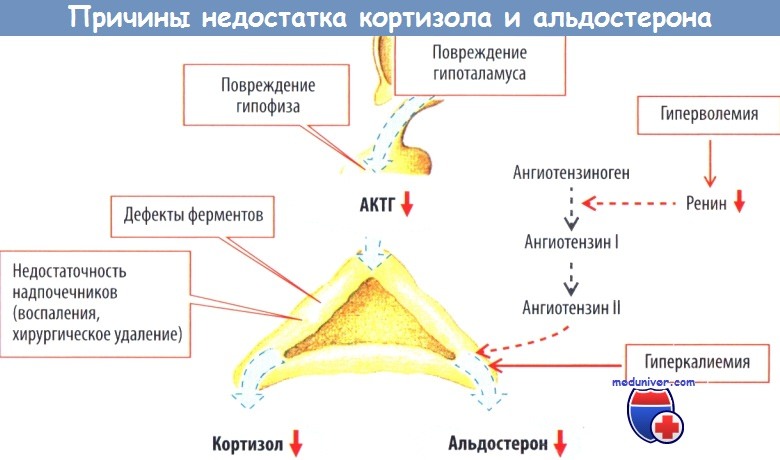
в) Альдостерон и артериальная гипертензия. У пациентов с повышенным артериальным давлением отмечается повышение уровня альдостерона в плазме крови, который коррелирует с увеличением массы миокарда левого желудочка, а также сам по себе является фактором риска развития гипертонии.
Первичный гиперальдостеронизм, возникший в результате двусторонней гиперплазии надпочечников или альдостерон-продуцирующей аденомы, встречается с распространенностью от 0,5% до 4,8% среди пациентов с артериальной гипертензией и от 4,5% до 22% среди пациентов с резистентной гипертензией.
Повышение уровня альдостерона в сочетании с ожирением и ИР приводит к негеномным эффектам, ответственным за развитие воспаления и окислительного стресса, которые способствуют появлению резистентной гипертензии. Помимо способности ингибировать эндотелий-зависимую релаксацию за счет снижения биодоступности NO, периваскулярный фиброз, вызванный альдостероном, снижает эластичность сосудов и увеличивает их жесткость, тогда как повышенный обмен Na+/H+ способствует пролиферации гладкомышечных клеток сосудов.
Это приводит к повышению артериального давления, которое возникает из-за классических эффектов альдостерона, способствующих удержанию солей и увеличению объема циркулирующей крови, вызывая тяжелую гипертензию.
Механизмы, способствующие развитию гипертензии, включают увеличение объема плазмы крови из-за задержки натрия и жидкости и сужение сосудов из-за дефицита калия. Было показано, что альдостерон снижает биодоступность NO, тем самым подавляя эндотелий-зависимую релаксацию. Опосредованный альдостероном периваскулярный фиброз снижает эластичность сосудов.
г) Альдостерон и структура сердца. При гиперальдостеронизме развивается неадекватное ремоделирование сердца, гипертрофия левого желудочка (ГЛЖ), сердечный фиброз и диастолическая дисфункция. ГЛЖ, наблюдаемая при первичном гиперальдостеронизме, более выражена по сравнению с гипертрофией на фоне гипертонии. Было также показано, что альдостерон способствует отложению коллагена, активирует воспалительные клетки и стимулирует пролиферацию фибробластов.
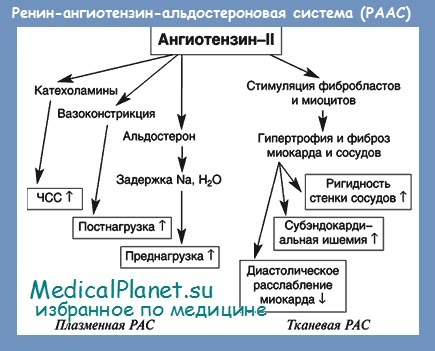
д) Альдостерон и хроническая сердечная недостаточность. Уровень альдостерона может повышаться при сердечной недостаточности и инфаркте миокарда, что вносит свой вклад в патологическое ремоделирование сердечно-сосудистой системы за счет прямого воздействия на отложение коллагена и, как следствие, развитие сердечно-сосудистого фиброза. Повышенный уровень альдостерона также способствует развитию дисфункции эндотелия и сосудистого воспаления. Терапия антагонистами альдостерона рекомендуется пациентам с умеренно выраженными или выраженными симптомами сердечной недостаточности и снижения фракции выброса ЛЖ или с дисфункцией ЛЖ в раннем периоде после инфаркта миокарда.
1. Феохромоцитома. Феохромоцитома — это катехоламин-продуцирующее образование из хромофинных клеток мозгового вещества надпочечников и симпатических ганглиев (катехоламин-секретирующие параганглиомы или вненадпочечниковые феохромоцитомы). В ряде случаев заболевание может протекать бессимптомно, в этом случае диагноз ставится по результатам лабораторного обследования, визуализирующего исследования надпочечников или генетического тестирования. Среди частых проявлений заболевания у пациентов можно выделить артериальную гипертензию (эпизодическую или стойкую) и пароксизмальные симптомы, такие как головокружение, головную боль, «приливы», потоотделение и сердцебиение.
Стойкая или пароксизмальная артериальная гипертензия присутствует более чем у 50% пациентов с феохромоцитомой. У пациентов с феохромоцитомой была продемонстрирована более высокая вариабельность артериального давления по сравнению с пациентами с гипертонической болезнью, которая также ассоциирована с более высокой частотой поражения органов-мишеней.
Также могут наблюдаться маркеры эндотелиальной дисфункции, такие как увеличение толщины комплекса интима-медиа сонной артерии. Эти изменения связаны с влиянием избытка катехоламинов на рост и утолщение сосудистой стенки. Было показано, что в условиях нормализации уровней катехоламинов после хирургического удаления феохромоцитомы снижается толщина комплекса интима-медиа сонной артерии и регрессирует фиброз стенки сонной артерии.
Действие избытка катехоламинов также может привести к кардиомиопатии, ишемической болезни сердца, «оглушению» миокарда и в редких случаях к кардиогенному шоку. У пациентов с кардиомиопатией, ассоциированной с феохромоцитомой, может наблюдаться отек легких, острая боль в груди и ишемия/инфаркт миокарда. Отек легких является результатом повышения проницаемости легочных капилляров, сопротивления периферических сосудов и гидростатического давления, а также переполнения или сужения эфферентных легочных вен.
Ишемия или инфаркт миокарда могут быть результатом спазма коронарных артерий, при этом действие катехоламинов приводит к сужению сосудов, снижению коронарного кровотока и увеличению потребности сердца в кислороде.
Было показано, что кардиомиопатия, вызванная катехоламинами, регрессирует после хирургического лечения феохромоцитомы. Вероятность обратного развития кардиомиопатии зависит от раннего выявления и лечения основного заболевания (Lenders и соавт., 2005).
Видео физиология гормонов надпочечника - профессор, д.м.н. П.Е. Умрюхин
- Читать "Влияние паратиреоидного гормона (ПТГ) на развитие сердечно-сосудистых заболеваний"
Редактор: Искандер Милевски. Дата публикации: 25.12.2023
- Влияние АКТГ и кортизола на развитие сердечно-сосудистых заболеваний
- Влияние альдостерона на развитие сердечно-сосудистых заболеваний
- Влияние паратиреоидного гормона (ПТГ) на развитие сердечно-сосудистых заболеваний
- Влияние дисбактериоза на развитие сердечно-сосудистых заболеваний
- Взаимосвязь между сахарным диабетом и артериальной гипертензией
- Взаимосвязь между щитовидной железой и артериальной гипертензией
- Взаимосвязь между минералкортикоидами, глюкокортикоидами и артериальной гипертензией, гипотензией
- Взаимосвязь между соматотропным гормоном (СТГ) и артериальной гипертензией
- Взаимосвязь между гиперпаратиреозом, витамином Д и артериальной гипертензией
- Взаимосвязь между половыми гормонами и артериальной гипертензией
- Гипофиз как причина болезни сердца
