Симбиотическая микрофлора человека в норме
Фундаментальные представления о значимости микробов-симбионтов для организма человека были заложены в трудах отечественных и зарубежных ученых еще в XIX столетии. Интерес к этой проблеме просуществовал до начала эры антибиотиков, затем несколько угас, но по мере расширения использования химиопрепаратов в медицинской практике, возник с новой силой, когда врачи начали сталкиваться с их побочными эффектами, выражающимися в подавлении нормальной микрофлоры. Изучение жизнедеятельности микробов-симбионтов позволяло сформировать более адекватные представления о биологических законах, лежащих в основе взаимоотношений организма хозяина и населяющей его микрофлоры.
Нормальная микрофлора — продукт интеграции человека с внешней средой. Она сформировалась и закрепилась в организме человека в процессе его эволюции. Можно сказать, что эволюция человеческого организма и окружающих и населяющих его живых существ шла параллельно. Менялся человек, менялись его физиологические и морфологические характеристики — изменялась среда обитания для его симбиотической микрофлоры. Вследствие этого появлялись популяции и сообщества микроорганизмов с новыми свойствами, приспособленными к изменившемуся человеку. В свою очередь, микроорганизмы постоянно воздействовали на организм хозяина и тот вынужден был приспосабливаться к их присутствию. Взаимная эволюция человека и его микрофлоры привела в конечном итоге к формированию сложной динамической системы. Произошло переложение ряда функций хозяина на его симбиотическую микрофлору. Простое сожительство макро- и микроорганизмов превратилось в прочный симбиоз. Недаром симбиотическую флору часто называют внешним органом человека.
Для лучшего понимания материала, который будет излагаться ниже, необходимо остановиться на основных терминах, принятых в экологии.
Формирование нормальной микрофлоры человека начинается с его контаминации микрофлорой родовых путей матери в процессе родов. Вначале поверхность тела и слизистые оболочки заселяются микроорганизмами родовых путей матери и ближайшего окружения внешней среды — рук персонала и матери, пеленок и воздушной среды палат. В течение первых нескольких дней микроорганизмы пока еще хаотично заселяют новорожденных и представляют в основном состав той флоры, которая окружает ребенка. Довольно скоро, по мере того как новорожденный соприкасается со все большим числом различных видов микроорганизмов, между последними начинают проявляться конкурентные взаимоотношения, благодаря которым будущие биотопы заселяются характерной для них микрофлорой и постепенно формируются биоценозы, свойственные взрослому организму. Различия в микробном населении различных биотопов обусловлены неодинаковыми анатомическими, физиологическими и биохимическими особенностями тех органов и систем, которые их образуют. Фактически процесс формирования нормальной микрофлоры представляет собой микробную сукцессию. Она лежит в основе становления микрофлоры для всех нестерильных областей тела человека.
а) Микрофлора кожи, уха и конъюнктивы. К важнейшим факторам, определяющим состав микрофлоры кожи, относятся ее pH (около 5,6), влажность, неодинаковая в различных участках кожи, выделение кожного сала и пота. Выделяют три главных региона, различающихся по составу флоры: 1 — подмышечная и перинеальная области, межпальцевые пространства; 2 — кисти рук, лицо и пуповина; 3 — руки и ноги. Микроорганизмы распределятся на коже неравномерно и образуют скопления в виде микроколоний. Колонии могут различаться по размеру. Наиболее многочисленна микрофлора промежности и подмышечной области. Число микроорганизмов здесь может достигать 106/см2. Микрофлору кожи составляют коагулазонегативные стафилококки (Staphylococcus epidermidis, S. capitis, S. warneri, S. hominis, S. haemolyticus, S. lugdunensis, S. auriculans), микрококки (в основном M. luteus), коринебактерии и пропионибактерии. Могут также встречаться гемолитические стрептококки, атипичные микобактерии и бациллы. Среди грамотрицательных микроорганизмов наиболее часто высеваются ацинетобактеры (до 25%), значительно реже — протеи, псевдомонады, энтеробактеры и клебсиеллы. Грибковая флора, в основном, представлена липолитическими дрожжами рода Malassezia, частота выделения которых достигает 100%. Могут также встречаться грибы рода Candida. Несмотря на то что кожа представляет собой открытый биотоп, здесь преобладают анаэробные виды, главным образом пропионибактерии, которые локализуются в толщине кожи.
Микрофлора наружного уха также очень напоминает микрофлору кожи. Здесь преобладают коагулазонегативные стафилококки и корииебактерии. Реже выделяются бациллы, микрококки, непатогенные нейссерии и микобактерии. Среди грибов встречаются Aspergillus, Altemaria, Penicillium и Candida.
Микрофлора конъюнктивы здоровых индивидуумов в основном представлена видами, встречающимися на коже: коагулазонегативными стафилококками, корино-бактериями, непатогенными нейссериями и зеленящими стрептококками.
б) Микрофлора респираторного тракта. Полость носа относительно бедна микрофлорой. Вместе с воздухом в носовую полость могут проникать самые различные бактерии, вирусы и грибы, в том числе патогенные и условно-патогенные. Часть этих микроорганизмов удаляется с выдыхаемым воздухом, часть — при чихании. Подавляющее их число не задерживается в полости носа и является транзиторной флорой этого биотопа у здорового человека. Только приблизительно около одного сантиметра наружных носовых ходов, как и кожа ходов, покрытых ороговевающим эпителием, может постоянно или длительно заселяться Staphylococcus aureus. Около 30 % населения являются носителями этого вида стафилококков: 15% постоянными и 15% транзиторными.
Колонизация носоглотки новорожденных в первые часы и дни жизни осуществляется, главным образом, за счет тех лиц, которые имеют наиболее близкий контакт с ними (матери, обслуживающий персонал родильных домов, другие дети). Нормальная микрофлора у детей формируется в течение нескольких месяцев и остается неизменной в течение жизни. Среди нормальной микрофлоры преобладают зеленящие стрептококки различных видов, непатогенные нейссерии и гемофильные бактерии, в основном, Haemophilusparainfluenzae, и коринеформные виды. Значительно реже выделяются стафилококки и микрококки. На слизистой оболочке носоглотки может формироваться носительство Neisseria meningitidis, Streptococcus pneumoniae и H. influenzae.
Сложнее состав микрофлоры ротоглотки (зева), так как последняя анатомически представляет собой более расширенный биотоп — перекрест респираторного и интестинального трактов. К микроорганизмам, перечисленным выше, добавляются представители семейства Enterobacteriaceae, энтерококки, лактобациллы, дрожжевые грибы. Частота выделения этих видов у здоровых людей сравнительно невысокая. Она возрастает после приема пищи, что позволяет их рассматривать в качестве транзиторных микроорганизмов. Из лакун миндалин и слизистой сумки, расположенной на задней стенке глотки, могут выделяться анаэробные бактерии: бактероиды, пептострептококки и др.
От проникновения микроорганизмов в нижние отделы глотки, трахею и бронхи предохраняет надгортанник, а также движение ресничек на слизистой бронхов, осуществляющих очистительную функцию. Попадающие сюда с вдыхаемым воздухом микроорганизмы постепенно удаляются или уничтожаются макрофагами. Мелкие бронхиолы и ацинусы легких в норме стерильны. Примыкающие к глотке синусы также обычно стерильны.
в) Микрофлора желудочно-кишечного тракта. Заселение слизистой полости рта новорожденных начинается сразу после рождения. Микроорганизмы из его ближайшего окружения колонизируют полость рта особенно активно в течение первых 6-10 часов после рождения. Большая их часть оказывается лишь транзиторными видами, так как не находит здесь подходящих условий для своего существования. Большинство микроорганизмов, приживляющихся на слизистой полости рта, принадлежит к резидентной (местной) микрофлоре рта матери и других лиц из окружения новорожденного. В дальнейшем происходит микробная сукцессия под влиянием различных внешних воздействий: смена окружающей среды, контакта с другими членами семьи, разнообразного питания, контакта с посудой и т.д. Помимо внешних воздействий, на процесс микробной сукцессии в полости рта существенное влияние оказывает прорезывание зубов у детей и переход на твердую пищу. Формируется микрофлора зубной пленки и микрофлора зубных карманов. В первые месяцы жизни в полости рта новорожденного преобладают аэробные и факультативно анаэробные виды бактерий — в первую очередь зеленящие стрептококки (в основном представителями групп: Streptococcus salivarius и S. mitis). Значительно реже определяются нейссерии, лактобациллы, коагулазонегативные стафилококки, представители семейства Enterobacteriaceae и грибы рода Candida. После прорезывания зубов в составе формирующейся зубной пленки появляются стрептококки из групп S. sanguis и S.mutans. Постепенно в микрофлоре полости рта, главным образом, за счет десневых карманов, начинают преобладать анаэробные бактерии.
В полости рта взрослых людей обнаруживают до 200 различных видов бактерий, включающих грамположительные и грамотрицательные микроорганизмы с аэробным, анаэробным и смешанным типом метаболизма, а также простейшие, микоплазмы и дрожжи. Число бактерий в слюне достигает 108КОЕ/мл и 1012 КОЕ/мл на десневом крае. Число анаэробных видов примерно в 100 раз превосходит число аэробов.
Полость рта представляет собой неоднородную среду. Различные анатомические образования формируют для обитающей здесь микрофлоры биотопы со своими местными условиями, что в свою очередь обуславливает разнообразие и неравномерность расселения симбионтов. В частности, на поверхности языка, слизистой щек и неба преобладают зеленящие стрептококки группы 5. salivarius, S. mitis, а на поверности зубов — группы S. sanguis и S. mutans. Эти виды микроорганизмов обладают адгезивной активностью в отношении колонизируемой поверхности. На десневом крае и в зубных карманах, где снижен окислительно-восстановительный (редокс) потенциал, преобладают анаэробные виды: превотеллы, трепонемы, вейлонеллы, актиномицеты, бактероиды, пропионибактерии, пептострептококки и др.
Чрезвычайно мало известно о микроорганизмах пищевода. Считается, что его микрофлора, в основном, представлена видами, попадающими сюда за счет транзита слюны и пищи из полости рта, а также слизи из носоглотки. Таким образом, нормальную флору пищевода составляют симбионты полости рта и носоглотки. Пока еще нет информации о том, приживляются ли какие-либо виды на его слизистой или только проходят транзитом.
Очень бедна микрофлора желудка. У новорожденного ребенка первых дней жизни, за счет невысокой кислотности желудочного сока, местная микрофлора более разнообразна и многочисленна, чем у взрослого человека. У взрослых лиц pH среды в желудке составляет около -2,0, что делает невозможным существование здесь большинства видов. Выживают лишь относительно кислотоустойчивые микроорганизмы: хеликобактеры, стрептококки, лактобациллы, стафилококки, грибы и некоторые анаэробные виды (пептострептококки, фузобактерии, бактероиды). Общая численность микроорганизмов в желудке не превышает 103 КОЕ/мл. Определенное влияние на состав микрофлоры желудка оказывает поступающая пища, которая отчасти, как буфер, нейтрализует соляную кислоту и создает условие для выживания большего числа видов.
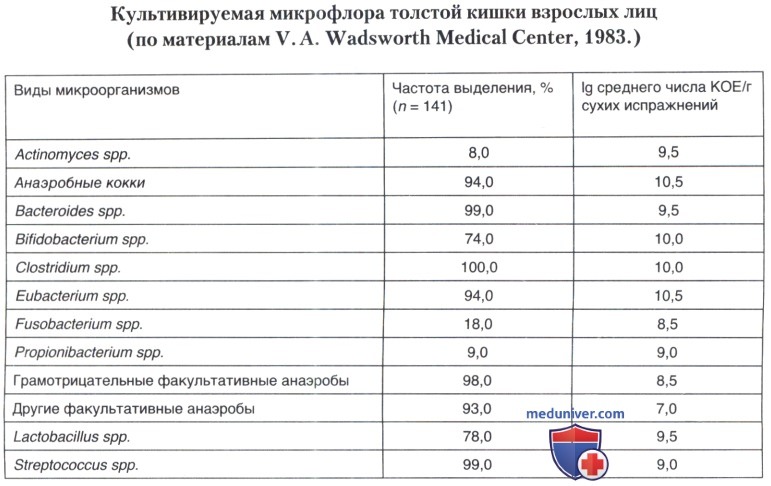
Микрофлора тонкой кишки взрослого человека на участке двенадцатиперстной, тощей и начального отдела подвздошной напоминает флору желудка. Число выделяемых здесь микроорганизмов при нормальной состоянии обычно не превышает 103 КОЕ/мл. Анаэробные виды лишь незначительно превышают число аэробных. В районе баугиниевой заслонки и толстой кишки число микроорганизмов значительно возрастает. Грамположительные и грамотрицательные анаэробные бактерии, в основном бифидобактерии, фузобактерии, бактероиды и клостридии значительно преобладают над аэробными видами. Согласно современным представлениям, вес микроорганизмов толстой кишки составляют одну треть веса сухих испражнений. В нативном состоянии микрофлора кишечника весит около 1,2 кг. Число анаэробных видов преобладает над аэробными в 1000-10 000 раз. Число видов культивируемых симбионтов по современным данным насчитывает около 450. По-видимому, существует еще очень большое число некультивируемых видов микроорганизмов, первые представления о которых были получены при исследовании срезов эпителия толстого кишечника с помощью электронной микроскопии. В таблице ниже показаны наиболее характерные культивируемые представители микрофлоры толстой кишки и их количественные параметры по данным Вадсвортского медицинского центра (Лос-Анджелес, США), которые до настоящего времени являются уникальными по широте охвата видов изолируемых микроорганизмов и глубине их идентификации. Авторами исследований была изучена микрофлора толстой кишки у 141 пациента с применением анаэробной техники. Идентификации подвергались все микроорганизмы, способные расти на искусственных питательных средах. Всего были выделены и идентифицированы около 170 видов микроорганизмов.
г) Формирование микрофлоры кишечника у детей. Наиболее обстоятельно изучен процесс микробной колонизации и сукцессии кишечника. Первичные (пионерные) сообщества микроорганизмов, сформировавшиеся в первые дни жизни ребенка, начинают быстро замещаться более адаптированными микроорганизмами, в основном, с аэробным или смешанным метаболизмом. Эти микроорганизмы, поглощая кислород из окружающей среды, снижают окислительно-восстановительный потенциал до уровня, необходимого для обитания здесь анаэробных видов. В дальнейшем анаэробные виды вытесняют представителей предшествующих сообществ до минимального числа, которое у здоровых более старших особей не превышает одного процента от всей микрофлоры. Считается, что формирование видового и количественного состава нормальной микрофлоры толстой кишки у ребенка заканчивается к двум годам и проходит в своем развитии четыре этапа. Каждый этап связан с изменением характера его питания. Первый период — период колонизации и адаптации; второй — кормление исключительно грудным молоком до первого прикорма; третий связан с началом прикорма; последний начинается с отнятия ребенка от груди. Важную роль в сукцессии микрофлоры толстой кишки ребенка играет не только изменение характера питания, но его рост и развитие (созревание физиологических функций, иммунитета, рост тканей), которые вместе с особенностями питания действуют на симбиотическую микрофлору как факторы среды ее обитания. Следует отметить, что организм человека — это не только среда обитания симбионтов, но и постоянный его экологический партнер. Это в значительной степени осложняет понимание многих процессов взаимоотношения «микрофлора — хозяин».
Существенную роль в становлении нормоценоза ребенка играет характер бактерииальной колонизации. По-разному происходит колонизация детей, рожденных естественным путем и после кесарева сечения. В первом случае они сразу после рождения начинают заселяться микрофлорой родовых путей матери, главным образом, кишечными палочками и стрептококками, во втором — представителями флоры непосредственно окружающей ребенка внешней среды, в частности, видами семейства Enterobacteriaceae, отличными от Escherichia coli. Тело ребенка после рождения может также, в зависимости от эпидемической обстановки в родильном доме, заселяться патогенными и условно-патогенными микроорганизмами из внешнего окружения и непосредственно от матери. Это формирует для него состояние риска, и может явиться начальным этапом инфекционного процесса, развитие которого будет зависеть от ряда сопутствующих условий.
Из лечебной практики хорошо известно о фактах распространения возбудителей гнойно-воспалительных заболеваний в медицинских стационарах и родильных домах. Прерывание путей передачи этих инфекций является важной задачей профилактики внутрибольничных инфекций. Было установлено, что будущие облигатные симбионты организма ребенка могут распространяться такими же путями. Следовательно, нужно корректировать профилактические мероприятия таким образом, чтобы не нарушить нормальную колонизацию ребенка. Лучшим средством для выполнения этой задачи на сегодня является организация родильных домов с совместным пребыванием матери и ребенка, когда ребенок после рождения не размещается в палате новорожденных, а остается в индивидуальной палате вместе с матерью. При такой системе содержания дети быстрее заселяются нормальной микрофлорой матери и тем самым защищаются от колонизации госпитальными штаммами. Это в дальнейшем снижает у новорожденных риск возникновения внутрибольничных инфекций.
Иначе происходит формирование микрофлоры у детей с отклонениями от нормы — недоношенных, с малым весом при рождении и родившихся с родовыми травмами. У этих групп детей отмечается отставание в формировании нормального биоценоза толстой кишки. Они чаще подвержены колонизации условно-патогенными видами и риску возникновения гнойно-воспалительных заболеваний. Более позднее формирование нормальной микрофлоры отмечается также у здоровых детей, рожденных кесаревым сечением.
Процессы микробной колонизации желудочно-кишечного тракта ребенка во многом определяются ролью нативного грудного молока. Установлено важное значение иммуноглобулинов женского молока для формирования местной иммунологической защиты пищеварительного тракта ребенка. Грудное кормление особенно важно в первые недели жизни ребенка, когда происходит его адаптация к условиям внешней среды, формирование кишечной микрофлоры, т.е. в период, когда слизистая кишечника еще не вырабатывает собственных IgA, и дети в это время не имеют факторов местной защиты против разнообразных патогенных микроорганизмов. Грудное молоко также является фактором передачи различных микроорганизмов и содержит в своем составе вещества, стимулирующие рост бифидобактерий (бифидум фактор). Оно способствует нормальной колонизации и повышает устойчивость детского организма к колонизации патогенной и условно-патогенной микрофлорой. Вероятно, это осуществляется, с одной стороны, за счет стимуляции роста бифидофлоры специфическими субстратами молока матери, с другой — за счет неспецифических факторов защиты (лактоферрин, лизоцим, макрофаги), а также специфических клеточных (В-лимфоциты) и гуморальных факторов (антитела всех классов, но в основном IgA). Наличие в грудном молоке большого разнообразия антител различной специфичности свидетельствует о его селективной роли в отборе будущей симбиотической флоры ребенка. Однако его роль в становлении нормальной микрофлоры толстой кишки у здоровых и больных детей неоднозначна. У больных детей в палате интенсивной терапии, а также у недоношенных и детей с малой массой при рождении, по сравнению со здоровыми, отмечается значительно меньший эффект влияния грудного молока на становление нормальной микрофлоры толстой кишки. Наблюдаемый факт, с позиции микробной экологии, можно объяснить тем, что кишечник больного ребенка представляет собой среду обитания для будущих симбионтов, значительно отличающуюся от таковой у здорового ребенка, и грудное молоко в этих условиях не является полностью адекватным стимулятором микробного роста. С двухлетнего возраста микрофлора кишечника здорового ребенка практически неотличима от таковой взрослого человека.
д) Микрофлора уретры. Микрофлора уретры, как правило, обитает только в дистальном ее участке. Остальная часть обычно стерильна. Среди микроорганизмов, выделяемых из уретры, преобладают представители семейства Enterobacteriaceae, в основном Е. соН. Часто встречаются также коагулазонегативные стафилококки, энтерококки, коринебактерии, лактобациллы, альфа-стрептококки, микобактерии. Реже выделяются анаэробные виды: бактероиды и пептострептококки. Помимо бактериальных видов здесь обитают микоплазмы, уреаплазмы и грибы рода Candida.
е) Микрофлора влагалища. Влагалище относится к числу полых органов, соприкасающихся с внешней средой и, естественно, богато заселенных микроорганизмами. Его анатомические особенности и сложные физиологические функции во многом определяют видовое разнообразие вегетирующих здесь микробных сообществ. Важную роль также играют анатомо-физиологические особенности, связанные с такими важными факторами, как возраст женщины (препубертатный период, репродуктивный возраст, состояние после климакса), беременность, гормональный статус, период менструального цикла, сексуальная активность, наличие воспалительных процессов, хирургические вмешательства. На состояние влагалищной микрофлоры влияют также различные экзогенные факторы: терапия антибактериальными, антимикотическими, гормональными и цитостатическими препаратами, коитус, применение контрацептивов, гигиенические мероприятия, аппликации бактерицидными препаратами, тесно прилегающее синтетическое белье, купание в сильно хлорированных бассейнах и др.
Микрофлора половых путей претерпевает значительные изменения в процессе роста и развития женского организма. Микробное заселение влагалища новорожденных девочек начинается во время их прохождения по родовым путям матери. Вследствие трансплацентарной передачи эстрогенов и частично за счет их продукции синтициальными клетками плаценты вагинальный эпителий новорожденных приобретает свойства эпителия женщин репродуктивного возраста. Это сохраняется в течение 2-3 недель после рождения. В это время вагинальная микрофлора новорожденной девочки соответствует микрофлоре ее матери. Отмечается явное преобладание лактобацилл. Через три недели эстрогены расщепляются в результате естественного метаболизма. Вследствие этого клетки вагинального эпителия подвергаются отрубевидному шелушению и остается тонкий многослойный эпителий. Уменьшается концентрация гликогена, снижается продукция кислоты микрофлорой и эпителиальными ферментами, возрастает значение pH среды с 4,5 до 7,0. Новые условия приводят к изменению видового и количественного состава местной микрофлоры. В частности, повышение pH приводит к снижению окислительно-восстановительного потенциала и формирует условия, благоприятные для жизни анаэробных бактерий.
С возрастом, по мере полового созревания, увеличивается уровень эстрогенов, выделяемых во влагалище, утолщается эпителий, накапливается гликоген, снижается pH среды до 4,0-4,5. Начинается селекция кислотоустойчивых бактерий (в основном лактобацилл), способных утилизировать гликоген. Снижение pH приводит к повышению редокс потенциала и ухудшению условий для роста анаэробных бактерий. Отмечается уменьшение видового разнообразия бактерий, но возрастает их абсолютное число.
После менопаузы наблюдается обратное развитие — уменьшается выделение эстрогенов, снижается уровень гликогена в эпителии, повышается pH среды, начинают исчезать кислотоустойчивые бактерии. Видовой состав микрофлоры становится более разнообразным и непостоянным.
У женщин репродуктивного возраста видовой и количественный состав микрофлоры влагалища подвержен постоянным колебаниям, связанным с менструальными циклами.
В межменструальный период, который делится на две фазы: пролиферативную, характеризующуюся выделением эстрогенов, утолщением эпителия и накоплением в нем гликогена, и секреторную, когда усиливается выделение прогестерона и происходит слущивание эпителия, также наблюдается изменение микрофлоры. Для пролиферативной фазы (пф) характерно более высокое абсолютное число аэробных и анаэробных видов, их большее видовое разнообразие по сравнению с секреторной фазой (сф). Наиболее выраженные различия в частоте выделения установлены для Lactobacillus spp. (пф — 61,53 % и сф — 3,7 %) и Bacteroides fragilis (пф — 42,6 % и сф — 29,6%).
Глубокие изменения в состоянии влагалищной микрофлоры наблюдаются во время беременности. Лактобациллы с аэробным и анаэробным метаболизмом — это основные представители цервикальной и вагинальной микрофлоры здоровых беременных и небеременных женщин. Большинство исследователей обнаруживают эти микроорганизмы более чем у 70% обследованных женщин, хотя в целом данные варьируют от 17 до 100%. Считается, что только эти микроорганизмы можно отнести к истинно нормальной микрофлоре влагалища, так как они даже при высоких концентрациях не вызывают заболеваний у женщин.
Количественное содержание лактобацилл зависит от физиологического статуса и состояния здоровья женщин. У здоровых их концентрация может достигать 107-109 КОЕ на 1 мл секрета.
Во время беременности, особенно к моменту родов, отмечается избыток гликогена, число симбионтов возрастает в 3-10 раз по сравнению с небеременными женщинами, количество лактобацилл резко возрастает.
Второе место после них среди факультативно анаэробных грамположительных палочек влагалища занимают коринеформные бактерии. Считается, что эти микроорганизмы могут играть протективную роль в генитальном тракте женщин, предотвращая колонизацию более патогенными видами. Их количество к моменту родов несколько увеличивается и падает через три дня после родов.
Gardnerella vaginalis (старые названия — Haemophilus vaginalis, Corynebacterium vaginale) выделяют у обследованных до 71%. Их концентрация у здоровых женщин может достигать в среднем 106 КОЕ/мл.
Факультативные грамположительные кокки представлены, в основном, стафилококками и стрептококками. Staphylococcus epidevnidis выделяется из шейки матки и влагалища до 74,1% обследованных женщин. Частота выделения 5. aureus достигает 22,2 % обследованных. Число женщин — носителей стафилококков уменьшается к началу родов и резко возрастает через три дня после родов. По данным отдельных исследователей, частота выделения коагулазоположительных и коагулазоотрицательных стафилококков в этом локусе может достигать 90 %. Альфа-гемолитические и негемолитические стрептококки обычно присутствуют во влагалище у женщин. Частота их выделения может достигать 61,3%. Наличие здесь бета-гемолитических стрептококков серогруппы А — нетипичное явление. Напротив, стрептококки серогруппы В периодически выделяются у здоровых беременных и небеременных женщин из этого биотопа. Во влагалище также часто встречаются стрептококки серогруппы D, включая энтерококки. Процент женщин — носителей стрептококков уменьшается на 34-40 неделях беременности, минимальный уровень носительства отмечали через три дня после родов.
Среди грамотрицательных видов доминирует Е. coli, частота ее выделения достигает 1/3 обследованных женщин. Кроме кишечных палочек, выделяются также другие представители этого семейства: Klebsiella и Proteus. Частота выделения последних может достигать 13%. Изредка находили также Enterobacter, Acinetobacter и Haemophilus.
Среди грибов наиболее часто выделяются С. albicans — до 33%, реже Candida glabrata — у 2,9% обследованных. Частота обнаружения С. albicans может возрастать к моменту родов.
В редких случаях обнаруживают Branchamella catarrhalis и нейссерии. Периодически выделяют Listeria monocytogenes.
С момента внедрения в микробиологические и экологические исследования анаэробной техники многие представления о доминирующей микрофлоре различных биотопов организма человека и животных были пересмотрены. Не стала исключением и микрофлора влагалища здоровых женщин. Несмотря на различия в отношении ее композиции по данным различных исследователей, большинство пришло к общему заключению о преобладании в этом локусе анаэробов над аэробами. Считается, что их соотношение составляет приблизительно 1:10 в пользу анаэробных видов.
Среди анаэробов наиболее часто обнаруживают грамположительные кокки. Вместе с микроаэрофилами они выделяются до 75% у женщин репродуктивного возраста. Это в основном Peptococcusspp. или Peptostreptococcusspp. У беременных женщин частота их выделения может достигать 40 %.
Грамположительные анаэробные палочки, помимо лактобацилл, могут быть представлены видами: Bifidobacterium, Eubacterium, Propionibacterium, Actinomyces и Clostridium.
Частота выделения бифидобактерий у небеременных женщин обычно не превышает 13 %, у беременных может достигать 40 %. Эубактерии у небеременных женщин выделяли в единичных случаях. У беременных женщин частота их обнаружения достигает 26%.
Частота выделения Actinomyces spp. по одним данным достигает 12,8% обследованных женщин, по другим — эти виды вообще не выделяются из влагалища и шейки матки. У беременных женщин одни исследователи их не обнаруживают, другие — их выделяют в 11,0%.
Клостридии во влагалище у небеременных женщин обнаруживаются в 18% случаев, у беременных — в 1,9%.
Очень широк диапазон частоты выделения анаэробных грамотрицательных палочек — от 4 до 65% обследованных женщин. Главным образом они представлены видами Bacteroides и Prevotella. У беременных женщин частота выделения бактероидов по одним данным составляет 13 % по другим — может достигать 20%.
Реже изолируются Fusobacterium. Их выделяют у небеременных женщин с частотой до 25% и в 3% у беременных.
Грамотрицательные анаэробные кокки выделяются у беременных и небеременных с частотой до 14,7%. В единичных случаях из влагалища здоровых женщин выделяют виды Mobiluncus.
В вагинальном отделяемом здоровых небеременных и беременных женщин периодически могут также обнаруживаться Mobiluncus hominis - 19,8 и 3,0% и Ureaplasma urealyticum — 25,2 и 30,0% соответственно.
Физиологические функции нормальной микрофлоры. К настоящему времени вполне установлена роль нормальной микрофлоры в физиологии организма хозяина. Трудно назвать функции макроорганизма, в которых бы не участвовали его симбионты. Уже упоминалась важная роль симбиотической микрофлоры в обеспечении местного иммунитета слизистых и кожи (колонизационной резистентность). Помимо этого, она играет важную роль в поддержании общего иммунитета хозяина путем его постоянной антигенной стимуляции. Считается, что эволюционно сложившиеся симбиотические отношения макроорганизма и его микрофлоры являются основой иммунологического гомеостаза.
Симбионты толстой кишки человека играют важную роль в пищеварении. Они участвуют в белковом обмене (способствуют гидролизу белков, расщепляют щелочную фосфатазу и холинэстеразу), сбраживают углеводы, омыляют жиры, утилизируют клетчатку, поддерживают ионный гомеостаз организма, выполняют энергетические функции, участвуют в обмене желчных кислот и синтезе витаминов, регулируют перистальтику кишечника, детоксицируют и выводят вредные вещества и т.д.. Широкое участие симбионтов толстой кишки в метаболизме хозяина позволяет рассматривать их в качестве своеобразного экстракорпорального органа. Применение биохимических методов исследований микрофлоры описано в отдельной статье на сайте.
- Читать далее "Классификация микрофлоры человека"
Редактор: Искандер Милевски. Дата публикации: 15.6.2020
- Основные определения принятые в экологии
- Симбиотическая микрофлора человека в норме
- Классификация микрофлоры человека
- Колонизационная резистентность (КР) человека
- Двойственная роль нормальной микрофлоры человека
- Нарушение состояния нормальной микрофлоры (дисбактериозы)
- Восстановление нормальной микрофлоры (лечение дисбактериозов)
- Характеристика подсистем и вариантов взаимоотношений микрофлоры с хозяином
- Основные характеристики микробного ценоза. Особенности микробных отношений
- Эпителий и микрофлора человека
