Хроническая обструктивная болезнь легких. Эпидемиология, причины
Нарушение дыхания при ХОБЛ, связанной с курением, — следствие заболевания мелких дыхательных путей (обструктивный бронхиолит) и альвеолярной деструкции (эмфизема). Это отдельные патологические процессы, каждый из которых вносит свой вклад в общую проблему нарушения дыхания у заболевших. Необратимое препятствие потоку развивается при ряде других заболеваний, включая хроническую астму, бронхоэктазию (и MB), облитерирующий бронхиолит и саркоидоз. Эти заболевания имеют разную этиологию, патологию и естественное развитие, поэтому важно рассматривать их в отдельности от ХОБЛ.
а) Эпидемиология. Курение — главный внешний фактор риска для развития ХОБЛ. Точная заболеваемость ХОБЛ неизвестна, поскольку на ранних стадиях оно протекает бессимптомно.
• В 1996 г. на долю ХОБЛ приходилось более 2 млн смертей в мире.
• В Великобритании в 2004 г. 26 000 смертей приписывали ХОБЛ.
• В Великобритании заболеваемость ХОБЛ превышает 1 млн.
• В США установлено, что у 6,6% взрослой части населения имеется выявленная на спирометрии ХОБЛ.
Заболеваемость ХОБЛ среди женщин растет за счет увеличения количества курящих женщин. С повышением распространенности курения в Китае и развивающихся странах прогнозируют, что заболеваемость ХОБЛ в мире настолько возрастет к 2020 г., что станет причиной смерти более 4,5 млн человек, сделав ее 3-й, наиболее распространенной причиной смерти в мире.
б) ХОБЛ и курение:
• Курение — единственный важный фактор риска ХОБЛ.
• Взаимосвязь между общим количеством выкуренных сигарет и ОФВг относительно слабая в популяции. Так, менее 10% колебаний в OOB1 объясняются различиями в количестве пачек, выкуренных в год (одна пачка в год эквивалентна 20 сигаретам в день на протяжении года).
• В своем продольном исследовании курильщиков среднего возраста Флетчер и Пето определили подгруппу курильщиков с быстрым снижением ОФВ1
• Такие «чувствительные курильщики» составляют приблизительно 15% курящей популяции.
• Эти данные часто неверно интерпретируют, как полагающие, что заболеваемость ХОБЛ среди курильщиков составляет 15%. Это совсем не так.
• Распространенность выявленной на спирометрии ХОБЛ у пожилой части популяции курильщиков намного превышает 15%.
• Наиболее чувствительные имеют запущенное заболевание на ранних стадиях.
Люди, курящие с детства, не достигают своего максимального ОФВ1 во взрослом состоянии и поэтому чувствительны даже к умеренному увеличению скорости снижения ОФВ1. По современным данным, высокий риск ХОБЛ в пожилом возрасте у курильщиков с детства в основном является следствием выкуривания более одной пачки день.
Знание того, что не все курильщики одинаково чувствительны к развитию ХОБЛ, и определение подгруппы чувствительных курильщиков, означают, что другие факторы, внешние или генетические, наряду с курением предрасполагают некоторых курящих к развитию ХОБЛ.
Примечание автора. Курение — это основной фактор риска ХОБЛ, но различия в чувствительности среди курильщиков означают, что важную роль играют и другие факторы.
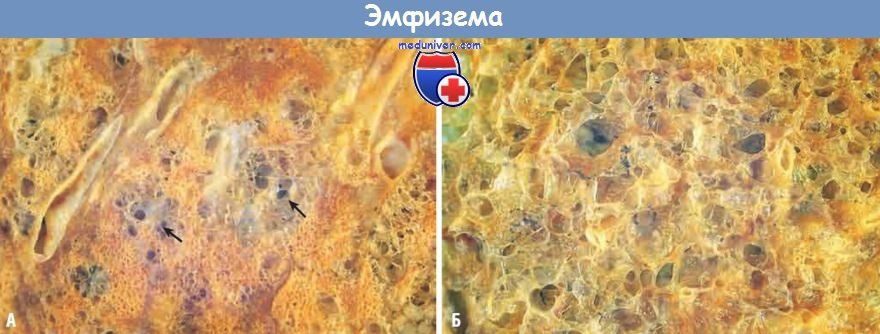
В центральных участках ацинусов видны выраженные эмфизематозные изменения (стрелки), окруженные относительно сохранными альвеолами.
(Б) Панацинарная эмфизема с расширением всей легочной дольки.
в) Внешние факторы. Ряд других внешних факторо, кроме курения, вызывает снижение ОФВ1 и нарушение дыхания. К ним относятся:
• профессиональные вредности (например, рабочие подземных тоннелей);
• бытовое топливо;
• низкая масса тела при рождении;
• пассивное курение в детском возрасте;
• вирусные инфекции дыхательных путей;
• социальный экономический класс.
Несколько исследований популяции выявили обратную связь между пищевыми антиоксидантами (найдены в фруктах и овощах), функцией легких и (или) симптомами. Предполагают, что эти антиоксиданты защищают от вредных свободных радикалов сигаретного дыма. Однако нет доказательств, что повышение потребления пищевых антиоксидантов защищает от связанной с курением ХОБЛ. По сравнению с эффектом курения эффект других установленных внешних факторов является относительно слабым, и ни один из установленных на сегодня внешних факторов должным образом не объясняет различия в чувствительности к ХОБЛ среди курильщиков.
г) Генетические факторы ХОБЛ. На сегодняшний день единственным установленным генетическим фактором риска для развития ХОБЛ является дефицит α-1-антитрипсина (α-1-АТ). Это важный ингибитор фермента нейтрофильной эластазы, поэтому гомозиготы по дефициту а-1-АТ имеют высокий риск развития эмфиземы, если они курят. Однако на долю дефицита а-1-АТ приходится только 1-2% всех случаев ХОБЛ в клинической практике. Исследования, отбирающие семьи пациентов с ранним началом ХОБЛ и без дефицита α-1-АТ (называются пробандами), показывают, что у курящих сибсов пробандов в 3-4 раза выше риск ХОБЛ, чем у курильщиков, не являющихся родственниками. Некурящие сибсы этих пробандов имеют относительно нормальную функцию легких. Это указывает на то, что внешние факторы не являются причиной наследственной кластеризации. Повышение заболеваемости ХОБЛ среди курящих сибсов не зависит от выкуренных пачек сигарет в год и поддерживает гипотезу, что существуют другие, еще не установленные гены, предрасполагающие к развитию ХОБЛ. Огромное количество исследований стремится идентифицировать гены, предрасполагающие к развитию ХОБЛ: самыми распространенными типами исследований являются исследования генов - кандидатов и анализ сцепления между генными локусами.
Примечание автора. На сегодняшний день дефицит α-1-АТ — это единственный доказанный генетический фактор риска ХОБЛ, и проводится его скрининг по уровню в крови.
д) Исследования генов-кандидатов. Исследования генов-кандидатов являются популярными, поскольку они относительно просты в выполнении. Вкратце, исследователи определяют ген, предположительно играющий важную роль в развитии ХОБЛ, и сравнивают частоту мутации в этом гене-кандидате у больных ХОБЛ с частотой у пациентов без ХОБЛ. При большей частоте мутации или полиморфизма в популяции с ХОБЛ поддерживается гипотеза, что ген предрасполагает к ХОБЛ. Эти исследования базируются на идентификации возможных генов-кандидатов. Большинство исследуемых генов кодируют протеины, являющиеся антиоксидантами, ингибиторами ПР или медиаторами воспаления, поддерживая современную гипотезу по механизму патогенеза ХОБЛ.
е) Примеры генов-кандидатов ХОБЛ.
- Антиокшданты:
• GSTP1.GSTM1.
• ЕРНХ1.
• НМОХ1.
- Протеазы/ингибиторы протеаз
• ММР1.9и12.
• SERPINA3.
- Воспаление:
• ФНО-а.
• Трансформирующий фактор роста-(3.
• Витамин-D-связывающий белок.
• ИЛ-13.
Гены глутатион-S-трансферазы (Glutathione S transferase, GST) и микросомальной эпоксидгидролазы (microsomal epoxide hydrolase, ЕРНХ) кодируют ферменты, нейтрализующие вредные субстанции в табачном дыме, тогда как гемоксигеназа-1 (haem oxygenase-1, HMOX) — это фермент, участвующий в образовании антиоксидантов. Матриксметалопротеиназы (Matrix metaloproteinases, MMP) — это цинксодержащие ферменты, разрушающие коллаген, инактивирующие а-1-АТ и активирующие ФНО-а. Ингибиторы ММР — это, возможно, будущие терапевтические средства в лечении ХОБЛ.
Существует ряд ограничений к подходу генов-кандидатов, важное из которых — возможность только исследовать ранее установленные гены, тем самым исключается вероятность идентифицировать новые гены, предрасполагающие к развитию ХОБЛ. В идеале, исследование также должно включать контрольных субъектов, идентичных больным во всех отношениях (включая анамнез курения и выборку из той же популяции), кроме того, что они не имеют ХОБЛ. Это редко достигается, и поэтому трудно определить, являются ли положительные связи результатом систематической ошибки отбора. Поэтому многие из положительных связей генов-кандидатов, описанные выше, не являются воспроизводимыми. Наконец, часто исследования включают аллели и гены, увеличивающие риск статистической ошибки I типа, если используется b-величина 0,05.
ж) Анализ сцепления между генными локусами при ХОБЛ. Анализ сцепления между генными локусами — это наиболее сложный метод идентификации участков генома, сегрегирующегося от фенотипа заболевания в популяции. Его выполняют посредством идентификации огромного количества одиночных нуклеотидных полиморфизмов (single nucleotide polymorphisms, SNPs) в геноме человека. Анализ сцепления между генными локусами имеет преимущество в том, что позволяет идентифицировать ранее нераспознанные гены, связанные с ХОБЛ. К примеру, Сильверман и коллеги идентифицировали сцепление ОФВ1/ФЖЕЛ с участком на хромосоме 2q. Эти исследования дают важные представления о генетической базе ХОБЛ.
з) Эффект определения фенотипа при ХОБЛ. Ограничение современных исследований заключается в том, что они обычно определяют фенотип ХОБЛ по наличию необратимого препятствия потоку. ХОБЛ сама по себе является гетерогенным заболеванием, при котором нарушение дыхания — это следствие эмфиземы и заболевания мелких дыхательных путей. Если каждый из этих компонентов имеет отдельную генетическую предрасположенность, то неспособность адекватно определить фенотип уменьшает возможности исследования идентифицировать важные гены. Внедрение ВРКТ дает вероятность дальнейшего уточнения фенотипа ХОБЛ с помощью квантификации эмфиземы. Уточнение фенотипа ХОБЛ позволяет идентифицировать чувствительные гены эмфиземы и заболевания мелких дыхательных путей.
и) Заключение. Курение — главный фактор риска для развития ХОБЛ. Однако увеличивается количество данных, что существует генетическая чувствительность к ХОБЛ.
к) Список использованной литературы:
1. British Thoracic Society 2003. The burden of lung disease. A statistics report from the British Thoracic Society.
2. Fletcher C., Peto R. The natural history of chronic airflow obstruction // Br Med J. — 1977. — Vol. 1 (6077). - P. 1645-1648.
3. Lomas D.A., Silverman E.K. The genetics of chronic obstructive pulmonary disease // Resf J Res. -2001. - Vol. 2 (1). - P. 20-26.
4. Lundback B„ Lindberg A., Lindstrom M. et al. Not 15 but 50% of smoker develop COPD? Report from the Obstructive Lung Disease in Northern Sweden Studies // Respir Med — 2003. — Vol. 97 (2). — P. 115-122.
5. McCloskey S.C.. Patel D„ Stephenson T.J. et al. Siblings of patients with severe COPD have a significant risk of airflow obstruction // Am J. Respir. Crit. Care Med. - 2001. - Vol. 164 (8 Pt 1). - P. 1419-1424.
6. Murray C.J., Lopez A.D. Alternative projections of mortality and disability by cause 1990-2020: Global Burden of Disease Study // Lancet. —1997. — Vol. 349 (9064). - P. 1498-1504.
7. Patel B.D., Coxson H.O., Pillai S.G. etal. Airway wall thickening and emphysema show independent familial aggregation in chronic obstructive pulmonary disease // Am J Respir Crit Care Med. — 2008. — Vol. 178. - P. 500-505.
8. Silverman E.K., Palmer L.J. Case-control association studies for the genetics of complex respiratory diseases // Am J Respir Cell Mol Biol. — 2000. — Vol. 22(6). - P. 645-648.
9. Silvermann E.K.. Palmer L.J. Genomewide linkage analysis of quantitative spirometric phenotypes in severe early-onset chronic obstructive pulmonary disease // Am. J. Hum. Genet. — 2002. — Vol. 70 (5). - P. 1229-1239.
- Читать "Патофизиология ХОБЛ. Механизмы повреждения легких"
- Возврат в раздел "медицинская физиология"
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Метотрексат, препараты золота при бронхиальной астме. Применение
- Астма беременных. Диагностика, лечение
- Обострение астмы. Частота, причины
- Клиника обострений астмы. Диагностика
- Лечение обострений астмы. Препараты
- Дифференциация обострений астмы. Критерии жизнеопасной астмы
- Хроническая астма. Клиника, течение
- Оценка эффективности лечения астмы. Выявление вероятности обострения
- Алгоритмы последовательности лечения астмы. Этапы
- Хроническая обструктивная болезнь легких. Эпидемиология, причины
