Гормоны и их влияние на мозг, поведение
Многие принципы взаимодействия лекарственных препаратов с организмом можно применить к определенным гормонам, которые воздействуют на рецепторы нейронов. Гормоны синтезируются специальными железами в головном мозге и теле. Взаимодействие гормонов мозга и остального организма обеспечивает возникновение регулирующей их активность петли обратной связи.
В течение жизни уровень гормонов меняется, влияя на развитие и функционирование всего организма (Nugent et al., 2012). Эндокринные системы во многом напоминают активирующие нейромедиаторные системы, за исключением гормонов, которые распространяются через кровь. Кроме того, многие вырабатываемые эндокринными железами гормоны способны действовать как нейромедиаторы, и наоборот, многие нейромедиаторы действуют как гормоны.
а) Иерархия гормонов. Многие гормоны образуют петли обратной связи, которые задействуют головной мозг и остальной организм. Как показано на рис. 1, гипоталамус вырабатывает нейрогормоны, которые стимулируют гипофиз, заставляя его выбрасывать в кровь рилизинг-гормоны. Гормоны гипофиза, в свою очередь, воздействуют на остальные железы внутренней секреции, заставляя их выбрасывать в кровь соответствующие гормоны, которые взаимодействуют с различными мишенями и передают в мозг сигнал о необходимости усиления или снижения выработки гормона.
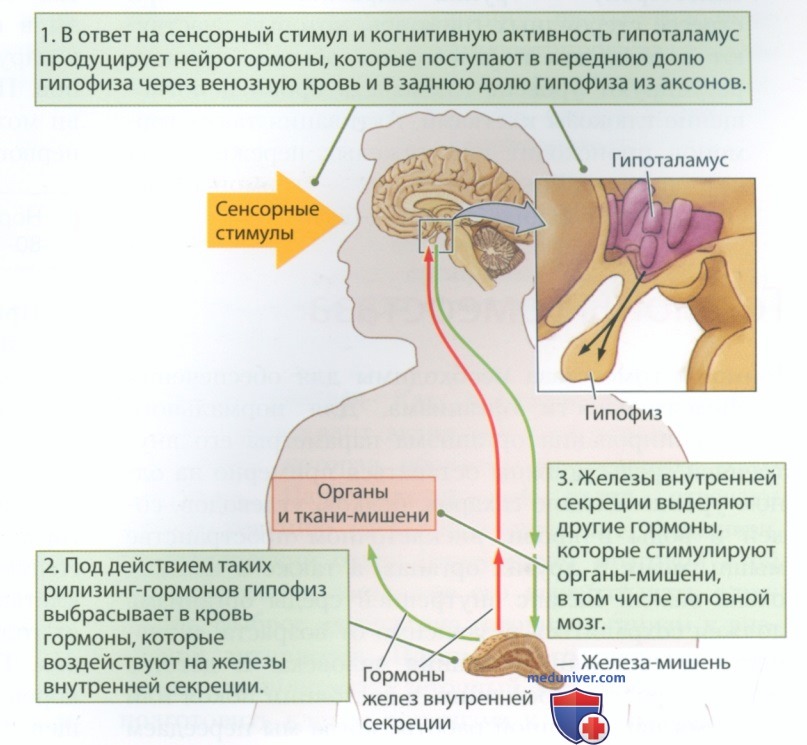
Гормоны не только воздействуют на внутренние органы, но также влияют практически на все функции мозга. Почти все нейроны мозга содержат рецепторы для взаимодействия с различными гормонами. Гормоны не только влияют на развитие половых органов и внешность человека, но также воздействуют на нейромедиаторы — особенно в нейронах, задействованных в половом развитии и поведении (Barth et al., 2015). Гормоны могут влиять на экспрессию генов, связываясь со специфическими рецепторами на поверхности и внутри клетки, а затем, проникая в ядро, повлиять на транскрипцию гена.
Транскрипция, в свою очередь, влияет на синтез белков, задействованных в различных клеточных процессах. Таким образом, гормоны определяют структуру организма и мозга, а также влияют на поведение.
Хотя неясно, каким образом гормоны продуцируют поведение или вносят свой вклад в сложные формы поведения, разнообразие их функций позволяет понять, почему организм использует гормоны в качестве мессенджеров: мишени гормонов разбросаны по всему организму, поэтому наилучший из возможных способов достигнуть мишеней — распространяться с кровью, которая попадает во все отделы организма.
б) Классы гормонов и их функции. Гормоны могут быть использованы в качестве препаратов для профилактики и лечения заболеваний. Люди принимают синтетические гормоны в качестве заместительной терапии в случае отсутствия или дисфункции продуцирующих соответствующие гормоны желез. Кроме того, люди принимают гормоны, прежде всего половые, чтобы замедлить старение, стать сильнее и выносливее или получить преимущество в спорте. Около 100 вырабатываемых человеческим организмом гормонов по их химической структуре делят на стероиды и пептиды.
Стероидные гормоны, такие как тестостерон и кортизол, синтезируются из холестерина и являются жирорастворимыми. Стероиды диффундируют от места их синтеза в железах внутренней секреции, в том числе в гонадах, коре надпочечников и щитовидной железе. Они связываются с рецепторами стероидных гормонов на клеточной мембране или внутри клетки и взаимодействуют с ДНК клетки, влияя на транскрипцию генов.
Пептидные гормоны, такие как инсулин, гормон роста и эндорфины, синтезируются в клетке точно так же, как другие белки. Они влияют на активность клетки-мишени, связываясь с метаботропными рецепторами на клеточной мембране и обеспечивая выработку вторичного мессенджера, который оказывает воздействие на физиологические процессы в клетке или транскрипцию гена.
Стероидные и пептидные гормоны делят на три основные функциональные группы в зависимости от регулируемого ими поведения; каждый гормон может входить более чем в одну группу:
1. Гормоны гомеостаза поддерживают динамическое равновесие внутренней среды организма и обеспечивают регуляцию физиологических систем. Минералокортикоиды (например, альдостерон) регулируют водно-солевой баланс крови и клеток, влияя на уровень натрия, калия и кальция, а также участвуют в поддержании пищеварения.
2. Гонадостероиды (половые гормоны) регулируют репродуктивные функции. Они определяют развитие организма по мужскому (тестостерон) или женскому (эстроген) типу, влияют на половое поведение и процесс зачатия, у женщин регулируют менструальный цикл (эстроген и прогестерон), деторождение и лактацию (пролактин, окситоцин). Эти гормоны, в особенности окситоцин, отвечают за формирование привязанности матери к ребенку. Некоторым животным, например овцам, они необходимы для формирования привязанности.
3. Глюкокортикоиды (например кортизол и кортикостерон) — группа вырабатываемых при стрессе стероидных гормонов, которые участвуют в белковом и углеводном обмене, а также регулируют уровень глюкозы в крови и поглощение глюкозы клетками. Активация таких гормонов происходит при тяжелых переживаниях и в чрезвычайных ситуациях — гормоны обеспечивают реакцию «бей-или-беги».
в) Гормоны гомеостаза. Гормоны гомеостаза необходимы для обеспечения жизнедеятельности организма. Для нормального функционирования организма параметры его внутренней среды должны оставаться примерно на одном уровне. Баланс сахаров, белков, углеводов, солей и воды в крови, внеклеточном пространстве мышц, мозге и других органах, а также в клетках очень важен. Баланс внутренней среды организма должен сохраняться независимо от возраста, активности и состояния сознания человека. В детстве или во взрослом состоянии, в состоянии покоя или во время напряженной работы, когда мы переедаем или когда голодны, выжить нам позволяет постоянство внутренней среды.
Примером гомеостатической функции является регуляция уровня глюкозы в крови. В процессе пищеварения после приема пищи происходит повышение уровня глюкозы в крови. Определенная группа клеток поджелудочной железы выделяет инсулин — гормон гомеостаза, который дает вырабатываемому в печени и мышцах ферменту гликогенсинтазе команду начать запасать глюкозу в виде гликогена. Связанное с этим снижение уровня глюкозы способствует снижению стимуляции клеток поджелудочной железы, поэтому они перестают вырабатывать инсулин, а организм прекращает запасать гликоген. Когда организм нуждается в глюкозе как в источнике энергии, подключается другой гормон, глюкагон, действие которого противоположно действию инсулина.
Глюкагон стимулирует другой фермент, гликогенфосфорилазу, который инициирует расщепление гликогена до глюкозы.
Причиной сахарного диабета является неспособность клеток поджелудочной железы вырабатывать инсулин или недостаточная выработка инсулина. Из-за этого уровень глюкозы в крови снижается (гипогликемия) или повышается (гипергликемия). При гипергликемии уровень глюкозы в крови повышается, потому что инсулин не дает клеткам организма сигнал начать поглощение глюкозы. Как следствие, даже при высоком уровне глюкозы в крови глюкозное голодание может привести к нарушению функции клеток, в том числе нейронов. Постоянный высокий уровень глюкозы в крови может стать причиной повреждений глаз, почек, нервов, сердца и кровеносных сосудов.
При гипогликемии неправильное питание может привести к критическому снижению уровня глюкозы в крови и потере сознания. Эрик Стин и его коллеги (Eric Steen, 2005) считают, что инсулинорезистентность клеток головного мозга может быть связана с болезнью Альцгеймера. Состояние голода и потребление пищи регулирует целый ряд гормонов гомеостаза, в том числе лептин и грелин. Лептин (от греч. leptos — тонкий), вырабатываемый клетками жировой ткани (адипоцитами), подавляет голод, поэтому его называют гормоном насыщения.
Грелин (в основе названия индоевропейский корень gher — растущий), вырабатываемый в пищеварительном тракте, регулирует гормоны роста и участвует в регуляции энергетического гомеостаза. Грелин также вызывает голод. Он начинает вырабатываться, когда желудок пуст; после наполнения желудка выработка грелина прекращается. Лептин и грелин взаимодействуют с рецепторами одних и тех же нейронов дугообразного ядра гипоталамуса, участвуя в поддержании энергетического гомеостаза за счет регуляции потребления пищи.
в) Анаболико-андрогенные стероиды. Класс синтетических гомонов, родственных тестостерону — половому гормону, который вырабатывается в семенниках и отвечает за формирование мужских половых признаков. Анаболико-андрогенные стероиды способствуют наращиванию мышечной массы (анаболический эффект) и маскулинизации (андрогенный эффект). Анаболико-андрогенные стероиды, более известные как анаболические стероиды, были впервые получены для наращивания массы тела и повышения выносливости. В 1952 г. ими впервые воспользовались русские тяжелоатлеты, чтобы улучшить спортивные результаты и победить в международных соревнованиях.
Синтетические стероиды быстро приобрели популярность в других странах и среди других спортсменов, что в конце концов привело к запрету их применения в легкой атлетике и других видах спорта, а также к внедрению допинг-контроля. Внедрение допинг-контроля превратилось в игру «Кошки-мышки» — появляются новые анаболические стероиды, способы их применения, а следовательно, и способы их маскировки.
В наше время спортсмены и обычные люди одинаково часто употребляют анаболические стероиды. Свыше одного миллиона человек в США воспользовались анаболическими стероидами не только для повышения спортивной результативности, но также для улучшения телосложения и внешнего вида. Среди старшеклассников анаболические стероиды принимают не менее 7% юношей и 3% девушек.
Применение анаболических стероидов несет определенные риски для здоровья. Прием таких препаратов приводит к снижению выработки тестостерона, что негативно влияет на мужскую фертильность и сперматогенез. Одновременно с наращиванием мышечной массы повышается агрессивность. Анаболические стероиды увеличивают риск сердечного приступа и инсульта. Могут пострадать функции печени и почек, также возможно повышение риска развития рака. Прием анаболических стероидов также может приводить к облысению по мужскому типу. У женщин увеличивается в размерах клитор, появляются прыщи и повышенная волосатость, а голос становится более низким.
Анаболические стероиды одобрены для клинического применения. Тестостерон-заместительную терапию назначают мужчинам с гипогонадизмом. Ее также назначают для коррекции снижения мышечной массы после травм и восстановления мышечной массы при истощении. У женщин анаболические стероиды применяют для лечения эндометриоза и фиброзно-кистозной мастопатии.
г) Глюкокортикоиды и стресс. Стресс — это термин, который был позаимствован из инженерной отрасли. Он обозначает давление на объект, создаваемое специфическим фактором. Применительно к человеку и другим животным стрессор — это стимул, который влияет на гомеостаз и обеспечивает мобилизацию организма. Реакция на стресс, как поведенческая, так и физиологическая, предполагает мобилизацию и попытку уменьшить стресс.
Реакция на стресс может сохраняться после завершения вызвавшего стресс события и возникать в отсутствие очевидного стрессора. Хронический стресс изнуряет организм.
1. Стрессовая активация. Интересно, что организм одинаково реагирует на возбуждающие, вызывающие грусть и пугающие стрессоры. Роберт Сапольски (Robert Sapolsky, 2004) рисует яркую картину охоты голодного льва на зебру, чтобы проиллюстрировать реакцию на стресс. Ситуация охоты заставляет двух животных вести себя по-разному, однако у них наблюдается одна и та же физиологическая реакция. Реакция на стресс возникает под воздействием стрессора на организм в тот момент, когда мозг воспринимает стрессор и отвечает на его воздействие мобилизацией организма, задействовав гипоталамус. Реакция на стресс может быть быстрой и медленной.
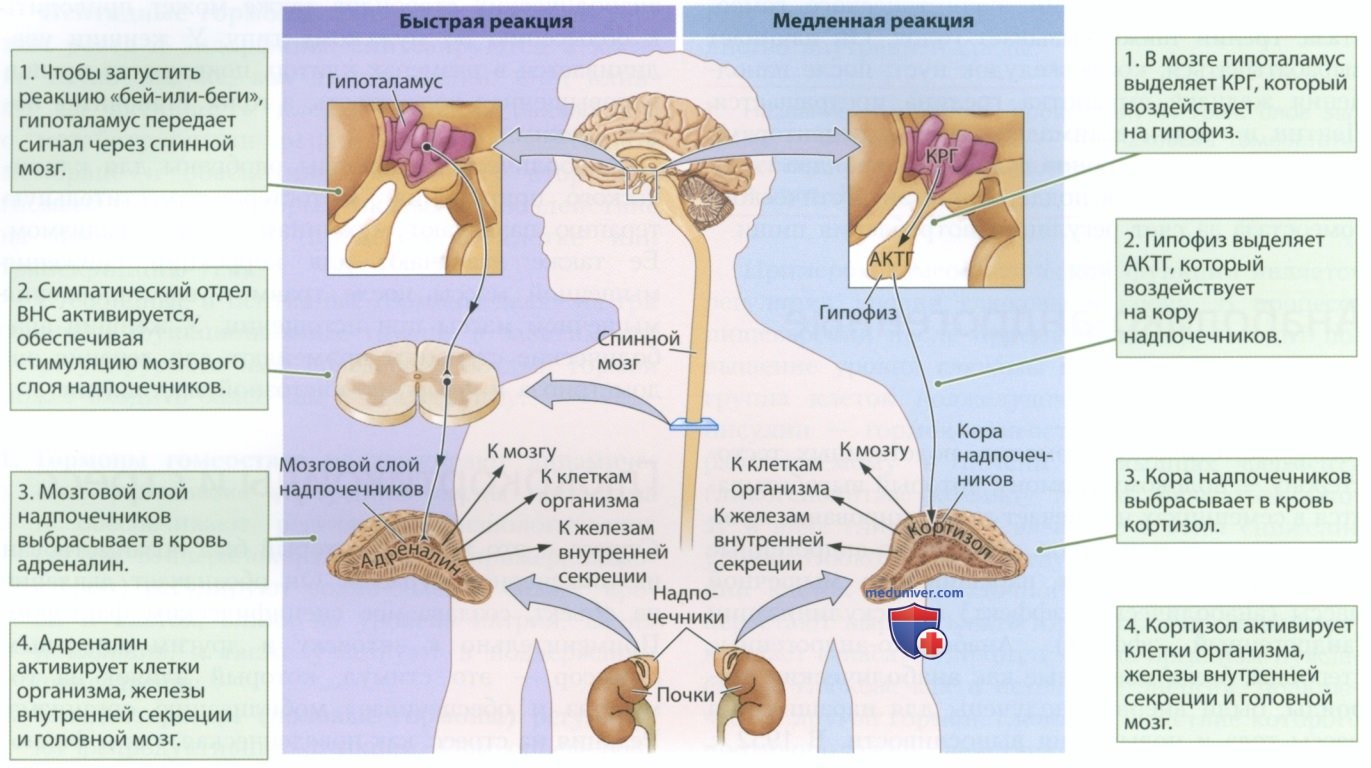
БЫСТРАЯ РЕАКЦИЯ. Как показано на рис. 2 (слева), происходит активация симпатического отдела ВНС, которая обеспечивает реакцию «бей-или-беги». Парасимпатический отдел, отвечающий за реакцию «отдохни-и-перевари», неактивен. Симпатический отдел стимулирует мозговой слой надпочечников, заставляя его вырабатывать адреналин. Выброс адреналина готовит организм к внезапной активности. Помимо всего прочего, адреналин стимулирует клеточный метаболизм, чтобы подготовить клетки организма к мобилизации.
P.S. Принцип 4. Процессы в ЦНС носят многоуровневый характер.
МЕДЛЕННАЯ РЕАКЦИЯ. Как показано на рис. 2 (справа), медленную реакцию регулирует стероидный гормон кортизол — глюкокортикоид, вырабатываемый корой надпочечников. Запуск кортизоловой реакции может занимать от нескольких минут до нескольких часов. Кортизол выполняет множество функций, в том числе отключает все системы организма, не задействованные в борьбе со стрессом. Например, кортизол отключает выработку инсулина, поэтому печень начинает высвобождать глюкозу, на время увеличивая доступный запас энергии. Он также отключает репродуктивные функции и подавляет выработку гормона роста. Так кортизол направляет все силы организма на борьбу со стрессом.
2. Завершение реакции на стресс. В норме реакция на стресс должна быть кратковременной. Организм мобилизуется, справляется с проблемой, задействовав физиологические и поведенческие механизмы, и завершает цикл реакции на стресс. Головной мозг отвечает как за запуск реакции на стресс, так и за ее завершение. Давайте представим себе, что будет, если реакция на стресс не завершится:
• организм продолжит расходовать энергию вместо того, чтобы запасать ее;
• расходование белков приведет к истощению мышц и возникновению общей слабости; подавление гормона роста приведет к тому, что организм не сможет расти;
• подавление процессов пищеварения приведет к снижению потребления и переработки пищи, необходимой для восполнения питательных веществ;
• подавление репродуктивных функций продолжится;
• подавление иммунной системы приведет к повышению риска инфицирования и заболевания.
Сапольски (2005) утверждает, что важную роль в завершении реакции на стресс играет гиппокамп. Он содержит множество рецепторов кортизола, а аксоны его нейронов проецируются на гипоталамус. Это значит, что гиппокамп имеет все необходимое для определения уровня кортизола в крови и передачи в гипоталамус сигнала о снижении уровня кортизола в крови.
Тем не менее связь между гиппокампом и уровнем кортизола в крови может быть не такой очевидной. Сапольски наблюдал рожденных в дикой природе верветок (карликовых зеленых мартышек), которые совершали набеги на сельскохозяйственные угодья в Кении, попадали в ловушки и оказывались в клетке. Он обнаружил, что некоторые мартышки болели и умирали от болезни, которая, как оказалось, была связана со стрессом. По-видимому, умирали занимавшие подчиненное положение особи, оказавшиеся в одних клетках с агрессивными доминантными животными. Вскрытие показало высокую частоту язвы желудка, увеличения надпочечников и выраженных дегенеративных изменений гиппокампа.
Повреждения гиппокампа могли быть следствием продолжительного воздействия высокого уровня кортизола, вырабатываемого из-за стресса, вызванного нахождением в одной клетке с агрессивной мартышкой.
Регуляцию уровня кортизола обычно осуществляет гиппокамп, однако если уровень кортизола остается повышенным из-за сохранения стрессовой ситуации, кортизол в конце концов повреждает гиппокамп, заставляя его уменьшиться в размерах. Поврежденный гиппокамп теряет способность снижать уровень кортизола. Таким образом, возникает порочный круг, который обеспечивает прогрессирующую дегенерацию гиппокампа и отсутствие регуляции уровня кортизола (рис. 3). Следует отметить, что исследования на крысах показали увеличение размеров миндалевидного тела под воздействием аналогичного стресса (Bourgin et al., 2015).
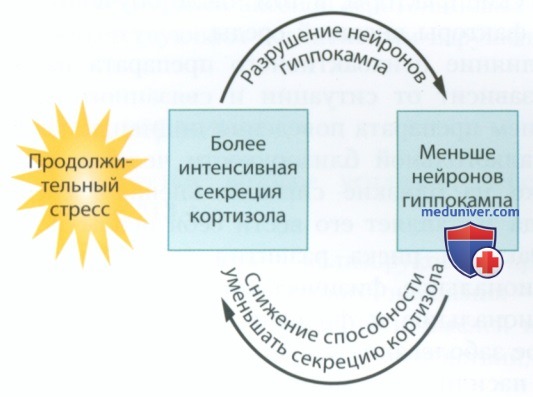
Поскольку крысы и обезьяны реагируют на стресс так же, как человек, чрезмерный стресс может привести к аналогичным изменениям в мозге человека. По мнению ученых, гиппокамп играет определенную роль в памяти, поэтому вызванные стрессом повреждения гиппокампа могут приводить к расстройствам памяти. Считается, что миндалевидное тело играет определенную роль в формировании эмоций, поэтому связанные со стрессом изменения могут приводить к усилению эмоциональных реакций. Такие поведенческие изменения напоминают посттравматическое стрессовое расстройство (ПТСР). Людям с ПТСР кажется, что они заново переживают травму, а переживаемое ими физиологическое возбуждение укрепляет их веру в неизбежность опасности.
Ученым пока не удалось установить, может ли кумулятивный эффект стресса приводить к повреждению гиппокампа у человека. Например, исследования женщин с ПТСР, перенесших сексуальное насилие в детстве, с использованием методов нейровизуализации выявили некоторые нарушения памяти и изменения размеров гиппокампа. Другие исследования не выявили различий между испытуемыми, пережившими насилие, и испытуемыми, не подвергавшимися насилию (Landre et al., 2010). Разные результаты, полученные в ходе похожих исследований, можно объяснить следующим образом.
Во-первых, неясно, какие именно повреждения гиппокампа приводят к стрессовому расстройству. Во-вторых, чувствительность методов нейровизуализации может быть недостаточной для выявления изменений функции клеток гиппокампа или потери умеренного количества клеток. В-третьих, реакция человека на стресс обусловлена особенностями его личности и меняющимися факторами внешней среды. В-четвертых, на нейрогенез в гиппокампе может влиять неонатальный стресс (Lajud & Тогпег, 2015). Долгосрочные последствия — это уменьшение размеров гиппокампа и повышенная восприимчивость к стрессу.
Следует отметить, что человек живет долго и в течение жизни накапливает опыт, что затрудняет анализ эффектов отдельных стрессовых ситуаций. Тем не менее Патрик Макгоуэн с коллегами (Patrick McGowan, 2009) обнаружили, что плотность рецепторов глюкокортикоидов в мозге покончивших с собой лиц, переживших сексуальное насилие в детстве, была ниже, чем в контрольной группе и в группе лиц, покончивших с собой, но не подвергавшихся сексуальному насилию в детстве.
Такое снижение уровня рецепторов и мРНК глюкокортикоидов может говорить о том, что жестокое обращение в детстве может приводить к эпигенетическим изменениям экспрессии генов глюкокортикоидов. Сниженный уровень рецепторов глюкокортикоидов, по-видимому, уменьшает способность гиппокампа подавлять реакцию на стресс. Исследование Макгоуэна очень важно, поскольку оно позволяет предположить возможность влияния стресса на функцию гиппокампа без уменьшения размеров гиппокампа. Указанное исследование также говорит о том, что стресс может вызывать множество изменений в различных отделах мозга. Эти изменения еще предстоит описать и исследовать (Clauss et al., 2015).
д) Закрепление изученного материала. Прежде чем продолжить, проверьте себя.
1. Гипоталамус вырабатывает _____ , который стимулирует _____ , заставляя выделять в кровь _____ . Уровень циркулирующих в крови гормонов обеспечивает передачу сигнала в(обратную связь).
2. В соответствии с химической структурой гормоны делят на _____ и _____ .
3. Можно сказать, что _____ гормоны обеспечивают постоянство внутренней среды организма, _____ гормоны регулируют размножение, а _____ регулируют стресс.
4. Один из классов синтетических гормонов — это _____ ; они способствуют наращиванию _____ и обладают _____ эффектом.
5. Реакция на стресс может быть быстрой, опосредованной выделением _____ , и медленной, опосредованной выделением _____ .
6. Расскажите, что объединяет стресс, кортизол и гиппокамп.
е) Ответы на вопросы для самоконтроля:
1. Нейрогормон; гипофиз; рилизинг-гормоны; головной мозг.
2. В любом порядке: стероидные гормоны; пептидные гормоны.
3. Гомеостатические; половые; глюкокортикостероиды.
4. Анаболические стероиды; мышечной массы; маскулинизирующим.
5. Адреналина; кортизола.
6. Гиппокамп играет важную роль в подавлении реакции на стресс — он регулирует уровень выработки кортизола, который участвует в медленной реакции на стресс. Кортизол отключает все системы организма, не задействованные в борьбе со стрессом и направляет все силы организма на борьбу с ним. При длительном стрессе сохраняющийся постоянно высокий уровень кортизола в конце концов может повредить гиппокамп.
- Читать далее "Резюме по влиянию психоактивных препаратов и гормонов на мозг, поведение"
Редактор: Искандер Милевски. Дата публикации: 28.7.2023
- Возможно ли улучшить умственную деятельность лекарствами и препаратами?
- Как препараты попадают в нервную систему? Гематоэнцефалический барьер (ГЭБ)
- Действие препаратов на синапсы: агонисты и антагонисты
- Холинергический синапс: примеры действия препаратов
- Толерантность (синдром привыкания) на примере алкоголя
- Сенситизация к психоактивным препаратам
- Классификация психоактивных препаратов по нейромедиаторным системам
- Причины индивидуальной реакции на психоактивный препарат
- Причины зависимости от психоактивных веществ и ее лечение
- Гормоны и их влияние на мозг, поведение
- Резюме по влиянию психоактивных препаратов и гормонов на мозг, поведение
