Методы лечения аневризмы брюшной аорты и их эффективность
а) Хирургическое лечение аневризмы брюшной аорты (Ао). Целью лечения аневризм брюшного отдела аорты (Ао) является продление жизни пациента путем предупреждения разрыва аневризмы. Для решения вопроса о проведении оперативного лечения нужно соотнести естественное течение аневризмы и ожидаемую продолжительность жизни с возможными заболеваемостью и смертностью при хирургическом вмешательстве.
При плановом хирургическом лечении аневризм операционная смертность в целом составляет 4-6% и 2% — у пациентов с низким риском. Однако операционная смертность возрастает до 19% при неотложном вмешательстве по восстановлению Ао и достигает 50% при восстановительном оперативном лечении разорвавшихся аневризм.
Размеры бессимптомных аневризм остаются основным показанием для восстановительного оперативного лечения, и в течение многих лет ведется дискуссия, при каком минимальном диаметре аневризмы следует проводить хирургическое вмешательство. Этот вопрос был изучен в двух крупномасштабных клинических исследованиях.
В исследовании United Kingdom Small Aneurysm Trial рандомизировали 1090 пациентов в возрасте 60-76 лет с малыми (диаметром от 4,0 до 5,5 см) аневризмами брюшного отдела Ао на группы раннего планового хирургического вмешательства или наблюдения с помощью УЗИ. При долгосрочном наблюдении исследование не выявило различий в выживаемости между группами, хотя после 8 лет ОС была немного ниже в группе раннего хирургического лечения. Но поскольку операционная смертность в этом исследовании составила 5,8%, некоторые врачи задаются вопросом, можно ли улучшить выживаемость после раннего хирургического вмешательства, если добиться снижения операционной смертности.
В исследовании ADAM (Aneurysm Detection and Management) Veterans Affairs Cooperative Study 1136 пациентов с небольшими (диаметром от 4,0 до 5,4 см) бессимптомными аневризмами были рандомизированы в группу неотложной восстановительной операции и группу наблюдения с помощью УЗИ или КТ через интервалы в 6 мес. Несмотря на низкую операционную смертность (2,1%), через 5 лет между этими двумя группами существенного различия не было.
Таким образом, пациентам с бессимптомными аневризмами размерами < 5,5 см хирургическое вмешательство в большинстве случаев не показано.
Однако следует отметить, что пациентов, участвовавших в этих исследованиях, тщательно наблюдали как консервативно, так и с помощью визуализирующих методов. Такое тщательное наблюдение пациентов в практике обычно не проводят. Другое важное ограничение — обе группы состояли почти полностью из мужчин (United Kingdom Small Aneurysm Trial — 78%, ADAM — 99%), а поскольку риск разрыва аневризмы у женщин больше и происходит в меньших по диаметру аневризмах, чем у мужчин, результаты исследований нельзя экстраполировать на женщин. Учитывая тенденцию к частому разрыву аневризм меньших размеров у женщин, Joint Council of the American Association for Vascular Surgery и Society for Vascular Surgery официально рекомендовали проводить у женщин плановую операцию при диаметре аневризмы от 4,5 до 5 см.
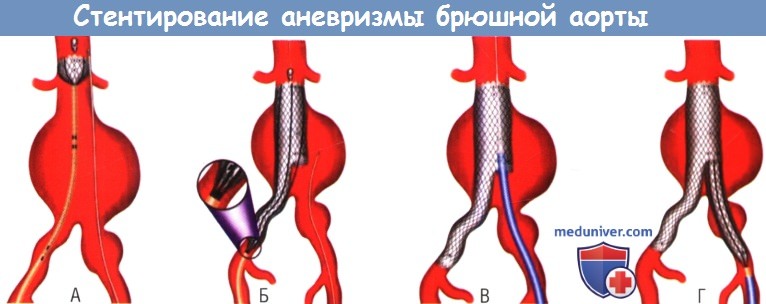
(А) Размещение катетера и проксимальная иммобилизация нерез правый бедренный доступ.
(Б) Устанавливают и расширяют основную и правую части стента.
(В) Канюлю для расширения левой части стента вводят через левый бедренный доступ.
(Г) Левую часть стента расширяют, завершая эндоваскулярное устранение аневризмы аорты с вовлечением левой подвздошной артерии.
Хирургическое восстановление брюшного отдела аорты (Ао) заключается во вскрытии аневризмы и установке искусственного протеза из дакрона или политетрафлуороэтилена (Gore-Tex), увеличивающегося в объеме. Иногда достаточно простого трубчатого трансплантата, хотя часто, чтобы иссечь аневризму полностью, операцию выполняют дистально в одной или обеих подвздошных артериях.
В случае больших аневризм большую часть аневризматической стенки оставляют на месте (внутримешотчатый подход Creech), уменьшая, таким образом, необходимость широкого рассечения Ао и сокращая время ее пережатия.
Менее инвазивной альтернативой открытому хирургическому вмешательству в связи с абдоминальными аневризмами Ао является чрескожная имплантация расширяемого эндоваскулярного стента. Устройство состоит из искусственного трубчатого трансплантата, который вводят, например, через бедренную артерию, и продвигают транслюминально через аневризму под рентгенологическим контролем; затем дистальный и проксимальный концы расширяемого стента закрепляют с помощью системы фиксации.
Для устранения аневризмы аорты (Ао) стент перекрывает регион аневризмы, выключая этот участок из кровообращения, но позволяя поддерживать аортальный кровоток дистально через просвет стента. В некоторых случаях используют бифуркационный стент с двумя рукавами на дистальном конце, предназначенными для расширения просвета внутри аневризматически измененных общих подвздошных ар терий. Показатель успешной имплантации стентов в прошлом десятилетии колебался от 78 до 99%, а в нескольких последних сообщениях составил 98%. Несмотря на эти многообещающие результаты, только 30-60% пациентов с абдоминальными аневризмами Ао анатомически подходят для эндоваскулярного восстановления. Одной из главных технических проблем, связанной с техникой имплантации стентов и еще не решенной, является частое внутреннее просачивание, которое ангиографически проявляется в виде постоянного потока контрастного вещества внутри аневризматического мешка, поскольку невозможно полностью исключить аневризму из аортальной циркуляции. Такое просачивание, если его оставить без лечения, может подвергать пациента постоянному риску увеличения или разрыва аневризмы, поэтому часто прибегают к повторному вмешательству.
Долгосрочный прогноз восстановления аорты (Ао) с помощью эндоваскулярного стентирования по сравнению с открытым хирургическим вмешательством остается неясным. Недавно в нескольких рандомизированных контролируемых исследованиях попробовали определить краткосрочный и среднесрочный прогнозы. Исследовательская группа Dutch Randomized Endovascular Aneurysm Management сравнила хирургическое восстановление с эндоваскулярным у 345 пациентов с абдоминальной аневризмой диаметром > 5 см, которые были подходящими кандидатами для каждого из этих методов. 30-суточная операционная смертность была достоверно ниже в группе эндоваскулярного стентирования по сравнению с группой хирургического вмешательства (1,2% vs 4,6%) [23]. В исследовании EVAR (Endovascular Aneurysm Repair) были аналогичным образом рандомизированы 1082 пациента и установлено достоверное и идентичное уменьшение операционной смертности: 1,7% в группе эндоваскулярного стентирования и 4,7% в группе хирургического вмешательства. Оба эти исследования вселяют оптимизм, т.к. четко демонстрируют снижение ранней смертности при эндоваскулярном стентировании.
Несмотря на хорошие показатели успешности восстановления с помощью эндоваскулярного стентирования в длительных исследованиях, есть сообщения о неблагоприятных исходах при этом вмешательстве, составляющих 3% случаев в год (1% — при разрыве и 2% — при переходе к хирургическому восстановлению), по сравнению с показателем 0,3% при хирургическом восстановлении. Неудивительно, что среднесрочные результаты были менее обнадеживающими. Действительно, согласно данным группы Dutch Randomized Endovascular Aneurysm Management, двухлетняя кумулятивная выживаемость при эндоваскулярном и хирургическом восстановлении фактически не отличалась (89,7 и 89,6% соответственно). В исследовании EVAR за 4 года наблюдения при постоянном уменьшении количества летальных исходов, связанных с аневризмами, в группе эндоваскулярного стентирования по сравнению с группой хирургического вмешательства (4% vs 7%; р = 0,04) достоверного различия в ОС между этими группами не было. Данные исследования показывают, что эндоваскулярное восстановление Ао не имеет явного преимущества перед хирургическим для тех пациентов, кто является хорошим кандидатом для обоих вмешательств.
В связи с этим в настоящее время применение эндоваскулярного стентирования при аневризмах брюшного отдела Ао в целом ограничивается пожилыми пациентами или лицами с высоким операционным риском.
б) Оценка риска операции на аневризме брюшной аорты (Ао). Поскольку пациенты с аневризмами брюшного отдела Ао почти во всех случаях имеют атеросклероз, вероятность наличия у них сопутствующих заболеваний коронарных, почечных и церебральных артерий существенно повышает риск хирургических вмешательств на сосудах. Действительно, 50% всех периоперационных летальных исходов при устранении аневризм происходят в результате ИМ. Кроме этого, в одном исследовании пациентов, подвергавшихся устранению аневризмы, при обычной коронарной артериографии была выявлена тяжелая КБС у 18% пациентов, включая 8% лиц без предшествующих симптомов коронарной ишемии. Среди пациентов с ангиографически достоверной КБС 50% имели множественные сосудистые поражения.
В нескольких исследованиях показано, что сцинти-графия миокарда является эффективным методом выявления пациентов с самым высоким риском периоперационных ишемических событий. Пациенты с обратимыми дефектами перфузии во многих сегментах миокарда имеют наиболее высокий риск, в этой подгруппе КАГ будет, вероятно, наиболее полезной. Для таких пациентов была хорошо доказана ценность изотопных визуализирующих методов с фармакологическим стрессом. Хотя нагрузочная сцинтиграфия также является ценным скрининговым методом, многие пациенты с ИБС не в состоянии достигнуть адекватной ЧСС из-за ограниченной способности к ФН. Другими ценными методами дооперационной оценки миокардиальной ишемии являются стресс-ЭхоКГ с добутамином и нагрузочная ЭКГ у пациентов с исходно нормальной ЭКГ и адекватной толерантностью к физической нагрузке.
Широко поддерживается выборочная дооперационная оценка с целью выявления и определения тяжести заболевания КА у пациентов с клиническими признаками. Некоторые исследователи предлагают проводить скрининг пациентам с убедительными кардиальными ФР, несмотря на отсутствие клинических признаков заболевания КА. Польза проведения дооперационной коронарной реваскуляризации (КШ или ангиопластики) пациентам с достоверно диагностированной КБС остается недоказанной. Результаты нерандомизированных исследований пациентов с достоверным поражением КА, подвергнутых хирургическому лечению, показывают более низкую смертность по сравнению с больными без выполнения КШ. Более того, в рандомизированном исследовании показано, что долгосрочный прогноз у пациентов с комбинированным поражением периферических артерий и высоким риском КБС улучшается при реваскуляризации КА у больных с трехсосудистым поражением. Как и в случае КШ, данных, подтверждающих, что дооперационное ЧКВ при значимом коронарном стенозе уменьшает риск хирургического вмешательства на больших сосудах, пока еще нет.
В дополнение к дооперациопному скринингу и коронарной реваскуляризации периоперационное инвазивное мониторирование гемодинамики и тщательное наблюдение может в дальнейшем уменьшить операционный риск, вторичный по отношению к коронарной ишемии. Более того, удастся предупредить ишемию миокарда и, возможно, ИМ назначением в периоперационном периоде р-АБ.
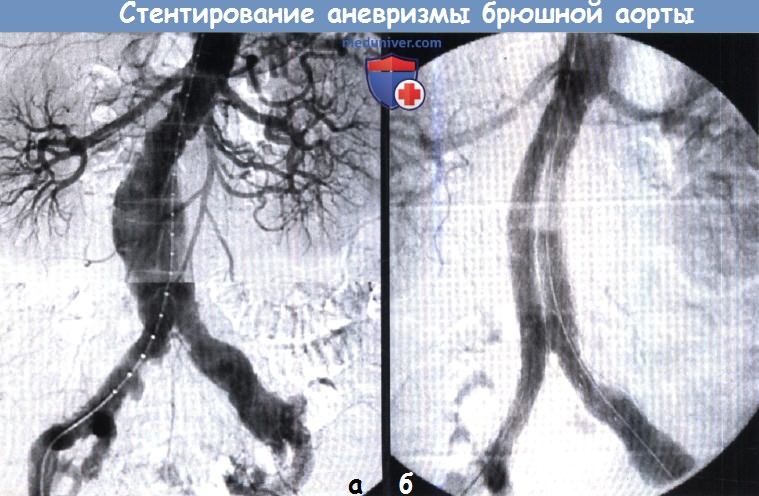
с двусторонним вовлечением подвздошных артерий до (А) и после (Б) расширения аортального стента.
в) Поздняя выживаемость. Анализ поздней выживаемости после операций по устранению аневризм брюшного отдела Ао среди 2500 пациентов выявил 1-, 5- и 10-летний коэффициенты выживаемости 93, 63 и 40% соответственно.
г) Консервативное лечение аневризмы брюшной аорты (Ао). Основным методом консервативного лечения аневризм брюшного отдела Ао является коррекция ФР. Большинство пациентов с аневризмами брюшного отдела Ао курят, поэтому, учитывая повышенный риск разрыва аневризмы среди активно курящих, пациенту следует прежде всего избавиться от этой пагубной привычки. Кроме этого, необходимо адекватно контролировать АГ. Для снижения риска расширения и разрыва аневризмы назначают на длительный период Р-АБ, т.к. их эффективность подтверждена и в экспериментах на животных, и в исследованиях с участием людей.
В экспериментальных моделях на мышах, склонных к развитию спонтанных аневризм Ао, пропранолол замедлял их развитие. Эффективность лекарственной терапии в этом эксперименте, возможно, не зависела от снижения АД или уменьшения скорости выброса АЖ (dP/dt), но могла быть обусловлена изменениями метаболизма соединительной ткани и структуры стенки Ао. Результаты исследований с участием людей противоречивы. В нескольких из них показано, что лечение пропранололом существенно не влияло на скорость роста аневризм малого размера (< 4 см), но уменьшало скорость роста больших аневризм (4-5 см и более) на > 50%. В связи с этим при консервативной терапии пациентам с большими аневризмами рекомендуются β-АБ.
При наличии ГХС необходимо ее лечение. Как уже упоминалось, экспериментальные данные свидетельствуют, что ингибиторы ГМГ-КоА-редуктазы (статины) могут оказывать защитное действие даже у пациентов с нормальным уровнем холестерина. В одном нерандомизированном исследовании 130 пациентов с абдоминальными аневризмами Ао сравнивали скорость роста аневризм при терапии статинами и у пациентов, не получавших статины. Через 2 года средний размер аневризмы достоверно увеличился с 4,5 до 5,3 см у пациентов, не получавших статины, в то время как на фоне терапии статинами средний размер аневризмы остался прежним (р < 0,001). Нужно, конечно, провести рандомизированные контролируемые исследования, чтобы подтвердить эти данные, но это сообщение свидетельствует о том, что статины можно применять для профилактики и лечения абдоминальных аневризм.
В дальнейшем при наличии аневризмы брюшного отдела аорты (Ао) размерами > 4 см нужен тщательный рутинный контроль для выявления либо быстрого ее расширения (> 0,5 см/год), либо увеличения размеров до > 5,5 см. Любое из этих изменений является показанием для хирургического лечения. В целях контроля рекомендуется проведение КТ каждые 6 мес, а у лиц с высоким риском — каждые 3 мес. Для мониторинга роста аневризм КТ предпочтительнее УЗИ, т.к. определение размера аневризмы с помощью КТ более точное.
- Читать "Причины и механизмы развития аневризмы грудной аорты"
Оглавление темы "Аневризма аорты.":- Аорта в норме и ее функции
- Возрастные изменения аорты от старости
- Методы обследования аорты при болезни
- Причины и механизмы развития аневризмы брюшной аорты
- Симптомы и клиника аневризмы брюшной аорты
- Методы обследования при аневризме брюшной аорты
- Каков риск разрыва аневризмы брюшной аорты? Прогноз
- Методы лечения аневризмы брюшной аорты и их эффективность
- Причины и механизмы развития аневризмы грудной аорты
- Симптомы и клиника аневризмы грудной аорты
