Меры профилактики остановки сердца при заболеваниях сердца
Внезапная сердечная смерть (ВСС) часто является первым клиническим признаком основных структурных поражений сердца и возникает у больных из группы низкого риска, поэтому уже давно исследователей интересовала разработка терапевтических стратегий, направленных на первичную профилактику внезапной сердечной смерти (ВСС).
После разочаровавших результатов исследования CAST и тревожных предположений об отсутствии эффективности и ПЭ ААП класса I, обычно назначаемых в целях первичной или вторичной профилактики внезапной сердечной смерти (ВСС), стали изучать эффективность применения амиодарона и ИКД-терапии.
Были проведены два исследования применения амиодарона у пациентов после ИС (в одном из них ФВ < 40%), которые не выявили пользу препарата в снижении смертности, однако в обоих исследованиях был продемонстрирован антиаритмический эффект в виде снижения летальных исходов, вызванных аритмией или ФЖ после реанимации. Анализ результатов показал, что одновременное применение β-АБ с ИКД снижает показатели смертности.
Одновременно с изучением амиодарона было выполнено первое рандомизированное контролируемое исследование MADIT, в котором сравнивали антиаритмиче-скую терапию (в основном амиодарона) с ИКД-терапией. Рандомизированные пациенты имели ФВ < 35%, неустойчивую ЖТ при амбулаторной регистрации и индуцируемую ЖТ, не купируемую прокаина-мидом. В этой группе очень высокого риска произошло снижение ОС на 54% после терапии с помощью ИКД по сравнению с медикаментозным лечением, в первую очередь амиодароном.
В то же время исследование, сравнивающее имплантацию имплантируемого кардиовертера-дефибриллятора (ИКД) без антиаритмической терапии у пациентов с ФВ < 36%, перенесших коронарное шунтирование (CABG-PATCH), не выявило какой-либо пользы от ИКД-терапии в снижении показателей ОС. Единственным маркером аритмических рисков, необходимым для включения в исследование, была положительная сигнал-усредненная ЭКГ. Исследование MUSTT было комплексным исследованием, целью которого было определить, может ли электрофизиологически зависимая терапия улучшить исходы у больных с неустойчивой или индуцируемой ЖТ и ИМ в анамнезе.
Результаты показали, что статистически значимое положительное влияние на показатели общей смертности (ОС) было достигнуто при выборе тактики лечения в зависимости от результатов ЭФИ. Из-за отсутствия реакции на лекарственную терапию наибольший успех был достигнут у пациентов с ИКД по сравнению с пациентами с индуцируемой тахикардией без лечения. Была отмечена 24% смертность среди пациентов с ИКД в течение последующих 5 лет по сравнению с 55% среди тех, кто получал электрофизиологически зависимую лекарственную терапию, и 48% среди тех, кто не получал лечения.
MADIT II было следующим из опубликованных исследований первичной профилактики после ИМ. В этом исследовании при ИКД-терапии был достигнут успех в снижении показателей смертности по сравнению с пациентами с ФВ < 30%, перенесших ИМ и получавших обычное лечение.
В исследование DEFINITE, целью которого было определение пользы профилактической ИКД-терапии у пациентов с неишемической КМП, статистическая значимость не была достигнута (р = 0,08). Однако представленные результаты продемонстрировали снижение относительного риска на 35% и абсолютного риска на 6% в течение 2 лет наблюдения.
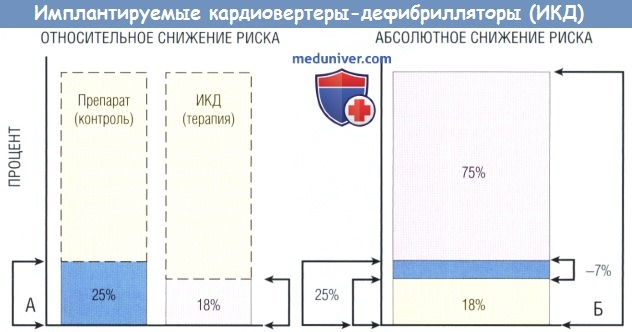
(А) В подгруппе ИКД-терапии смертность за 2 года составила 18% vs 25% в подгруппе, получавшей ААП, 27% относительного снижения фатальных событий в популяции.
(Б) Когда относительное снижение экстраполируют на общую численность населения, абсолютное снижение фатальных событий в общей популяции составляет 7%.
Исследование SCD-HeFT было выполнено с целью определения потенциальной пользы ИКД по сравнению с амиодароном и плацебо у пациентов с ХСН II/III ФК NYHA и ФВ < 35%. Результаты этого исследования показали уменьшение относительного риска на 23% и абсолютного риска на 7% в течение 5 лет. Амиодарон не имел дополнительных преимуществ по сравнению с обычной терапией.
Исследования первичной профилактики были разработаны для определения популяции пациентов с осложненными заболеваниями сердца с очень высоким риском ВСС и ОС вследствие тяжести основного заболевания. Большинство клинических работ, отвечая на вопрос об относительной эффективности лечения ААП по сравнению с ИКД-терапией, включали величину ФВ в качестве маркера поздних стадий болезни (критериями включения был диапазон 30-40% или менее).
В исследовании AVID по вторичной профилактике анализ результатов показал, что преимущества ИКД-терапии перед амиодароном у больных с ФВ 36-40% отсутствуют, и все преимущества относятся к ФВ < 35%. Это факт очень важен, т.к. он ставит вопрос о терапевтических возможностях стратегий как первичной, так и вторичной профилактики при ФВ > 35%. Такой ретроспективный анализ нуждается в подтверждениях, которые можно получить после проведения контролируемых исследований.
В то время как риск внезапной сердечной смертности (ВСС) и общей смертности (ОС) является самым высоким среди пациентов с поздними стадиями структурных поражений сердца и низкой ФВ из-за функциональных нарушений. Значительная часть общей тяжести ВСС приходится на пациентов с ИБС или различными неишемическими КМП с ФВ > 35-40%. Среди пациентов с СИ, связанной с различными формами КМП, общий риск смерти значительно ниже у пациентов с I ФК или начальным периодом II ФК, чем с окончанием III/IV ФК, а вероятность ВС выше в первых группах.
Несмотря на это, данные для выбора тактики первичной профилактики остановки сердца у таких пациентов отсутствуют. Ограничение обусловлено тем, что пациенты этих категорий, как правило, имеют низкий риск развития событий, но на них в совокупности приходится большое число внезапных сердечных смертей (ВСС).
В других группах, связанных с увеличением риска внезапной смерти (ВС) при отсутствии резкого уменьшения ФВ, например в некоторых случаях вирусного миокардита, ГКМП, ДПЖ и саркоидоза, выбор тактики ведения больного происходит без клинических испытаний и принятия терапевтических решений. Пациентам с симптоматическими желудочковыми аритмиями, связанными со структурными поражениями, такими как ДПЖ, при которой риск смерти в основном связан с аритмией, часто рекомендуется ИКД-терапия даже при отсутствии остановки сердца или гемодинамически значимой ЖТ.
Является ли антиаритмическая терапия столь же эффективной, остается неизвестным, но решение об использовании дефибрилляторов у больных с нарушениями ритма часто поддерживается формулировкой рисков на основе клинических маркеров. Среди наблюдений, в которых семейный анамнез играет роль в определении риска, клинические решения принимаются легче при наличии выраженной семейной истории ВСС. Этот подход поддерживается генетическими исследованиями ГКМП, в которых была установлена связь некоторых генетических мутаций с определенным риском ВСС, и клиническими результатами использования ИКД в группе больных ГКМП высокого риска.
Все больше внимания уделяется клинически трудноуловимым или бессимптомным структурным поражениям или исключительно электрофизиологическим проявлениям, такими как врожденные СУ QT, синдром Brugada и идиопатическая ФЖ. Процесс принятия решений но стратегии вторичной профилактики у пациентов с СУ QT относительно прост.
Лиц, выживших после остановки сердца или потенциально фатальных аритмий, особенно при наличии семейного анамнеза внезапной сердечной смерти (ВСС), как правило, лечат с помощью ИКД. β-АБ, по-прежнему, необходимы для не имевших событий членов семьи больного и, возможно, для некоторых пациентов с синкопе неясного происхождения.
Напротив, пациенты с выраженным СУ QT без семейного анамнеза ВСС, при отсутствии симптоматических аритмий или и того и другого вместе, как правило, в настоящее время лечат назначением β-АБ. Между этими пациентами находятся бессимптомные члены семьи пациентов с симптомами СУ QT. Учитывая сложность патофизиологии фатальных аритмий у таких больных, порог назначения ИКД-терапии увеличивается.
Генетический скрининг может быть полезен для определения конкретных 1079 рисков, особенно если отдельный риск аритмии доказан выявлением одного или нескольких модифицированных генов, взаимодействующих с дефектом, ответственным за поражение ионных каналов. В этом контексте семейный анамнез преждевременных ВСС у родственников пострадавших полезен в процессе принятия решений по профилактической терапии в этой категории больных.
Среди молекулярных синдромов аритмии синдром Brugada является тем заболеванием, о стратегиях лечения которого идут дискуссии до сих пор. ИКД рассматривают как предпочтительный вариант стратегии вторичной профилактики у выживших после остановки сердца и симптоматических пациентов, даже если она основана исключительно на результатах наблюдений. Однако основной подход в профилактике родственников пострадавших, особенно бессимптомных, пока не ясен.
Исследования выявили, что синкопе с электрографическими изменениями, указывающими на патологию в основных отведениях, служат маркером риска и достаточным основанием для ИКД-терапии, а основные электрографические изменения, связанные с индуцируемостыо желудочковых тахиаритмий во время ЭФИ, также являются маркером риска. И наоборот, отсутствие блокады правой ножки пучка Гиса и изменения сегмента ST-T без провокаций предполагают более низкий риск. Однако семейный анамнез ВСС остается важным фактором, влияющим на принятие обоснованного решения. Аналогичные рассуждения касаются членов семьи больных с ДПЖ.

- Читать "Меры профилактики остановки сердца среди населения"
Оглавление темы "Остановка сердца. Обмороки":- Стратегии антиаритмической терапии с целью профилактики остановки сердца
- Меры профилактики остановки сердца после реанимации
- Меры профилактики остановки сердца при заболеваниях сердца
- Меры профилактики остановки сердца среди населения
- Классификация причин обморка - синкопе
- Причины и механизмы потери сознания при ортостатической гипотензии
- Причины и механизмы рефлекторного обморока - синкопе
- Беседа и осмотр пациента с потерей сознания. Анамнез при обмороках
- Анализы и обследования у пациента с потерей сознания - обмороками (синкопе)
- Советы по оценке пациентов с обмороками (синкопе)
