Стеноз почечных артерий (СПА) - клиника, диагностика и лечение
Атеросклероз почечной артерии приводит к стенозу почечной артерии (СПА) и неизменно ассоциируется с возрастающим риском СССоб и смерти. Изучение общей популяции путем дуплексного ультразвукового сканирования сосудов почек у лиц > 65 лет выявило распространенность СПА, равную 6,8%. Распространенность СПА увеличивается с 20 до 30% в группах высокого риска (например, у пациентов с установленным атеросклерозом сосудов).
Стеноз почечных артерий (СПА) атеросклеротического генеза является прогрессирующим заболеванием и связано с последующей атрофией почек, несмотря на контроль АГ. Переход СПА в окклюзию наблюдается в более тяжелых случаях заболеваний (> 60%) с частотой от 10 до 20% в год.
Стеноз почечных артерий (СПА) атеросклеротического генеза — важная причина ПН, злокачественной АГ и синдромов сердечной дестабилизации — нестабильной стенокардии и скоротечного отека легких. Односторонний СПА проявляется клинически в виде АГ, опосредованной вазоконстрикцией, в то время как двусторонний СПА обусловливает АГ в результате перегрузки объемом.
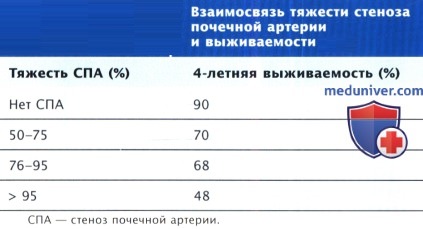
В США до 20% пациентов > 50 лет, находящихся на программном почечном диализе, имеют СПА атеросклеротического характера (ишемическую нефропатию), ставший причиной ПН. 2-, 5- и 10-летняя выживаемость пациентов со СПА, находящихся на диализе, составляет 56, 18 и 5% соответственно. Риск смерти зависит от тяжести СПА.
Медиана выживаемости у пациентов с атеросклеротическим СПА, находящихся на диализе, составила 25 мес по сравнению с 133 мес у пациентов с поликистозом почек. Очевидно, что ранняя диагностика СПА и профилактика терминальной стадии ПН крайне важны.
а) Диагностика стеноза почечных артерий (СПА). Такие клинические критерии диагностики СПА, как диастолическая АГ у пациентов > 55 лет, стойкая или злокачественная АГ, стойкая АГ у пациентов с ранее хорошо контролируемой АГ и/или увеличение уровня Кр в сыворотке крови, должны насторожить врача и ускорить дальнейшую диагностику. В качестве неинвазивных скрининг-тестов у пациентов с подозрением на СПА лучше всего использовать такие методы визуализации, как дуплексное ультразвуковое сканирование почечной артерии, КТА и МРА.
Метод инвазивной почечной ангиографии рекомендуется, если клинически вероятность СПА высока, а неинвазивные методы неубедительны или не соответствуют клиническим признакам. Некоторые эксперты также рекомендуют проведение почечной ангиографии во время катетеризации сердца и периферических сосудов у пациентов, которые находятся в группе повышенного риска СПА. Не рекомендуются проведение сцинтиграфии почек с каптоприлом, определение активности ренина в плазме (со стимуляцией каптоприлом или без нее) и селективное исследование ренина в почечных венах.
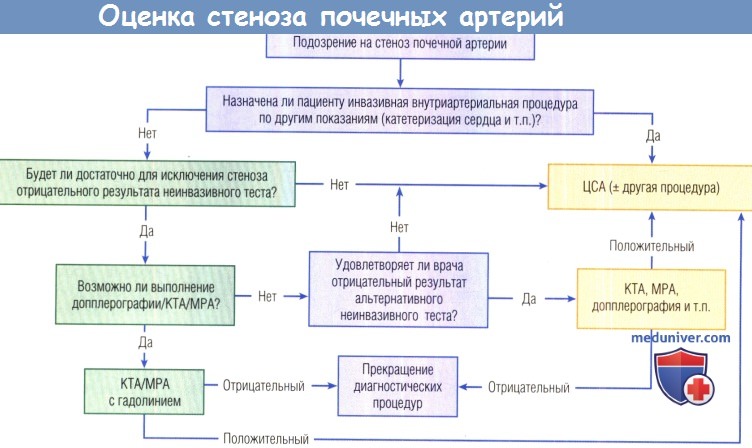
При наличии подозрения на стеноз, если пациенту назначена инвазивная внутриартериальная процедура, неинвазивную визуализацию откладывают и во время другой процедуры проводят низкообъемную цифровую субтракционную аортографию (ЦСА).
В других случаях врач должен оценить, можно ли по отрицательному результату неинвазивного теста исключить стеноз почечных артерий.
Если это так, следует выполнить неинвазивный тест. Если нет, то нужно рассмотреть возможность ЦСА и селективной ангиографии.
КТА — компьютерно-томографическая ангиография. МРА - магнитно-резонансная ангиография.
б) Лечение стеноза почечных артерий (СПА). После установления диагноза «анатомический стеноз почечной артерии» следует рассмотреть наиболее приемлемое лечение. Цели терапии включают контроль АД, сохранение или улучшение функции почек и по возможности снижение риска ССО и смерти. Решение о реваскуляризации принимают при наличии клинических показаний, обусловленных СПА с гемодина-мически значимым стенозом, что определяется по следующим признакам:
(1) сужение диаметра стенозированного сосуда на 50% с градиентом САД (измеряют катетером 5F или под давлением) от 20 мм рт. с г. или средним градиентом давления 10 мм рт. ст.;
(2) сужение диаметра стенозированного сосуда на 70%, измеряемое количественными ангиографическими методами;
(3) сужение диаметра стенозированного сосуда на 70%, определяемое методом ультразвуковой локации почечного кровотока.
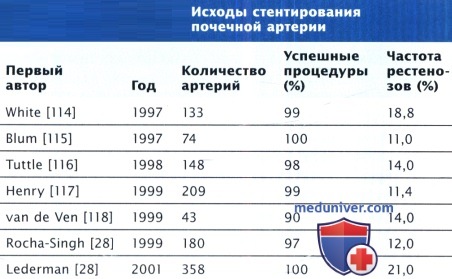
Хотя ЧТА остается единственным методом выбора при лечении фиброзно-мышечной дисплазии, первичная установка стента при атеросклеротическом СПА является стандартом лечения. Совершенно очевидно, что при почечной реваскуляризации стентирование обеспечивает более предсказуемые и гемодинамически благоприятные результаты. Согласно опубликованным данным, частота рестеноза при почечном стентировании может быть даже ниже.
Предиктором поздней проходимости почечного стента является резкое улучшение или увеличение его просвета. Почечные артерии большего диаметра (6 мм) реже подвергаются рестенозу, чем сосуды меньшего диаметра (< 4,5 мм). Длительное (5 лет) наблюдение двух случаев показало, что первичный уровень проходимости составил 79 и 84,5%, а вторичный — 92,4 и 98%. Почти все рестенозы происходят в течение первого года после имплантации стента, рестеноз после 2 лет встречается редко.
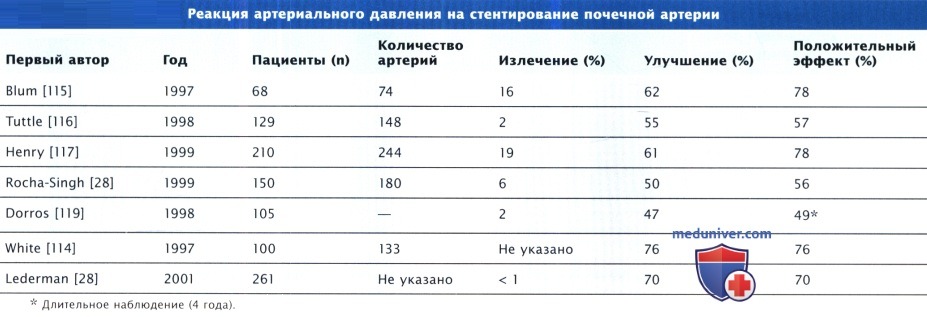
Однако, несмотря на технический успех стентирования более чем в 95% случаев, стеноз, выявляемый ангиографически, не прогнозирует клинический эффект. Это означает, что стеноз почечной артерии не имеет причинной связи с АГ либо успешно проведенная реваскуляризация не облегчает почечную перфузию.
Основная сложность в прогнозировании результатов лечения у больных с реноваскулярной патологией заключается в том, что они обычно имеют другие нефротоксические заболевания, которые могут влиять на исходы реваскуляризации, — СД, гипертоническую болезнь, сосудистые эмболии и лекарственные поражения.

в) Отбор пациентов. По аналогии с коронарным фракционным резервом кровотока почечный фракционный резерв кровотока служит показателем функциональной способности почек при стенозе почечной артерии. Согласно клиническим данным, при СПА выявлена слабая корреляция между количественными ангиографическими и гемодинамическими градиентами (пиковым, средним и гиперемическим), тогда как значительная корреляция выявлена между почечным фракционным резервом кровотока и базовым градиентом давления. Почечный фракционный резерв кровотока определяли у 17 пациентов с плохо контролируемой АГ и клиническим улучшением.
Аномальный почечный фракционный резерв кровотока (< 0,8) являлся предиктором лучшего контроля АД (86%) по сравнению с 30% случаев, где почечный фракционный резерв кровотока был в норме (р = 0,04).
МНУП обеспечивает спектр диуретических, натрийуретических эффектов и артериальную вазодилагацию, выступает антагонистом РАС и AT II и может служить биомаркером ответа организма на почечную реваскуляризацию. У 27 пациентов с неконтролируемой АГ и СПА (стеноз 70%) течение АГ улучшилось в 77% случаев из тех наблюдений, в которых выявили повышенный уровень МНУП, но сравнению с 5 пациентами, у которых базовый уровень МНУП < 80 пг/мл (р = 0,001).
Если после успешного стентирования уровень МНУП снижался на > 30%, отмечалось улучшение контроля АД в 94% случаев (у 16 больных из 17).
На основании индекса резистентности почечных артерий, измеренного неинвазивно с помощью ультразвуковой допплерографии, можно стратифицировать пациентов, которым, вероятно, сможет помочь вмешательство на почечных артериях. Однако существуют противоречивые данные о возможности индекса резистентности прогнозировать результаты лечения пациентов со СПА. Ретроспективное исследование, в котором большинству пациентов была проведена БАП, а не стентирование, показало, что повышенный индекс резистентности свидетельствует о низкой вероятности улучшения контроля АД или почечной функции после реваскуляризации.
Однако в проспективном исследовании, в котором 241 пациенту выполнили почечное стентирование, пациенты с аномальным индексом резистентности имели лучшую реакцию в плане АД и улучшение функции почек через 1 год после вмешательства. Веские доказательства и научная ценность последнего исследования позволяют сделать вывод, что повышенный индекс резистентности не должен быть препятствием для выполнения вмешательства на почечной артерии.
Несколько клинических исследований продемонстрировали, что успешное стентирование почечной артерии улучшает или стабилизирует функцию почек у пациентов с наличием атеросклеротической реноваскулярной недостаточности. Состояние пациентов с ПН и гемодинамически значимым СПА после установки стента также улучшилось. Успешное стентирование почечной артерии может значительно замедлить прогрессирование ПН. Расчет средних значений сывороточного Кр до и после установки стента показал четырехкратное замедление прогрессирования ПН после установки стента в почечной артерии.
Одним из основных предикторов улучшения почечной функции после чрескожной реваскуляризации является быс трое снижение функции почек до вмешательства. Этот факт свидетельствует о более остром процессе, при котором возможна его обратимость. Но = 20% пациентов после вмешательства на почках будут иметь снижение или ухудшение функции почек. Одним из способствующих этому факторов может быть атероэмболия в результате повреждения крупных АБ в Ао. Работа по адаптации к эмболическим осложнениям при вмешательстве на почках продолжается.
г) Односторонний стеноз почечных артерий и нефропатия. Традиционно считается, что односторонний СПА не вызывает ишемической нефропатии, если контралатеральная почечная артерия проходима. Тем не менее реваскуляризация односторонних СПА может улучшить или стабилизировать функцию почек. Два клинических исследования продемонстрировали улучшение функции почек у пациентов с односторонним стенозом почечной артерии.
Реваскуляризация одностороннего стеноза почечной артерии приводит к ощутимому улучшению функции пораженной стенозом почки. Восстановление кровотока в пораженной стенозом почке обусловливает гиперфильтрацию здоровой почки, что приводит к снижению протеинурии. Эти данные позволяют предположить, что у пациентов с нарушением функции почек коррекция односторонних СПА может улучшить и/или стабилизировать функцию почек.
Таким образом, чрескожное вмешательство при реноваскулярной патологии почек является безопасным и эффективным методом лечения и предпочтительнее открытой хирургической реваскуляризации. Стентирование почечной артерии может положительным образом повлиять на контроль АГ, улучшить и/или стабилизировать функцию почек, а также отсрочить необходимость гемодиализа у некоторых пациентов. Кроме того, разработка способов предупреждения атероэмболических осложнений еще больше повысит сохранность почечной паренхимы. Рекомендуемый в настоящее время системный подход к обследованию и лечению этого состояния проиллюстрирован на рисунках ниже.
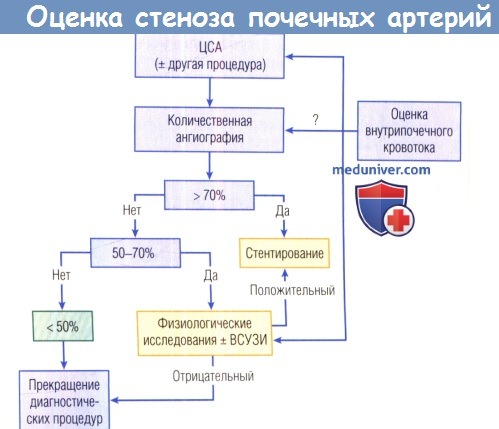
После выполнения цифровой субтракционной аортографии (ЦСА), которая подтвердила наличие поражения почечной артерии, следует провести количественную ангиографию с объективной оценкой тяжести стеноза.
Очень тяжелые поражения (> 70%) следует подвергать реваскуляризации, а умеренные поражения (< 50%) нет.
Промежуточные поражения следует оценивать физиологическими методами и/или проводить дополнительную анатомическую оценку тяжести стеноза, используя,
например, внутрисосудистое ультразвуковое исследование (ВСУЗИ) либо оценку фракционного резерва кровотока.
Отсутствие ускорения кровотока через стеноз или градиента давления служит основанием для выбора более мягких методов лечения.

(Б) Состояние после стентирования. Обратите внимание на небольшое остаточное сужение (стрелка).
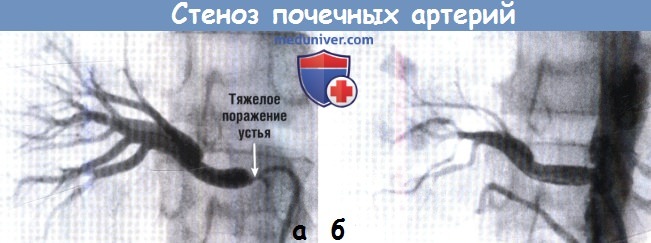
(Б) Состояние после стентирования. Обратите внимание на отсутствие заполнения дистального русла из-за атероэмболии.
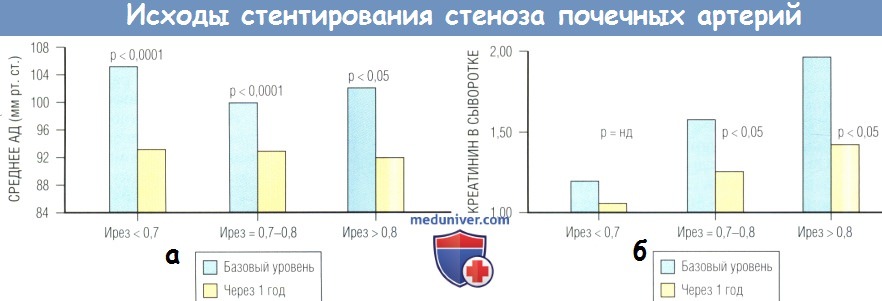
б - Изменения функции почек у пациентов с нормальным индексом резистентности (Ирез) < 0,7, умеренным повышением Ирез от 0,7 до 0,8 и тяжелым нефросклерозом (Ирез > 0,8) через 1 год после стентирования, нд — недостоверно.
- Читать "Хроническая брыжеечная ишемия (ХБИ) - клиника, диагностика и лечение"
Оглавление темы "Эндоваскулярное лечение стеноза сосудов.":- Эндоваскулярные методы лечения, стентирование бедренно-подколенной окклюзии
- Эндоваскулярные методы лечения, стентирование берцовой окклюзии
- Стеноз почечных артерий (СПА) - клиника, диагностика и лечение
- Хроническая брыжеечная ишемия (ХБИ) - клиника, диагностика и лечение
- Эндоваскулярные методы лечения, стентирование брахиоцефального ствола и подключичных артерий
- Эндоваскулярные методы лечения, стентирование сонных артерий
- Эндоваскулярные методы лечения, стентирование позвоночной артерии
- Методы лечения тромбоза глубоких вен ног (нижних конечностей)
- Методы лечения синдрома верхней полой вены (ВПВ)
