Методы лечения синдрома верхней полой вены (ВПВ)
Причиной синдрома верхней полой вены (ВПВ) является нарушение кровообращения в ней. Патологические процессы в соседних структурах могут привести к сдавлению или непосредственному поражению верхней полой вены (ВПВ). Выраженный венозный тромбоз приводит к развитию синдрома верхней полой вены (ВПВ) у 50% пациентов. В прошлом синдром верхней полой вены (ВПВ) чаще всего был следствием непосредственного сдавления опухолью. В настоящее время применение постоянных венозных катетеров в сочетании с ростом показателей выживаемости среди пациентов, перенесших химиотерапию, увеличивает частоту развития доброкачественного синдрома ВПВ у пациентов, проходящих лечение по поводу рака.
Широкое применение автоматического имплантируемого кардиовертера-дефибриллятора и многоэлектродных кардиостимуляторов увеличило частоту появления синдрома ВПВ и диагностирования этого состояния.
Чрескожное вмешательство при синдроме верхней полой вены (ВПВ). Определение и обзор консервативных и хирургических методов лечения синдрома ВПВ представлены в статье ниже. После первого описания положительных результатов чрескожного вмешательства при синдроме ВПВ у взрослых применение ангиопластики в качестве монотерапии было ограничено из-за высоких показателей неблагоприятных исходов и раннего рестеноза, вызываемого реакцией отдачи высокоэластичной стенки ВПВ.
Стентирование быстро стало популярным в данной области сосудистой терапии после первого сообщения в 1980-х гг. За истекший период были опубликованы сообщения о > 300 стентирований при синдроме ВПВ.
Стентирование при синдроме ВПВ злокачественной этиологии способствует быстрому разрешению симптомов. Пациенты практически сразу сообщают об устранении головной боли, нарушений зрения и других симптомов со стороны ЦНС. Такие симптомы, как одышка, кашель и отеки, как правило, разрешаются в течение 1-3 сут, однако иногда сохраняются в течение 1 нед. Стентирование способствует полному устранению симптомов у большинства пациентов с синдромом ВПВ злокачественной этиологии. В самой крупной серии исследований результаты, полученные у 76 пациентов с синдромом ВПВ, перенесших стентирование, сравнивали с данными пациентов из группы контроля, перенесших облучение. Метод был успешен в 100% случаев, у всех пациентов разрешение симптомов происходило в течение 48 час. 90% пациентов, подвергшихся стентированию, не имели симптомов обструкции ВПВ в момент смерти по сравнению с 12% пациентов, перенесших облучение.
Частота рецидивов синдрома ВПВ после чрескожного вмешательства значительно различалась у 45% пациентов. Это вполне объяснимо, поскольку причиной рецидива могут быть различные механизмы. Острый тромбоз стента вскоре после его установки может развиться у пациента, получающего недостаточную антикоагулянтную или антитромбоцитарную терапию. Возможно появление таких феноменов, как прорастание опухоли внутрь через отверстия стента, гиперплазия интимы или фиброзное рубцевание. Увеличение длины стента способно предупредить рецидив синдрома ВПВ, вызванный прорастанием опухоли за края стента, однако это может увеличить риск развития тромбоза или рестеноза стента ВПВ. Для пациентов с полной обструкцией ВПВ характерна наивысшая частота рецидивов синдрома ВПВ, но повторное проведение процедуры у таких пациентов, как правило, дает положительный результат в сочетании с установкой дополнительного стента, ангиопластикой, ТЛТ или комплексным применением этих методов.
В развитых странах синдром ВПВ незлокачественной этиологии (доброкачественный синдром ВПВ), как правило, имеет ятрогенное происхождение и чаще всего обусловлен использованием постоянных внутривенных катетеров и электродов кардиостимулятора. Такие осложнения, как венозный тромбоз и стеноз, связанные с установкой электрода кардиостимулятора, возникают у 30% пациентов, но лишь у некоторых из них появляются симптомы. Но наличие нескольких электродов, длительное использование поврежденного электрода или предшествующее инфицирование, вызванное установкой электрода, повышают риск развития синдрома ВПВ.
Самая крупная серия наблюдений чрескожного вмешательсва при доброкачественном синдроме ВПВ включала 16 больных. У 10 пациентов причиной развития синдрома ВПВ стал постоянный катетер, у 2 — электроды кардиостимулятора, у остальных — зоб, фиброзный медиасти-нит, трансплантация комплекса сердце-легкие и спонтанный тромбоз. Показатель проходимости сосудов у 13 пациентов, наблюдавшихся в среднем в течение 17 мес, составил 85%. Аналогичные результаты можно ожидать у пациентов с синдромом ВПВ, обусловленным применением центральных венозных инфузионных катетеров.
В идеале интервенционная терапия должна предусматривать удаление патогенных электродов или катетеров.
Таким образом, стентирование при злокачественной обструкции ВПВ является методом, не представляющим значительной опасности, обеспечивающим быстрое и длительное устранение симптоматики. Процедуру часто применяют в сочетании с химиотерапией или облучением с целью продления жизни пациенту и эффективного разрешения симптомов. Для пациентов с синдромом ВПВ незлокачественной этиологии стентирование является методом выбора, что подтверждено результатами среднесрочных наблюдений. Хирургическое вмешательство показано пациентам с доброкачественным синдромом ВПВ, рефрактерным к чрескожному вмешательству. К данной категории относится лишь небольшая часть пациентов, поскольку у большинства больных с рецидивирующим синдромом ВПВ наблюдаются положительные результаты после повторного чрескожного вмешательства.
Несмотря на различия в оборудовании и методах проведения процедур, основы эндоваскулярной терапии подходят для многих сосудистых зон. В целом стентирование сосудов стало основным направлением в чрескожной реваскуляризации, цель которой — устранение симптомов. В будущем основными задачами станут достижение стойких результатов эндоваскулярной терапии, а также изучение потенциала для профилактики осложнений прогрессирующей сосудистой патологии.
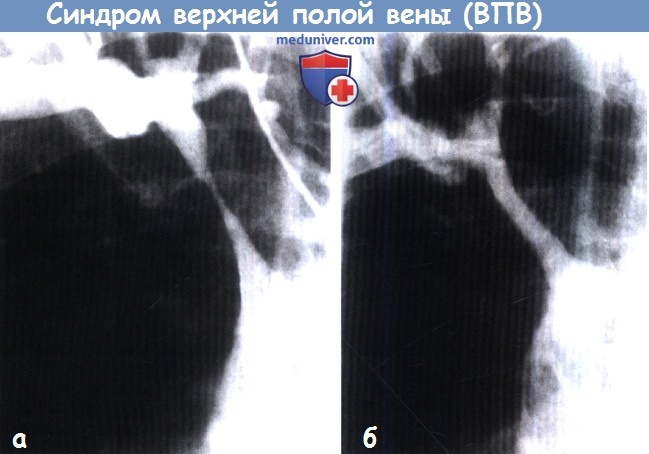
(А) Начальная флебограмма с выраженным стенозом верхней полой вены, который пройден 0,035-дюймовым проводником из бедренной вены.
Стеноз был предварительно дилатирован баллоном, и проведена установка большого самораскрывающегося стента для предотвращения реакции отдачи стенки сосуда.
(Б) Окончательная флебограмма.
- Читать "Сахарный диабет как причина болезней сердца"
Оглавление темы "Эндоваскулярное лечение стеноза сосудов.":- Эндоваскулярные методы лечения, стентирование бедренно-подколенной окклюзии
- Эндоваскулярные методы лечения, стентирование берцовой окклюзии
- Стеноз почечных артерий (СПА) - клиника, диагностика и лечение
- Хроническая брыжеечная ишемия (ХБИ) - клиника, диагностика и лечение
- Эндоваскулярные методы лечения, стентирование брахиоцефального ствола и подключичных артерий
- Эндоваскулярные методы лечения, стентирование сонных артерий
- Эндоваскулярные методы лечения, стентирование позвоночной артерии
- Методы лечения тромбоза глубоких вен ног (нижних конечностей)
- Методы лечения синдрома верхней полой вены (ВПВ)
