Эффективность стволовых клеток в лечении инфаркта миокарда
Все опубликованные работы демонстрируют, что инфузия аутологичных мононуклеарных клеток костного мозга (МККМ) безопасна и легко осуществима у пациентов с ОИМ. Исследование, выполненное Strauer B.E. и соавт., исследования TOPCARE-AMI и BOOST, исследование, проведенное Fernandez-Aviles F. и соавт., показали почти идентичные результаты: улучшение глобальной ФВ ЛЖ на 7-9%, значительное уменьшение конечного систолического объема ЛЖ и улучшение перфузии инфарцированной зоны через 4-6 мес после клеточной трансплантации клеток.
В то же время рандомизированное контролируемое исследование, проведенное Janssens S. и соавт., не выявило значительного эффекта на глобальную ФВ, а показало увеличение регионарной ФВ и уменьшение размера ИМ в группе, получавшей МККМ. Только одно большое исследование по трансплантации аутологичных СК при ОИМ — ASTAMI Autologous Stem-Cell Transplantation in Acute Myocardial Infarction) — не обнаружило никакого положительного эффекта. Причина отсутствия успеха клеточной терапии в исследовании ASTAMI неясна.
Поскольку доклинического функционального тестирования клеток, использовавшихся в исследовании ASTAMI, не проводили, невозможно судить о причинах отрицательного результата. Однако доклинические работы установили фундаментальную роль способа выделения клеток и техники манипуляции с ними для определения функциональной способности Кп, используемых для неоваскуляризации.
Все перечисленные исследования использовали всю популяцию мононуклеарных клеток костного мозга (МККМ), которая содержит 2-3% клеток CD34+, SP-клетки, мезенхимальные клетки и, вероятно, другие, пока еще не идентифицированные клеточные популяции. В одной из ветвей исследования TOPCARE-AMI у пациентов после ИМ, получивших культивированные ex vivo ЭКп, выявили улучшение функции сердца, как у тех, кто получал MKKM.
Следовательно, отдельные субпопуляции могут иметь одинаковую способность к функциональному восстановлению сердца, по крайней мере, при ОИМ. Подобным образом инфузия выделенных клеток CD133+, которые были обогащены ЭКп, увеличивала у пациентов с ОИМ глобальную ФВ.

в/м — внутримышечно; ИМ — инфаркт миокарда;
КМКп — костномозговые клетки-предшественники; МРТ — магнитно-резонансная томография;
ОИМ — острый инфаркт миокарда; ПЭТ — позитронная эмиссионная томография;
ЦКп — циркулирующие клетки-предшественники.
Положительные эффекты, наблюдавшиеся во всех пилотных исследованиях фазы I/II, были подтверждены крупнейшим на данный момент двойным слепым рандомизированным многоцентровым исследованием REPAIR-AMI, в котором использовали мононуклеарные клетки костного мозга (МККМ). Было продемонстрировано значительное увеличение глобальной и регионарной ФВ в группе больных, получавшей мононуклеарные клетки костного мозга (МККМ) (+5,5 процентных пункта-квантиля) по сравнению с плацебо (+3 процентных пункта-квантиля) после 4 мес наблюдения.
КСО в группе плацебо значительно увеличились, но остались неизменными в группе МККМ. В задачи исследования не входило изучение клинических конечных точек, тем не менее было выявлено, что частота совокупных событий (летальных исходов, ИМ и повторных госпитализаций в связи с СН) была значительно ниже после 1 года наблюдения у пациентов, получивших терапию МККМ, по сравнению с пациентами, получавшими плацебо.
Какие параметры могут влиять на исход? Большое количество пациентов, принявших участие в REPAIR-AMI, позволило протестировать некоторые вторичные конечные точки и разработать гипотезы для последующих исследований. Была выявлена значимая взаимосвязь между исходной ФВ и ее улучшением после терапии МККМ.
Пациенты с более низкой ФВ (< 48,9%) показывали значительное (в 3 раза выше) восстановление глобальной ФВ, указывающее на то, что у пациентов с более тяжелым ИМ терапия МККМ наиболее эффективна. И действительно, положительные эффекты в клинических конечных точках преимущественно наблюдались утех пациентов, которые исходно имели более низкую ФВ после ИМ. Это наблюдение подтвердило предыдущие результаты пилотного исследования TOPCARE-AMI.
Следующая определенная конечная точка давала ответ на вопрос «Влияет ли время введения мононуклеарных клеток костного мозга (МККМ) на исход?».
Удивительно, но пациенты, получившие терапию в период до 4 сут после ИМ, не имели преимуществ, в то время как позднее лечение (от 4 до 8 сут) обеспечивало положительную динамику ФВ во время наблюдения. Некоторые экспериментальные работы продемонстрировали обеспечение клетками цитопротективной активности параллельно с уменьшением апоптоза КМЦ. Это дает основание ожидать, что максимально эффективной будет наиболее ранняя инфузия клеток. На основании результатов исследования REPAIR-AMI можно предположить, что микроокружение после ОИМ меняется в течение первой недели после реперфузии, тем самым модулируя достижение введенными клетками цели и/или их последующую функциональную активность.
Хорошо известно, что ишемия/реперфузия вызывает преходящее изменение в экспрессии таких хемоаттрактивных факторов, как VEGF и SDF-1, которые важны для стимуляции перемещения и задержки клеток в тканях.
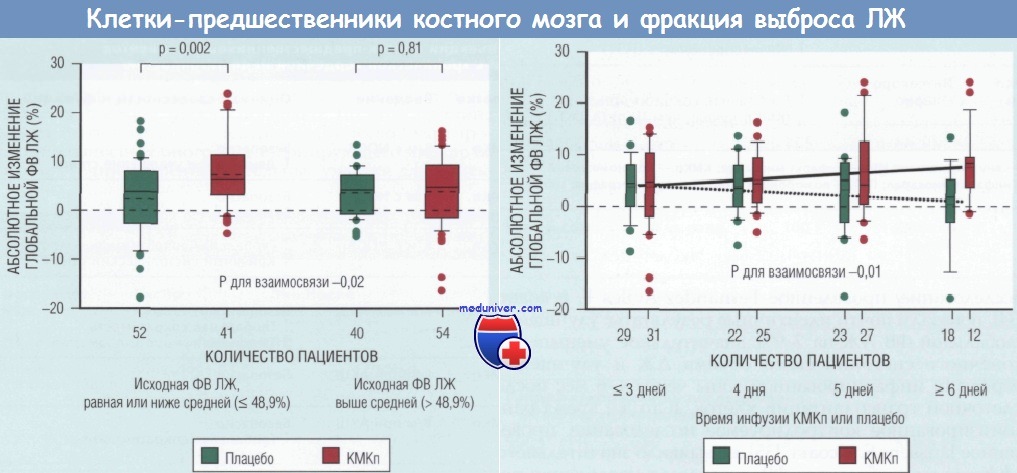
Взаимосвязь между исходной фракцией выброса левого желудочка и абсолютным ее изменением (А) и между временем интракоронарной инфузии костномозговых клеток-предшественников (КМКп) или плацебо после реперфузионной терапии и абсолютным изменением фракции выброса левого желудочка (Б).
На (А) значение Р для взаимосвязи определено методом дисперсионного анализа. На обоих графиках верхние и нижние границы каждого столбика диаграммы отражают 25-й и 75-й персентили, «усы» — 10-й и 90-й персентили, сплошная горизонтальная линия — медиану, пунктирная линия — среднее значение.
Все результаты, выходящие за пределы, представлены отдельными точками. На (Б) значение Р для взаимосвязи вычислялось с использованием общей линейной модели. Сплошная линия на (Б) — график регрессии для группы КМКп, а точечная линия — график регрессии для группы плацебо. ЛЖ — левый желудочек; ФВ — фракция выброса
Более того, начальное формирование отека сменяется преходящим вовлечением нескольких «волн» различных клеток. В связи с этим вполне возможно, что введение клеток будет наиболее полезным через несколько суток после реперфузии, а не сразу после нее. Ожидается, что последующие проспективные исследования дадут ответ и на этот вопрос.
Итак, доступные клинические данные указывают, что клеточная терапия элементами, полученными из костного мозга (КМ), достаточно легко выполнима и безопасна, исходя из имеющихся в настоящий момент результатов наблюдения (до 5 лет с момента начала первых работ). Ни в одном из исследований не отмечалось повышение частоты возникновения аритмий (как это было в исследованиях миобластов).
Более того, увеличение количества рестенозов, которые рассматривают как побочный эффект терапии Кп в виде образования бляшек или их воспаления, наблюдалось только при использовании клеток CD133+. Поскольку эти клетки выделяли с помощью мышиных антител, логично предположить, что антитела могли запускать локальную провоспалительную реакцию, хотя данные об образовании системных антимышиных антител у пациентов отсутствовали.
Во всех остальных исследованиях повышенного риска рестенозов не наблюдалось; даже наоборот, в исследовании REPAIR-AMI отмечалось значительное снижение потребности в процедурах по реваскуляризации.
Остается неясным, сохраняется ли улучшение, наблюдаемое в течение первых 6 мес после клеточной терапии, в течение более продолжительного периода. Тщательная оценка наблюдений в сроки до 18 мес в исследовании BOOST показывает, что ФВ у пациентов из группы клеточной терапии сохраняется неизменной от 6 до 18 мес, однако различия между получавшими клеточную терапию и контролем не были статистически значимы, т.к. увеличение ФВ наблюдалось и в контрольной группе. Небольшое количество пациентов (п = 30) недостаточно для определения статистических различий между двумя группами.
Долгосрочное наблюдение в течение 2 лет в ходе исследования TOPCARE-AMI на основании результатов МРТ показало, что ФВ сохраняется и даже улучшается у пациентов, получавших лечение наряду с параллельным стойким снижением уровней N-терминального натрийуретического пропептида В-типа, что дает основания предположить положительный эффект в плане долгосрочного ремоделироваия ЛЖ (Dimmeler S. и Zeiher A.M., неопубликованные данные). Все это свидетельствует о необходимости дальнейшей оценки влияния интракоронарного введения МККМ на клинический исход на большей когорте пациентов, перенесших тяжелый ИМ.
- Читать "Эффективность клеточной мобилизации в лечении инфаркта миокарда"
Оглавление темы "Лечение сердечной недостаточности":- Эффективность стволовых клеток в лечении инфаркта миокарда
- Эффективность клеточной мобилизации в лечении инфаркта миокарда
- Эффективность стволовых клеток и клеточной мобилизации в лечении ХСН
- Перспективы применения стволовых клеток и клеточной терапии болезней сердца
- Генная терапия болезней сердца и сердечной недостаточности
- Фармакогенетика терапии сердечной недостаточности
- Мильдоний и другие метаболические средства в лечении сердечной недостаточности
- Иммуномодуляторы в лечении сердечной недостаточности - эффективность статинов
- История паллиативной помощи больным с неизлечимыми заболеваниями
- Смертность от сердечно-сосудистых заболеваний в США
