Внутрибольничная пневмония в отделениях неврологии
Внутрибольничная пневмония — это пневмония, развившаяся через 48 ч и более после госпитализации больного при отсутствии инкубационного периода на момент поступления в стационар. Развитие пневмонии у неврологических больных сопровождается увеличением продолжительности пребывания в больнице, существенным удорожанием лечения и ростом показателей летальности. Одной из особенностей лечебного процесса является перевод в НО пациентов после оказания медицинской помощи в ОРИТ (например, при инсульте). Кроме того, во многих отделениях неврологии имеются блоки или палаты интенсивной терапии (БИТ, ПИТ).
Пневмонии составляют 44% от всех ВБИ в ОРИТ, у 18,9% больных они развиваются в ходе интенсивной терапии. Интубация и искусственная вентиляция легких, осуществляемые в ОРИТ, значительно увеличивают риск развития ВБП.
Пневмония — ведущая причина летальности, связанной с ВБИ, в НО. Ориентировочная частота летальных исходов при этой ВБИ составляет 30%, а летальность при вентилятор-ассоциированных пневмониях (ВАП) может достигать 71%.
К группе высокого риска возникновения пневмонии с неблагоприятным исходом относятся пациенты с тяжелым течением основного неврологического заболевания, с нарушенным сознанием, находившиеся ранее на ИВЛ, интубированные больные. Каждые сутки пребывания больного на ИВЛ увеличивают риск развития ВБП на 1-3%.
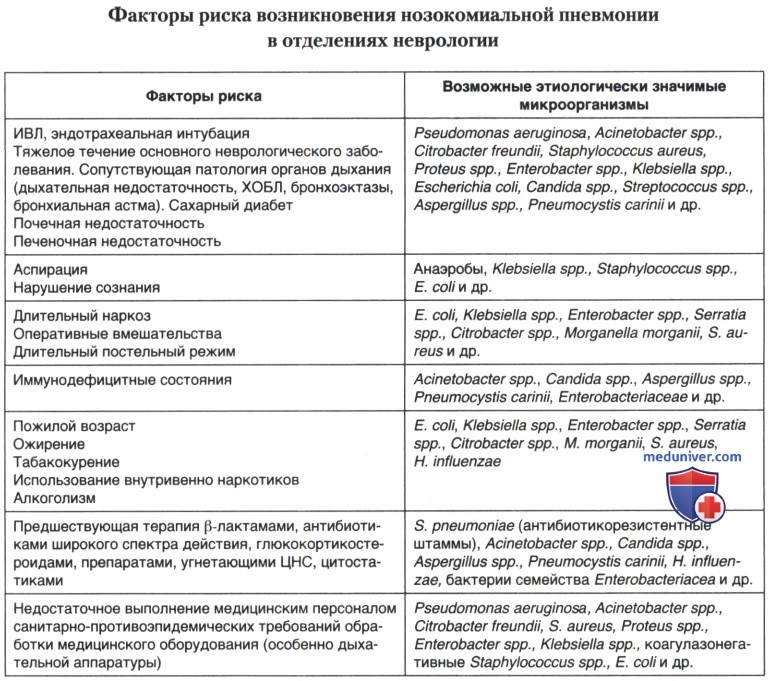
Факторы риска возникновения ВБП у больных НО представлены в таблице ниже. Кроме вышеперечисленных, это тяжелые сопутствующие заболевания, длительная госпитализация и/или послеоперационный период, постельный режим, анестезия и операции на органах грудной и брюшной полости, табакокурение, пожилой возраст, ожирение, сахарный диабет, алкоголизм, иммунодефицитные состояния, продолжительное и неадекватное применение антибиотиков, особенно предшествующая терапия β-лактамами.
Известно, что микроорганизмы, продуцирующие БЛРС, часто устойчивы к другим классам антибиотиков, включая аминогликозиды и фторхинолоны. Препараты, угнетающие ЦНС, кортикостероиды и цитостатики, так же как и продолжительное и неадекватное применение антибиотиков, подавляют иммунитет.
Длительный наркоз приводит к нарушению деятельности мерцательного эпителия слизистых оболочек дыхательных путей. Дисфункция ресничек эпителия отмечается в течение 2-3 суток после оперативного вмешательства.
Немалое значение имеет и недостаточное выполнение медицинским персоналом санитарно-гигиенических требований, неполная дезинфекция оборудования, особенно дыхательной аппаратуры.
Выделяют следующие пути инфицирования легких в условиях НО:
• экзогенный (через воздух, ингалируемые медицинские газы, инфицированную эндотрахеальную трубку или эндоскоп, оборудование для проведения ИВЛ);
• эндогенный (аспирация секрета из ротоглотки, аспирация содержимого пищевода и желудка, гематогенное инфицирование из отдаленных очагов инфекции, транслокация микроорганизмов из желудочно-кишечного тракта, инфицирование из плевральной полости). Таким образом, к эндогенным источникам инфицирования легких относятся микрофлора носоглотки, ротоглотки, придаточных пазух носа, желудочно-кишечного тракта, кожи, возбудители из альтернативных очагов инфекции.
Диагностика ВБП основывается прежде всего на данных рентгенологического исследования легких — появлении на рентгенограмме свежих очаговых изменений в легких. Клинические признаки ВБП — повышение температуры тела свыше 38°С, кашель, бронхиальная гиперсекреция, локально выслушиваемые хрипы в легких, бронхиальное дыхание, гнойная мокрота. В общем анализе крови выявляют лейкопению или лейкоцитоз, палочкоядерный сдвиг более 10%.
Пневмония, развившаяся на фоне нейтропении, практически всегда является госпитальной. К нейтропении относят состояния, при которых концентрация нейтрофилов ниже 500 клеток в 1 мм3. Различают транзиторную и продолжительную (более 7 дней) нейтропению. Нейтропению наблюдают:
• у онкогематологических больных и у больных с солидными злокачественными новообразованиями на фоне цитотоксического лечения;
• у реципиентов донорских органов, получающих иммуносупрессивную терапию;
• на фоне длительной иммуносупрессивной терапии (включая кортикостероиды), проводимой по различным показаниям.
Спектр возбудителей нозокомиальной пневмонии является полимикробным, свойственным для конкретного неврологического стационара. Их распространение определяется особенностями микроэкологической среды, формирующейся в условиях того или иного НО. Они зависят от характера патологических процессов у больных, в отношении которых специализируется отделение, особенностей лечебно-диагностических процедур, характера и возможности формирования госпитальных штаммов.
Этиологическим фактором ВБП в НО наиболее часто являются: Р. aeruginosa (до 30%), S. aureus (до 30%), Acinetobacter spp. (до 10%). Значимую роль играют Enterobacter spp., Е. coli, К. pneumoniae, Proteus spp., Serratia marcescens, H. influenzae, S. pneumoniae. Многие штаммы указанных патогенов, как отмечено ранее, обладают устойчивостью к пенициллинам, цефалоспоринам I—III поколений, аминогликозидам. При тяжелом течении могут выделяться высокорезистентные грамотрицательные микроорганизмы (Р. aeruginosa, Acinetobacter spp., метициллин-резистентный S. aureus (MRSA), Candida spp., Aspergillus spp., Pneumocystis carinii).
При искусственной вентиляции легких возможно другое соотношение этиологически значимых микроорганизмов: Р. aeruginosa spp. (41%), Acinetobacter spp. (12%), S. aureus (11%), Proteus spp. (11%), Enterobacter spp. (9%), Klebsiella spp. (5%), другие представители Staphylococcus spp. (7%), E. coli (3%), Candida spp. (1%).
Пневмонии, развившиеся на фоне нейтропении, отличаются от других госпитальных пневмоний возрастанием роли сравнительно мало патогенных микроорганизмов:
• коагулазонегативных стафилококков;
• стрептококков группы «viridans»;
• энтерококков;
• грибов (Candida spp., Aspergillus spp.).
При наличии нейтропении базисная терапии включает эритромицин (так как частым возбудителем пневмонии у этих пациентов является легионелла).

Препараты выбора при нейтропении: карбапенемы, антипсевдомонадные цефа-лоспорины III—IV поколения + аминогликозиды (при назначении аминогликозидов следует учитывать высокую частоту распространения устойчивости к гентамицину), фторхинолоны, гликопептиды (гликопептиды показаны при подтверждении либо высокой вероятности этиологической роли метициллин-резистентных стафилококков или энтерококков). При эмпирической терапии основанием для назначения гликопептидов является неэффективность предшествовавшей терапии.
Таким образом, чаще всего ВБП в НО имеют полимикробную бактериальную этиологию. В большинстве случаев их развитие обусловлено аэробными грамотрицательными бактериями и грамноложительными кокками (S. aureus).
В неврологическом отделении необходимо строгое соблюдение мер по прерыванию путей передачи возбудителей при угрозе возникновения экзогенной инфекции из внутрибольничной среды. К ним относятся: дезинфекция и соответствующий уход за оборудованием, применяемым в блоках интенсивной терапии НО, использование стерильной воды для промывания оборудования многоразового использования, соблюдение барьерных мер предосторожности при контакте с секретом дыхательных путей. Один их основных факторов, играющий важную роль в распространении ВВП, — перекрестная колонизация в ОРИТ, ПИТ и непосредственно в НО, инфицирование антибиотикорезистентными штаммами.
Профилактика перекрестной контаминации или колонизации пациентов через руки медперсонала является необходимой мерой по предотвращению ВВП, а гигиена рук — неотъемлемой частью системы мер борьбы и профилактики ВБП, в частности, ВБП, в отделениях неврологии. Мытье рук медицинского персонала после оказания помощи каждому пациенту и использование перчаток при проведении процедур позволяют значительно снизить перекрестную контаминацию больных в условиях НО.
Колонизация трахеи у находящихся на ИВЛ может быть следствием миграции микроорганизмов с манжеты эндотрахеальной трубки, на которой они постепенно скапливаются, на поверхность трубки, образуя биопленку, защищающую от воздействия антимикробных препаратов и защитных сил организма.
Аспирация бактерий из носоглотки и верхних отделов желудочно-кишечного тракта в нижние дыхательные пути — наиболее распространенный механизм развития ВБП. Установка назогастрального зонда может быть причиной рефлюкса желудочного содержимого и способствовать колонизации носоглотки.
Предполагают, что именно колонизация ротоглотки грамотрицательными бактериями, с последующей микроаспирацией и попаданием их в легкие, является наиболее значимым механизмом развития вентилятор-ассоциированных пневмоний. Для профилактики орофарингеальной колонизации следует проводить адекватный туалет ротоглотки 0,12% раствором хлоргексидина.
Для предотвращения аспирации, связанной с кормлением пациентов через зонд, рекомендуется приподнятое положение верхней части туловища на 30°-45°; по возможности быстрое прекращение зондового питания и удаление зонда; эффективное дренирование подсвязочного пространства.
В Блоках интенсивной терапии НО при использовании аппаратов ИВЛ все расходные материалы, соприкасающиеся с дыхательными путями пациента, должны быть стерильными (эндотрахеальные трубки, трахеостомические канюли, катетеры для аспирации секрета трахеобронхиального дерева). Рекомендуется удаление эндо-трахеальных, трахеостомических и энтеральных трубок немедленно после устранения причин для их применения. Показаниями для замены дыхательного контура аппаратов ИВЛ являются явное загрязнение и/или нарушение его функционирования. Замену дыхательного контура аппаратов ИВЛ рекомендуется проводить не чаще, чем через каждые 48 ч.
Показано периодическое удаление конденсата из трубок дыхательного контура аппаратов ИВЛ, который может быть контаминирован микроорганизмами. В дыхательном контуре в обязательном порядке должны использоваться бактериальные фильтры.
У пациентов, находящихся на ИВЛ, необходимо использовать все возможные нефармакологические методы, направленные на уменьшение гастроэзофагеального рефлюкса, предотвращение аспирации и непосредственного попадания патогенов в нижние дыхательные пути, что будет способствовать эффективному снижению частоты возникновения ВАП. К ним относятся: аспирация секрета из надманжетного пространства у больных на ИВЛ, дренирование подсвязочного пространства, приподнимание головного конца кровати и тщательный уход за дыхательной аппаратурой, включающий периодический контроль давления в дыхательном контуре.
Серьезной проблемой является проведение этиотропного лечения ВБП, возникших в НО больниц. Оно требует непрерывного контроля за проведением антибиотикотерапии, направленной на уменьшение селективного давления антимикробных препаратов. Частота БЛРС-продуцирующих возбудителей ВБП неодинакова в НО различных медицинских учреждений.
Однако многочисленные исследования свидетельствуют о драматическом увеличении за последние 10 лет превалирования в ОРИТ, блоках интенсивной терапии НО и отделениях неврологии продуцентов БЛРС практически во всех регионах мира. По данным многоцентрового исследования MYSTIC, в Европе наибольшая частота БЛРС отмечается в России, Польше и Турции.
Продуцентами БЛРС в НО могут быть различные грамотрицательные бактерии, но наиболее часто они определяются у Klebsiella spp., Escherichia coli, Enterobacter spp., Serratia spp., Citrobacter spp. Все бактерии, продуцирующие БЛРС, можно определенно отнести к полирезистентным. Сниженная чувствительность in vitro хотя бы к одному из тестируемых цефалоспоринов III поколения является косвенным признаком продукции БЛРС.
Практически важно помнить, что устойчивость штаммов-продуцентов БЛРС к цефалоспоринам III поколения часто ассоциируется с устойчивостью к аминогликозидам и фторхинолонам. Активность in vitro и клиническую эффективность в отношении этих микроорганизмов могут сохранять ингибитор-защищенные β-лактамы (пиперациллин/тазобактам, цефоперазон/сульбактам) и цефалоспорины IV поколения (цефепим). Но наиболее надежным арсеналом антибактериальной терапии являются карбапенемы — имипенем, меропенем, эртапенем. При наличии MRSA к ним присоединяют линезолид или ванкомицин.
- Читать далее "Инфекция кровотока (сепсис) в отделениях неврологии"
Редактор: Искандер Милевски. Дата публикации: 19.11.2020
- Туберкулез в психиатрических стационарах
- Внутрибольничные инфекции (ВБИ) в отделениях неврологии
- Внутрибольничная пневмония в отделениях неврологии
- Инфекция кровотока (сепсис) в отделениях неврологии
- Инфекция мочевыводящих путей в отделении неврологии
- Болезнь Крейтцфельдта-Якоба (БКЯ) как новая внутрибольничная инфекция
- Внутрибольничные инфекции (ВБИ) в эндоскопии
- Конструктивные особенности эндоскопов значимые в эпидемологии внутрибольничных инфекций
- Типы инфицирования пациентов в эндоскопии
- Этиология внутрибольничных инфекций (ВБИ) в эндоскопии
