Факторы риска стентирования коронарных артерий (чрескожного коронарного вмешательства, ЧКВ)
Оценка потенциальных преимуществ и рисков чрескожного коронарного вмешательства (ЧКВ) предполагает анализ 5 основных факторов риска: объема пораженного миокарда, морфологических особенностей поражения КА, функционального состояния сердечнососудистой системы (в т.ч. функции ЛЖ, характера ритма, сопутствующей патологии клапанов), наличия дисфункции почек и коморбидной патологии, которая может увеличивать риск ЧКВ.
Каждый из этих факторов риска (ФР) независимо определяет преимущества и риски ЧКВ. Адекватное планирование ЧКВ заключается в тщательном анализе этих факторов.
а) Объем пораженного миокарда. Площадь жизнеспособного миокарда, кровоснабжаемого соответствующей КА, является основным фактором, определяющим непосредственный риск стентирования (ЧКВ). Вмешательство на коронарном сосуде приводит к остановке коронарного кровотока на несколько секунд или минут, поэтому способность организма перенести достаточно длительную окклюзию КА зависит от площади жизнеспособного миокарда, кровоснабжаемого этим сосудом, и от наличия и выраженности коллатерального кровообращения в ишемизированной зоне.
Хотя риск острой окклюзии значительно уменьшился с появлением коронарных стентов, развитие других интраоперационных осложнений, в частности окклюзии большой боковой ветви, дистальной эмболии, перфорации или отсутствия восстановления кровотока (феномен no reflow), может привести к быстрому ухудшению состояния больного в зависимости от площади пораженного миокарда. При возникновении тромбоза стента клинические последствия также зависят от площади миокарда, кровоснабжаемого через этот стент.
Предикторами развития сердечно-сосудистого коллапса при наличии осложнений ЧКВ являются площадь пораженного миокарда, диаметр сосуда до проведения процедуры, многососудистое поражение и диффузный характер поражения.
Вопрос проведения полной реваскуляризации при наличии многососудистого поражения в один или несколько этапов остается спорным. При ИМ↑ST обычно рекомендуется проводить реваскуляризацию только соответствующей инфаркт-зависимой КА при условии отсутствия у пациента кардиогенного шока, обусловленного поражением других участков миокарда. В этих случаях можно отсрочить дальнейшую реваскуляризацию на 3-7 дней.
В остальных ситуациях количество сосудов, подвергаемых пластике в течение одной процедуры, определяется наличием осложнений во время вмешательства, временем, необходимым для вмешательства на дополнительных сосудах, функциональным состоянием почек, а также способностью пациента перенести длительную процедуру. Следующий этап можно выполнить через 4-8 нед после первичного вмешательства.

б) Морфологические особенности поражения коронарных артерий (КА). Ряд ангиографических особенностей увеличивают техническую сложность ЧКВ и риск развития осложнений в ближайшем и отдаленном периодах. Появление коронарных стентов позволило снизить потребность в экстренной операции КШ с 3-8% при БАП до 1% при имплантации стента, но все же сохраняется риск развития интраоперационного ИМ, тромбоза стента или дистальной эмболии и феномена no reflow.
Проходимость сосуда и характер его поражения остаются важными предикторами исходов вмешательства у больных, которым имплантируют стент. Недавно проведенные анализы регистров подтвердили влияние характера поражения сосудов на успех вмешательства и риск развития осложнений в ближайшем и отдаленном периодах.
1. Хроническая тотальная окклюзия. Окклюзия КА возникает у 50% больных с тяжелой КБС (стеноз > 70%) и является наиболее частой причиной направления больных на операцию КШ, а не на ЧКВ. Результаты реканализации тотальной окклюзии КА с помощью проводника зависят от длительности и протяженности (> 15 мм) окклюзии, наличия коллатералей, отсутствия или наличия «ниппеля», обеспечивающего продвижение проводника. Хотя в настоящее время используют новые технологии для реканализации даже рефрактерной окклюзии, техническое усовершенствование проводников и катетеров позволило улучшить показатели за последние годы. После реканализации тотальной окклюзии возможна имплантация стента с лекарственным покрытием с целью профилактики рецидива.
2. Шунты из большой подкожной вены. Вмешательства на венозных шунтах составляют 8% всех ЧКВ; при этом отмечается повышенный риск развития ИМ после вмешательства вследствие атероэмболий во время ЧКВ. При отсутствии восстановления кровотока введение артериальных вазодилататоров в венозный шунт может улучшить кровоток в дистальных сосудах, однако все равно сохраняется высокий риск смерти и ИМ. Более выраженная дегенерация шунта и более выраженная окклюзия (АБ большого размера) ассоциируются с более высоким риском осложнений, чем при менее выраженном поражении венозного шунта.
При наличии анатомических особенностей, свидетельствующих о высоком риске поражения венозного шунта, следует использовать альтернативные подходы через нативные КА, если это возможно. Уровень рестенозов венозных шунтов после имплантации стентов более низкий, чем после БАП. Применение стентов с лекарственным покрытием еще больше снижает частоту рестенозов, но стенты с сиролимусом не подходят для венозных шунтов диаметром > 4,5 мм, в этих случаях следует выбирать металлические стенты без покрытия.
3. Поражение в области бифуркации. Продолжаются споры относительно оптимального метода лечения поражений с вовлечением обеих ветвей в области бифуркации КА. «Проваливание» АБ в прилегающий основной сосуд или в боковую ветвь ограничивает возможности обычной БАП. Устройства для удаления АБ, используемые, например, при направленной атерэктомии, лишь частично уменьшают этот риск. Стратификация риска перед проведением ЧКВ при бифуркационном поражении включает определение степени атеросклеротического поражения обоих сосудов, оценку относительного размера сосуда и распространение поражения в основном сосуде и боковой ветви, а также расположения сосудов относительно друг друга.
Обычно предпочтительнее имплантация стента в один сосуд, а не одновременно в основной сосуд и боковую ветвь, но при распространенном поражении обоих сосудов используют различные стратегии — одновременную имплантацию двух стентов методами kissing, crush, culotte или Т-стентирование. По-видимому, применение стентов с лекарственным покрытием способствует уменьшению частоты рестенозов по сравнению с использованием металлических стентов без покрытия, однако рестеноз после имплантации стента с лекарственным покрытием обычно возникает в устье боковой ветви. Независимо от метода коррекции бифуркационного поражения необходимо выполнить заключительную баллонную дилатацию по kissing-технологии основного сосуда и боковой ветви.
В настоящее время проводят клинические исследования новых стентов для бифуркаций КА, и результаты их обнадеживают.
4. Кальцинированное поражение. Наличие диффузного кальциноза в КА создает определенные сложности для проведения ЧКВ, поскольку наличие кальция в стенке сосуда приводит к неравномерности сужений и нарушению эластичности, что очень затрудняет введение проводников, баллонов и стентов. Диффузная кальцинация коронарных сосудов также делает стенку артерии ригидной, что требует большего давления в баллоне для достижения полного расправления стента, при этом иногда встречаются недилатируемые участки, которые остаются резистентными к любому уровню давления. Ротационная атерэктомия существенно уменьшает степень кальцинации сосудистой стенки и облегчает доставку и расправление стента.
5. Тромб. Обычная ангиография обладает низкой чувствительностью в отношении выявления тромбов в КА, а наличие большого, выявляемого при ангиографии тромба увеличивает риск осложнений во время процедуры. Тромб больших размеров может во время ЧКВ фрагментироваться, что приведет к эмболии. Тромб также может попасть между элементами стента и сузить просвет сосуда, возможен даже острый тромбоз соответствующего сосуда. Кроме того, большие коронарные тромбы могут вызывать эмболию других КА или попадать в кровоток головного мозга и других органов.
в) Предрасполагающее функциональное состояние сердца. Функция ЛЖ является важным предиктором исхода ЧКВ. На каждые 10% снижения ФВ в покое приходится двукратное увеличение госпитальной смертности после ЧКВ. Наличие сопутствующей патологии клапанного аппарата или желудочковых аритмий еще больше увеличивает риск ЧКВ при дисфункции ЛЖ. При наличии тяжелой дисфункции ЛЖ (ФВ < 35%) или большом объеме пораженного миокарда может быть полезной внутриаортальная баллонная контрпульсация. Устройства для кардиопульмональной поддержки, которые не способствовали снижению давления в ЛЖ, были заменены на чрескожные устройства для поддержки функции ЛЖ, размещаемые в левом предсердии (например, TandemHeart, CardiacAssist Inc., Pittsburgh, PA) или непосредственно в ЛЖ (например, Impella LP 2.5, Abiomed Inc., Danvers, MA).
Эти устройства позволяют выполнять ЧКВ больным очень высокого риска без развития гемодинамического коллапса во время процедуры.
г) Почечная недостаточность. Заболеваемость и смертность, ассоциированные с ЧКВ, непосредственно связаны со степенью поражения почек. У больных даже с незначительной дисфункцией почек риск смерти в течение 1 года после ЧКВ на 20% выше, чем у пациентов с нормальной функцией почек. Нарушение функции почек после введения контрастного вещества во время ангиографии может быть связано с контраст-индуцированной нефропатией, синдромом холестериновой эмболии или с их сочетанием.
Риск контраст-индуцированной нефропатии определяется дозой контрастного вещества, степенью гидратации во время процедуры, исходным состоянием функции почек, возрастом, состоянием гемодинамики, наличием анемии и СД, а риск синдрома холестериновой эмболии зависит от характера манипуляций на восходящей или нисходящей аорте, пораженной атеросклерозом, что приводит к высвобождению кристаллов холестерина. Хотя риск гемодиализа у больных с неосложненной контраст-индуцированной нефропатией составляет < 3%, госпитальная смертность больных на гемодиализе > 30%. Незначительная дисфункция почек после ЧКВ может увеличить риск смерти в течение 1 года в 4 раза по сравнению с пациентами с нормальной функцией почек.
д) Сопутствующая патология. Некоторые сопутствующие заболевания могут увеличивать ближайший и отдаленный риск ЧКВ, что необходимо учитывать при оценке рисков, преимуществ и выборе тактики у больных, направленных на ЧКВ. У пациентов с СД частота рецидивов выше при использовании металлических стентов без покрытия, кроме того, у таких больных было продемонстрировано преимущество операции КШ по сравнению с БАП нескольких сосудов в отношении выживаемости. В настоящее время проводят исследования с целью определения, сохраняется ли такое же преимущество при использовании стентов с лекарственным покрытием.
Наличие геморрагического диатеза или необходимость постоянной терапии варфарином могут быть препятствиями для длительного приема комбинации аспирина и клопидогрела, повышая тем самым риск тромбоза стента. Необходимость отмены двойной антитромбоцитарной терапии перед некардиохирургическим вмешательством вскоре после имплантации стента также может привести к его тромбозу. В этих случаях методом выбора может быть имплантация металлического стента без покрытия, особенно если предстоящую операцию можно отложить на 6-8 нед после имплантации стента.
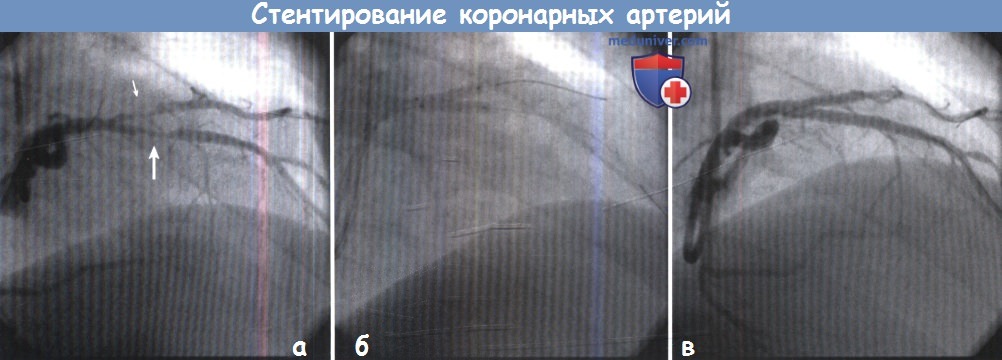
(А) Сложное бифуркационное поражение с вовлечением ЛПНА (большая стрелка) и ее диагональной ветви (маленькая стрелка).
(Б) После расширения обеих ветвей с помощью баллона выполнена одновременная имплантация двух стентов Cypher размером 3 x 18 мм в ЛПНА и диагональную ветвь.
(В) В результате постдилатации обеих артерий с одновременным расправлением стентов удалось достичь очень хорошего ангиографического результата.

(А) Сложное бифуркационное поражение с вовлечением ЛПНА (большая стрелка) и ее диагональной ветви (маленькая стрелка).
(Б) После расширения обеих ветвей с помощью баллона выполнена одновременная имплантация двух стентов Cypher размером 3 x 18 мм в ЛПНА и диагональную ветвь.
(В) В результате постдилатации обеих артерий с одновременным расправлением стентов удалось достичь очень хорошего ангиографического результата.
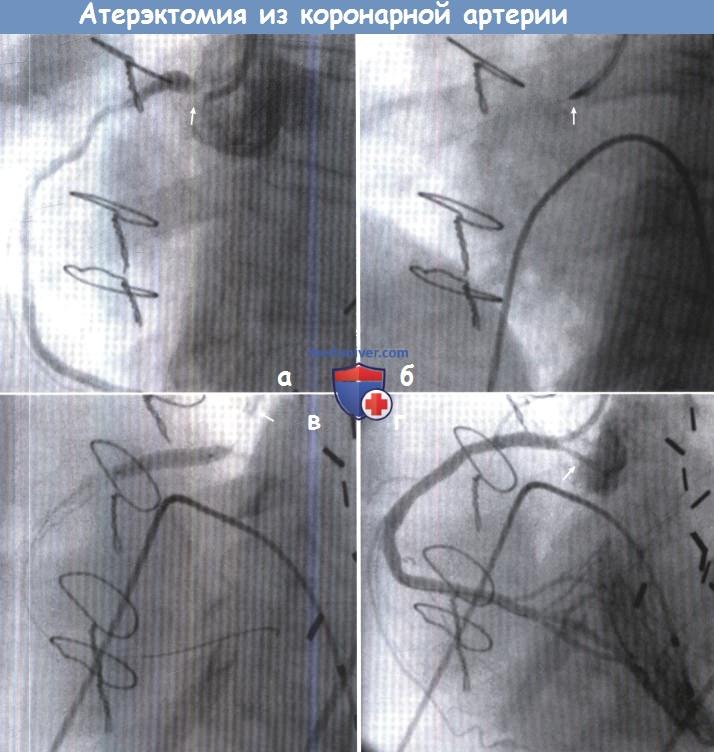
(А) Выраженный кальциноз устья ПКА (стрелка) делает невозможным проведение обычной БАП с имплантацией стента.
(Б) Наконечник (стрелка) для ротационной атерэктомии диаметром 1,25 мм был введен в сосуд для удаления кальция из устья артерии.
Дополнительно был использован наконечник для ротационной атерэктомии диаметром 1,50 мм для полного удаления кальцинированной бляшки.
(В) После предилатации с помощью баллона диаметром 2,5 мм в сосуд поставили стент Cypher (Cordis Corp, Warren, NJ) размером 3,5 x 23 мм и расправили поддавлением 16 атм.
Обратите внимание, что проводник удалили (стрелка), чтобы имплантировать стент в самое устье ПКА.
(Г) Достигнут очень хороший ангиографический результат, признаков остаточных стенозов нет.
Обратите внимание на свободное поступление контрастного вещества из устья после имплантации стента (стрелка).
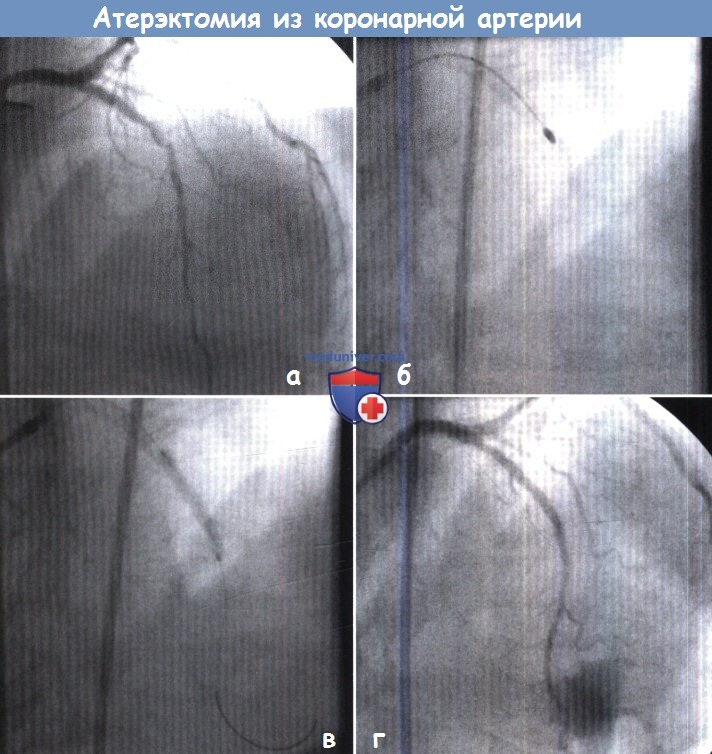
(А) Выраженный кальциноз и диффузный стеноз ЛПНА, выполнение обычной баллонной ангиопластики признано невозможным.
(Б) Наконечник для ротационной атерэктомии диаметром 1,5 мм, вращающийся с частотой 160 000 об/мин, был введен в сосуд для удаления кальция.
(В) После этого стало возможным провести через место сужения стент размером 3 х 28 мм и расправить его под давлением 16 атм.
Полное расправление стента было бы невозможно без предварительной атерэктомии.
(Г) На последней ангиограмме остаточные стенозы отсутствуют, определеляется нормальный кровоток по дистальным сосудам.
- Читать "Сосудистый доступ при стентировании коронарной артерии (чрескожном коронарном вмешательстве, ЧКВ)"
Оглавление темы "Стентирование коронарных артерий (чрескожное коронарное вмешательство, ЧКВ).":- История и варианты чрескожного коронарного вмешательства (ЧКВ)
- Показания для стентирования коронарных артерий (чрескожного коронарного вмешательства, ЧКВ)
- Факторы риска стентирования коронарных артерий (чрескожного коронарного вмешательства, ЧКВ)
- Сосудистый доступ при стентировании коронарной артерии (чрескожном коронарном вмешательстве, ЧКВ)
- Что делают при баллонной ангиопластике (БАП)? Возможности
- Что делают при коронарной атерэктомии? Возможности
- Что делают при тромбэктомии? Возможности
- Устройства для профилактики эмболии коронарных артерий после чрескожного коронарного вмешательства (ЧКВ)
- Виды коронарных стентов и их возможности
- Антитромбоцитарные средства при стентировании коронарных артерий (чрескожном коронарном вмешательстве, ЧКВ)
