Лечение, профилактика инфекций у травматологических и ортопедических пациентов
При разработке схем антибиотикопрофилактики и эмпирической терапии имеют существенное значение сведения, полученные в результате микробиологических исследований. Они должны быть дополнены данными о чувствительности выделенных культур микроорганизмов к антибактериальным препаратам (АБП).
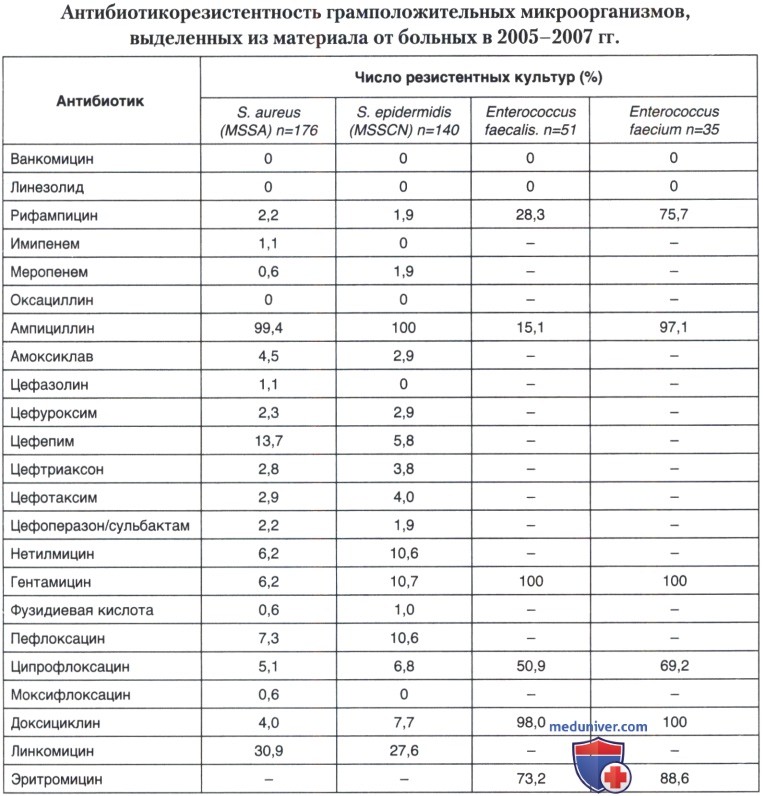
Результаты определения резистентности грамположительных микроорганизмов, выделенных из материала от больных ЦИТО в 2005-2007 гг., к АБП представлены в табл. 7.4. Следует подчеркнуть, что отношение к метициллину (оксациллину) является основополагающим моментом при оценке антибиотикорезистентности бактерий рода Staphylococcus, поскольку именно эти данные служат отправной точкой при выборе антибиотика. С целью эмпирической терапии используют те антимикробные средства, резистентность к которым не превышает 25%.
Бактерии рода Staphylococcus, чувствительные к оксациллину (метициллину, MS-штаммы), демонстрировали in vitro низкую резистентность к широкому ряду антимикробных препаратов. Среди них не выявлено штаммов, устойчивых к ванкомицину и линезолиду. Частота резистентности культур 5. aureus менее 15% отмечена практически для всех препаратов, в отношении которых определялся этот показатель. Исключение составили линкомицин и ампициллин — к этим антибиотикам были устойчивы 30,9 и 99,4% культур соответственно. Резистентность культур S. epidermidis была практически идентична таковой для S. aureus.
Следовательно, перечень антибиотиков, которые могут быть применены для лечения инфекционных осложнений, вызванных метициллин-чувствительными (MS) штаммами стафилококка, достаточно широк. Эти же препараты могут быть использованы для эмпирической терапии — за исключением тех случаев, когда комплексная оценка состояния больного диктует необходимость применения сразу ванкомицина или линезолида.
Весьма ограничено число антибиотиков, активных в отношении бактерий рода Enterococcus, особенно Е. faecium. Представляется важным в каждом случае выявления энтерококков в материале от больных оценивать их клиническую значимость и, следовательно, необходимость антибактериальной терапии с тем, чтобы не использовать препараты резерва не по назначению.
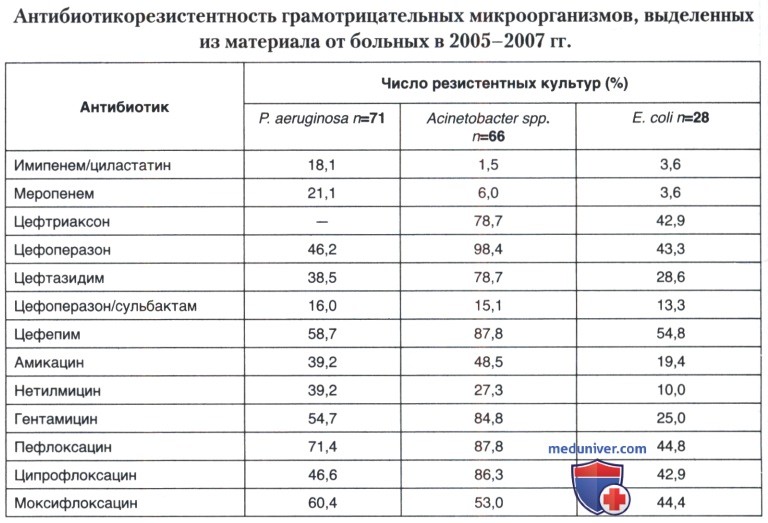
Результаты определения антибиотикорезистентности грамотрицательных бактерий свидетельствуют о проблематичности адекватной антибиотикотерапии инфекционных осложнений, вызванных Р. aeruginosa и бактериями рода Acinetobacter. Среди культур Р. aeruginosa 18,1% были устойчивы к имипенем/ циластатину и 21,1% — к меропенему, препаратам, относящимся, как известно, к числу наиболее высокоактивных. Самой низкой оказалась частота резистентности к цефоиеразон/сульбактаму — 16%. Устойчивость к остальным антибиотикам превышала 30%.
Культуры Acinetobacter spp. демонстрировали низкую резистентность к имипенем/циластатину (1,5%), меронему (6%) и цефоперазон/сульбактаму (15,1%). Все прочие препараты, к которым определяли резистентность, могут быть использованы для лечения соответствующей инфекции только на основании антибиотикограммы, так как резистентность к ним очень высока и составляет 27,3-98,4%.
Установлена высокая чувствительность культур Е. coli к карбаненемам, цефоперазон/сульбактаму и аминогликозидам (нетилмицину, амикацину и гентамицину). Вместе с тем 28,6% культур кишечной палочки были резистентны к цефтазидиму, что является опосредованным признаком наличия у этих штаммов β-лактамаз расширенного спектра — ферментов, блокирующих действие антибиотиков — β-лактамов. Лечение инфекции, обусловленной такими микроорганизмами, может быть успешным только при использовании карбапенемов, несмотря на результаты определения антибиотикорезистентности in vitro.
На основании полученных данных разработаны и внедрены в практику рациональные схемы целенаправленной антибиотикопрофилактики и антибиотикотерапии инфекционных осложнений у больных в травматолого-ортопедическом стационаре.
Профилактическое применение антибиотиков показано в тех случаях, когда имеет место микробное загрязнение области операции (подтвержденное или предполагаемое), либо проводится имплантация инородного материала, прежде всего эндопротеза. Общепризнанно, что антибиотикопрофилактику целесообразно проводить при первичной или вторичной хирургической обработке ран с обширным размозжением мягких тканей, погружном (накостном, либо внутрикостном) остеосинтезе переломов костей, эндопротезировании, ауто- и аллопластике несросшихся переломов.
В случае плановых оперативных вмешательств без использования имплантатов, удаления фиксаторов при сросшихся переломах и др. нет необходимости применять антибиотикопрофилактику. Речь идет, безусловно, о неосложненных операциях. Еще раз подчеркнем, что антибиотикопрофилактика является лишь одним и отнюдь не главенствующим компонентом в многофакторной системе предупреждения инфекции.
Антибиотикопрофилактика должна быть начата во время вводного наркоза. В неосложненных случаях продолжительность ее не превышает 24-48 ч. Цель данной процедуры — уничтожить микроорганизмы, попавшие в рану (эндогенно или экзогенно) во время оперативного вмешательства. Для продолжения лечения антибиотиками должны быть основания — наличие данных, указывающих на инфекционное неблагополучие. В этом случае речь идет уже о так называемой «периоперационной антибиотикотерапии».
В схемы антибиотикопрофилактики оппортунистических инфекций при лечении пациентов травматолого-ортопедического стационара целесообразно включать цефалоспорины второго (цефуроксим) и третьего (цефтриаксон) поколений, защищенные аминопенициллины, в частности амоксициллин/клавуланат.
При необходимости проведения эмпирической терапии назначают препараты с учетом развития у больного гнойно-воспалительного процесса, его характера и локализации. В этой ситуации речь идет о периоперационной терапии, и при обнаружении грамположительных возбудителей инфекции рекомендуется применять линезолид и ванкомицин, если грамотрицательные — препараты различных групп, включая карбапенемы. Возможен вариант комбинированной терапии.
Назначение нескольких антибиотиков одновременно базируется всегда на результатах микробиологического исследования и анализа клинической ситуации, когда есть основания предполагать, что в качестве возбудителей инфекции выступают различные виды бактерий, в том числе анаэробные, или сочетание бактерий и грибов.
Таким образом, проведение на современном методическом и техническом уровне микробиологического мониторинга материала от больных в травматолого-ортопедической клинике позволяет своевременно установить микробную этиологию осложнения и выбрать наиболее эффективный препарат по результатам определения антибиотикорезистентности. Комплексная оценка состояния больного в динамике, возможная при тесном сотрудничестве лечащего врача и микробиолога, является основой оптимизации антимикробной профилактики и терапии у травматолого-ортопедических больных различных категорий.
- Читать далее "Инфекционный бурсит как гнойно-воспалительное заболевание и осложнение"
Редактор: Искандер Милевски. Дата публикации: 15.7.2020
- Фурункул и карбункул как форма острой инфекции мягких тканей
- Раневые внутрибольничные инфекции (ВБИ)
- Причины раневой инфекции (этиология и патогенез)
- Возбудители оппортунистических инфекций в травматолого-ортопедических клиниках
- Лечение, профилактика инфекций у травматологических и ортопедических пациентов
- Инфекционный бурсит как гнойно-воспалительное заболевание и осложнение
- Инфекционный артрит как гнойно-воспалительное заболевание и осложнение
- Остеомиелит как гнойно-воспалительное заболевание и осложнение
- Инфекция протезированного сустава как гнойно-воспалительное заболевание и осложнение
- Группы оппортунистических микроорганизмов вызывающие инфекции при ожоговой травме
